Framleiðslu ónæmis í slímhúð með lungnagjöf á nanóögnum sem miðar á frumu
Jul 05, 2023
ÁSTANDUR
Við komumst áður að því að nanóögn smíðuð með mótefnavaka, bensalkónklóríði (BK) og c-fjölglútamínsýru (c-PGA) sýndi mikla ónæmisörvun Th1 og Th2-gerð eftir gjöf undir húð. Til að fyrirbyggja öndunarfærasýkingar ætti hins vegar að framkalla ónæmi slímhúðar. Í þessari rannsókn könnuðum við áhrif lungnagjafar nanóagna sem samanstendur af ovalbumin (OVA) sem mótefnavaka fyrirmynd, BK og c-PGA á framköllun slímhúðarónæmis í lungum og sermi.
Fléttan var sterklega tekin upp af RAW264.7 og DC2.4 frumum. Eftir lungnagjöf var lungnateymsla lengri fyrir OVA/BK/c-PGA flókið en fyrir OVA eitt sér. OVA-sértækt immúnóglóbúlín (Ig)G í sermi var mjög framkallað af fléttunni. Hátt IgG- og IgA-gildi voru einnig framkölluð í berkju- og lungnaskolunarvökvanum og in vivo komu ekki fram eiturverkanir. Að lokum, við framkölluðum slímhúðarónæmi á áhrifaríkan og öruggan hátt með gjöf OVA/BK/c-PGA flóka í lungum.
Á undanförnum árum hafa fleiri og fleiri rannsóknir sýnt að slímhúðarónæmi gegnir mikilvægu hlutverki í ónæmiskerfi líkamans. Slímhúðarónæmi vísar til ónæmiskerfis mannslíkamans sem byggir á slímhimnu og varnargeta þess miðar aðallega að innrás sýkla í slímhúð manna eins og öndunarfæri, meltingarveg og æxlunarfæri.
Sjálft slímhúðarónæmi gerir líkamann ekki ónæmari, en það getur hjálpað líkama okkar að takast á við innrás erlendra sýkla á skilvirkari hátt. Með því að örva stöðugt ónæmi slímhúðar framleiðir líkami okkar fleiri mótefni, sem eykur ónæmi okkar.
Svo, hvernig er hægt að örva ónæmi slímhúðar? Hér eru nokkrar tillögur:
1. Fáðu þér nóg af C-vítamíni. C-vítamín er náttúrulegt andoxunarefni sem eykur starfsemi ónæmisfrumna, sem hjálpar til við að berjast gegn sýkingum. Ávextir og grænt laufgrænmeti eins og sítrónur, appelsínur og jarðarber eru rík af C-vítamíni.
2. Auka inntöku mjólkursýrugerla. Mjólkursýrugerlar geta stuðlað að jafnvægi í þarmaflóru og hindrað vöxt skaðlegra baktería. Algeng matvæli fyrir mjólkursýrubakteríur eru jógúrt, súrkál, kimchi osfrv.
3. Æfðu þig í öndun Djúpt andardráttur. Djúp öndun eykur súrefnisframboð og loftræstingu til lungna, sem getur hjálpað til við að fjarlægja uppsafnaða sýkla úr lungunum.
Í stuttu máli, örvun slímhúðarónæmis er mikilvæg leið til að bæta ónæmi. Við ættum að reyna okkar besta til að bæta slímhúðarónæmi okkar með mataræði og lífsvenjum, til að vernda heilsu okkar. Frá þessu sjónarhorni þurfum við að bæta friðhelgi. Cistanche getur bætt friðhelgi verulega vegna þess að kjötaska inniheldur margs konar líffræðilega virka efnisþætti, eins og fjölsykrur, tvo sveppi og Huang Li, sem geta örvað ónæmiskerfið. Ýmsar tegundir frumna, auka ónæmisvirkni þeirra.

Smelltu cistanche deserticola viðbót
1. Inngangur
Bráðar öndunarfærasýkingar eru næstum örugglega helsta dánarorsök barna < 5 ára í þróunarlöndum (Williams o.fl., 2002). Nokkur bóluefni, eins og bóluefni gegn inflúensu, kíghósta og pneumókokkum, hafa verið þróuð við öndunarfærasýkingum (White, 1988; Pittman, 1991; Chen o.fl., 2020). Flest þessara bóluefna eru gefin í vöðva og undir húð, sem gæti í raun framkallað sermi immúnóglóbúlín (Ig)G. Hins vegar eru aðrar leiðir gagnlegar til að örva slímhúðarónæmi til að koma í veg fyrir bráðar öndunarfærasýkingar. Greint hefur verið frá slímhúðargjöfum, svo sem í nef og lungum, til að framkalla IgA í slímhúð á áhrifaríkan hátt og koma í veg fyrir öndunarfærasýkingar (Giri o.fl., 2005; Ainai o.fl., 2017).
Á hinn bóginn ættu bóluefni til gjafar í nef og lungum ekki að innihalda hjálparefni sem tilkynnt hefur verið um að valdi bólguviðbrögðum og sáramyndun á lyfjagjafastaðnum (Tamura o.fl., 1988; McKee o.fl., 2007). Önnur aðferð til að bæta virkni bóluefna án hjálparefna er að þróa kerfi sem getur skilað bóluefnum á áhrifaríkan hátt inn í frumur sem gefa mótefnavaka í slímhúð (APC).
Í fyrri rannsókn þróuðum við nýjan bóluefnisferju sem var smíðaður með mótefnavaka, bensalkónklóríði (BK) og c-fjölglútamínsýru (c-PGA). Flétta sem samanstendur af ovalbumin (OVA) sem fyrirmynd mótefnavaka, BK og c-PGA (OVA/BK/c-PGA flókið) skilaði OVA á áhrifaríkan hátt inn í tannfrumur og bætti OVA-sértæka IgG-örvun í sermi eftir gjöf undir húð í músum (Kurosaki o.fl. ., 2012). Þessi rannsókn miðar að því að kanna áhrif lungnagjafar á OVA/BK/c-PGA flóknu á framköllun slímhúðarónæmis í lungum og sermi.
2. Efni og aðferðir
2.1. Efni
OVA var keypt frá Sigma-Aldrich (St. Louis, MO, Bandaríkjunum). BK var fengið frá Nacalai Tesque, Inc. (Kyoto, Japan). c-PGA var útvegað af Yakult Pharmaceutical Industry Co., Ltd. (Tókýó, Japan). Fluorescein ísóþíósýanat-merkt OVA (FITC-OVA) og Alexa Fluor 647-merkt OVA (Alexa647- OVA) var fengið frá Invitrogen (Carls, CA, Bandaríkjunum). Fósturnautasermi (FBS) var keypt frá Biological Industries Ltd. (Kibbutz Beit Haemek, Ísrael). OPTI-MEM I var fengin frá GIBCO BRL (Grand Island, NY, Bandaríkjunum), og forblönduð sýklalyfjalausn sem innihélt penicillín, streptómýsín og L-glútamín var fengin frá Wako Pure Chemical Industries, Ltd. (Osaka, Japan). Dulbecco's Modified Eagle Medium (DMEM) og RPMI1640 miðill voru fengin frá Nissui Pharmaceutical Co., Ltd. (Tokyo, Japan).
2.2. Flókinn undirbúningur
Áður bjuggum við til OVA/BK/c-PGA flókið í þyngdarhlutfallinu 1:0.2:0.2 (Kurosaki o.fl., 2012). Til að undirbúa OVA/BK flókið var viðeigandi magni af BK lausn (pH 5.0) leyst upp í 5 prósent glúkósa blandað saman við OVA lausn (pH 7.0) leyst upp í 5 prósent glúkósa og látið standa í 15 mínútur við 4 C. Til að húða OVA/BK flókið með c-PGA var c-PGA lausn (pH 7,0) uppleyst í 5 prósent glúkósa bætt við OVA/BK flókið og látið standa í 15 mínútur til viðbótar kl. 4 C. Kornastærð og f-möguleiki hvers fléttu var mældur með því að nota Zetasiser Nano ZS (Malvern Instruments, Ltd., Malvern, Bretlandi).
2.3. Frumur
Músaátfrumufrumulína RAW264.7 og dendritic frumulína DC2.4 voru notuð. RAW264.7 frumur voru ræktaðar í DMEM bætt við 10 prósent FBS og sýklalyfjum. DC2.4 frumur voru ræktaðar í RPMI1640 æti sem bætt var við 10 prósent FBS, sýklalyfjum, 1 mM ónauðsynlegum amínósýrum og 1 nM 2-merkaptóetanóli. Þessar frumur voru metnar undir rakaðri andrúmslofti með 5 prósent CO2 í lofti við 37C.

2.4. In vitro frumuupptöku tilraun
RAW264.7 frumur og DC2.4 frumur voru húðaðar á 24-brunnsplötur (Corning, NY, USA) með þéttleikanum 2.0 104 frumur/holu og ræktaðar í 50{ {21}} ml af ræktunarmiðli. Eftir 24- klst. forræktun var efnið skipt út fyrir OPTI-MEM I miðli og frumurnar voru ræktaðar með 5 mg FITC-OVA og flókið sem innihélt 5 mg FITC-OVA í 2 klst. Eftir ræktun voru þessar frumur þvegnar með PBS og skoðaðar í flúrljómandi smásjá (BIOREVO BZ-9000; Keyence Co., Osaka, Japan). Eftir athugun voru þessar frumur lýsaðar í 300 l af leysingarjafna (pH 7,8 og 0,1 M Tris/HCl jafnalausn sem inniheldur 0,05 prósent Triton X-100 og 2 mM EDTA). Lysötin voru sett í 96-brunnsplötur og flúrljómun FITC-OVA var mæld við losunarbylgjulengd 530 nm með örvunarbylgjulengd 480 nm, með því að nota flúorómetrískan örplötulesara (Infinite-200Pro M-Plex, Tecan Japan Co., Ltd., Kanagawa, Japan). Próteininnihald lysatsins var ákvarðað með Bradford prófun með því að nota BSA sem staðal. Frásog var mæld með því að nota örplötulesarann við 570 nm. Upptaka FITC-OVA var sýnd sem mg á hvert mg prótein.
2.5. Dýr
Dýraumönnun og tilraunaaðgerðir voru framkvæmdar af leiðbeiningum um dýratilraunir Nagasaki háskólans með samþykki frá dýraumönnunar- og notkunarnefndinni. Karlkyns C57BL/6N mýs (5 vikna gamlar) voru keyptar frá Japan SLC (Shizuoka, Japan). Eftir að hafa verið flutt var músunum leyft að aðlagast nýju umhverfi sínu í 1 dag fyrir tilraunirnar. Lungnagjöf (40 ml) var framkvæmd með því að nota tungubælandi með ljósi með sjálfvirkri öndun í músum sem svæfðar voru með innöndun á ísóflurani (Horiguchi o.fl., 2015).
2.6. Lungnasöfnun flókinna
Til að kanna uppsöfnun OVA var 40 mg Alexa647-OVA og flókið sem innihélt 40 mg Alexa647- OVA í rúmmáli 40 ml á mús gefið í mýs með lungnaleið. Sex dögum eftir gjöfina var músum fórnað og lungun krufin. Flúrljómunarstyrkur Alexa647-OVA í músarlunga sást með Xenogen IVIS Lumina System ásamt Living Image hugbúnaði til gagnaöflunar (Xenogen, Co, Almeda, CA, USA). Eftir athugunina voru þessi lungu gerð einsleit með lýsisbuffi og einsleitt efni skilið í skilvindu við 15,000 snúninga á mínútu (Kubota-3500, Kubota Corporation, Tókýó, Japan) í 5 mínútur og flúrljómun Alexa647 í þeim flotefnum var ákvarðað með örplötuleiðara við örvun og útblástursbylgjulengd 640 og 670 nm, í sömu röð.
2.7. Ónæmisaðgerð
Mýs voru bólusettar með 5 prósenta glúkósalausn, 40 mg OVA, tómu fléttu af 8 mg BK og 8 mg c-PGA (fartæki) og OVA/BK/c-PGA fléttu sem innihélt 40 mg OVA með lungnagjöf, 4 sinnum vikulega. Tveimur vikum eftir síðustu bólusetningu fékkst berkjualveolar lavage fluid (BALF) og sermi. BALF og sermi voru notuð fyrir ensímtengd ónæmissogandi próf (ELISA) próf.
2.8. Ákvörðun örvunar á OVA-sértækum mótefnum
Fyrir OVA húðun var 100 ml af OVA lausn (10 mg/ml, í 1 M natríumvetniskarbónati) bætt við hvern brunn af ELISA plötunum (Thermo Fisher Scientific Inc., Waltham, MA, Bandaríkjunum) og ræktaðar yfir nótt við 4 C. Plöturnar voru þvegnar þrisvar sinnum með fosfat-buffuðum saltvatni sem innihélt 0,05 prósent Tween-20 (PBST), 200 ml af blokkandi hvarfefni N 102 (Nichiyu, Co., Ltd., Tókýó, Japan Bætt við til að hindra ósértæka bindingu og síðan ræktuð í 6 klst við 4 C. Plöturnar voru þvegnar tvisvar með PBST. Síðan var 100 ml skammtar af 1000-falt þynntu sermi og óþynntu BALF sýni bætt í hvern brunn og ræktuð yfir nótt við 4 C. Eftir fimm sinnum þvott með PBST, 100 ml af hverri af piparrótarperoxídasa (HRP) – samtengdu geitamótefni -mús IgG, IgA, IgM, IgE, IgG1, IgG2a, IgG2b og IgG3 (1:10,000) (Abcam, Cambridge, Bretlandi) – var bætt í hvern brunn og ræktað við stofuhita í 1 klst. síðan þvegið fimm sinnum með PBST. TMB Ein lausn (Promega, WI, USA) var notuð og útbúin samkvæmt leiðbeiningum framleiðanda. Hvarfið var síðan stöðvað eftir 15 mínútur með því að bæta við 1 N saltsýru. Frásog var lesið við 450 nm með því að nota örplötulesara.
2.9. In vivo eiturhrif OVA/BK/c-PGA flókins
OVA og OVA/BK/c-PGA flókið var gefið músum með lungnaleið. BALF fékkst 3 og 24 klst. eftir gjöf frá músum. Tuttugu og fjórum tímum eftir gjöf var lungað einnig krufið. Virkni laktat dehýdrógenasa (LDH) í BALF var mæld með því að nota QuantiChromTM laktat dehýdrógenasa Kit (BioAssay Systems, CA, USA) samkvæmt leiðbeiningum verksmiðjunnar. Lungnasýnin voru fest í 4 prósenta paraformaldehýðfosfatjafnalausn. Skurðskurðurinn og hematoxýlín-eósín (HE) litunin var falin GenoStaff (Tókýó, Japan). HE-litaðir hlutar lungna sáust með smásjá við 20 stækkun.
2.10. tölfræðigreining
Tölfræðileg marktækni mismunar milli hópanna tveggja var metin með því að framkvæma t-próf nemenda. Margfaldur samanburður meðal hópanna var gerður með því að framkvæma Tukey prófið. p-gildi < .05 voru talin gefa vísbendingu um tölfræðilega marktekt.
3. Úrslit
3.1. Eðlisefnafræðilegir eiginleikar fléttunnar
Við smíðuðum anjóníska OVA/BK/c-PGA flókið í þyngdarhlutfallinu 1:0.2:0.2. C-PGA-húðaða flókið var með kornastærð um það bil 105,4 nm og f-getu upp á um það bil 35,5 mV.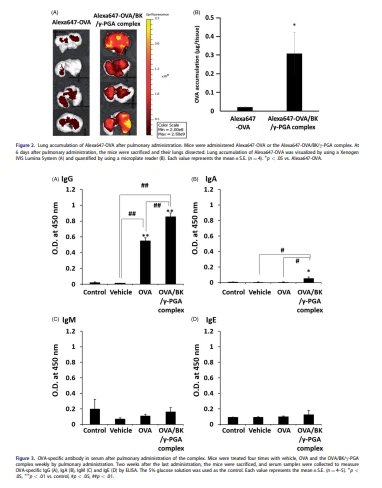

3.2. Frumuupptaka fléttunnar
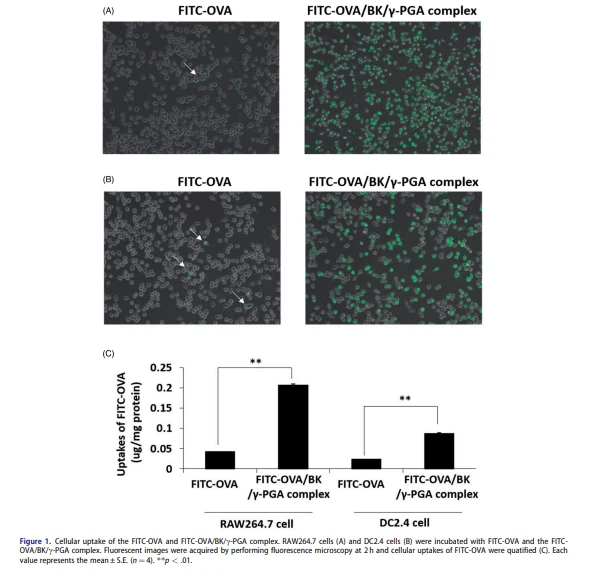
RAW264.7 frumur og DC2.4 frumur voru meðhöndlaðar með FITC-OVA og FITC-OVA/BK/c-PGA fléttu og frumuupptaka FITC-OVA var sýnd, eins og sýnt er á mynd 1. FITC-OVA/BK/ c-PGA flókið var mjög tekið af RAW264.7 frumunum og DC2.4 frumunum og sterk græn flúrljómun FITC-OVA sást (mynd 1 (A, B), í sömu röð). Á sama tíma sást lítið magn af FITC-OVA í báðum frumum sem voru meðhöndlaðar með FITC-OVA.
Frumuupptaka FITC-OVA var magngreind í RAW264.7 frumum og DC2.4 frumum (Mynd 1(C)). FITC-OVA/BK/c-PGA flókið sýndi marktækt meiri upptöku en FITC-OVA í báðum frumum (p <.01).
3.3. Lungnasöfnun Alexa647-OVA eftir lungnagjöf
Alexa647-OVA og Alexa647-OVA/BK/c-PGA flókið var gefið músum með lungnaleið til að ákvarða lungnauppsöfnun Alexa647-OVA sem mótefnavaka. 6 dögum eftir gjöf voru lungun krufin og flúrljómunarstyrkur þeirra sýndur með því að nota Xenogen IVIS Lumina System. Ex-vivo flúrljómandi mynd er sýnd á mynd 2(A). Mikill flúrljómunarstyrkur sást í öllu lungunni 6 dögum eftir gjöf í lungum, þó engin flúrljómun hafi verið í milta, hjarta, nýrum og lifur (gögn ekki sýnd). Lungnasöfnun var meiri fyrir Alexa647-OVA/BK/c-PGA flókið en fyrir Alexa647-OVA á degi 6. Eins og sést á mynd 2(B), var lungnasöfnun marktækt meiri fyrir Alexa 647-OVA/BK/c-PGA flókið en fyrir Alexa647- OVA (p < .05).

3.4. OVA-sértækt mótefni í sermi eftir lungnagjöf á fléttunni
5 prósent glúkósalausn, BK/c-PGA flókið (fartæki), OVA og OVA/BK/c-PGA flókið var gefið með lungnaleiðinni í mýs fjórum sinnum, og síðan OVA-sértæk IgG, IgA, IgM, og IgE voru ákvörðuð með ELISA eins og sýnt er á mynd 3. Lungnagjöf OVA og OVA/BK/c-PGA flókið jók IgG gildi í músum, þó að OVA sértækt IgG hafi ekki fundist í músum sem fengu 5 prósent glúkósa og burðarefni. Ennfremur var IgG og IgA framleiðsla marktækt meiri eftir gjöf OVA/BK/c-PGA flóksins en eftir gjöf OVA (p < .05 eða .01). Aftur á móti voru OVA-sértæk IgM og IgE ekki framkölluð af OVA eða OVA/BK/c-PGA fléttunni.

3.5. OVA-sértækt mótefni í BALF eftir lungnagjöf á fléttunni
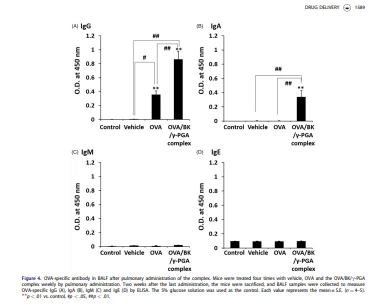
OVA-sértæk IgG, IgA, IgM og IgE í BALF voru einnig ákvörðuð, eins og sýnt er á mynd 4. Magn IgG jókst marktækt með OVA miðað við magn eftir gjöf viðmiðunar og burðarefnis (p < 0,05 eða .01). Engu að síður jók OVA/BK/c-PGA flókið marktækt, ekki aðeins IgG heldur einnig IgA í BALF (p < .01). Hins vegar var OVA-sértækt IgM og IgE ekki framkallað af OVA eða OVA/BK/c-PGA fléttunni.
3.6. IgG undirgerðir í sermi eftir lungnagjöf á fléttunni
Örvunaráhrif OVA-sértækra IgG undirtegunda, eins og IgG1, IgG2a, IgG2b og IgG3 í sermi voru ákvörðuð eins og sýnt er á mynd 5. Samanborið við samanburðinn og burðarefnið, jók OVA marktækt aðeins IgG1 (p <.01). Mótefnamagn allra undirtegunda framkallað af OVA/BK/c-PGA flókinu var marktækt hærra en gildið sem var framkallað af samanburði og burðarefni (p < 0,05 eða 0,01).
3.7. IgG undirgerðir í BALF eftir lungnagjöf á fléttunni
OVA-sértækar IgG undirgerðir, eins og IgG1, IgG2a, IgG2b og IgG3 í BALF voru einnig ákvarðaðar, eins og sýnt er á mynd 6. OVA jók aðeins marktækt IgG1 gildi miðað við það sem var framkallað af samanburði og burðarefni (p < 0,01) . Samanborið við samanburðinn, burðarefnið og OVA, olli OVA/BK/c-PGA flókið marktækt hærra mótefnamagn allra undirtegunda (p < 0,05 eða 0,01).

3.8. In vivo eiturhrif OVA/BK/c-PGA flókins
Músum var gefið 5 prósent glúkósalausn, OVA og OVA/BK/c-PGA flókið. LDH virkni í BALF var ákvörðuð 3 eða 24 klst. eftir gjöf (Mynd 7). Gjöf OVA og OVA/BK/c-PGA flóka hafði lítil áhrif á LDH gildi í BALF.
Tuttugu og fjórum klukkustundum eftir gjöf voru lungun krufin úr þessum músum til vefjafræðilegrar greiningar. HE-litaðir lungnaskurðir eru sýndir á mynd 8. Engin vefjafræðileg frávik komu fram í músunum sem fengu OVA og OVA/BK/c-PGA flókið.
4. Umræður
Lungað stjórnar öndun og verður fyrir mörgum sýkingum, svo sem veirum og bakteríum sem valda öndunarfærasýkingum. Þessir sýklar sýkjast í gegnum slímhúð lungna, þannig að slímhúðarónæmi verður að vera framkallað til að vernda gegn öndunarfærasýkingum. Koma í veg fyrir öndunarfærasýkingar, ónæmi slímhúðar gegnir mikilvægu hlutverki; þó getur gjöf bóluefnisins í húð og í vöðva ekki örvað ónæmi slímhúðarinnar verulega (Ito o.fl., 2003; Amorij o.fl., 2007). Ónæmiskerfið í slímhúðinni sem framkallar seytandi IgA er þróað á yfirborði slímhúðarinnar. Tilkynnt hefur verið um nokkrar APC, svo sem tannfrumur og átfrumur, staðsettar á yfirborði slímhúðarinnar (Kopf o.fl., 2015). Ennfremur er berkjutengdur eitilvefur (BALT) að finna í berkjuslímhúðinni og er eitilfrumur sem gegnir aðalhlutverki í ónæmi öndunarfæra slímhúðarinnar (Bienenstock, 1980). Gert er ráð fyrir að lungnagjöf bóluefnisins örvi ónæmiskerfið í slímhúðinni á áhrifaríkan hátt. Þess vegna smíðuðum við OVA/BK/c-PGA flókið til að meta notagildi þess sem bóluefni gefið með lungnaleiðinni.
Mynd 4 sýnir BALF styrk OVA-sértækra mótefna eftir lungnagjöf á OVA og OVA/BK/c-PGA flókinu. Gjöf OVA í lungum jók IgG en hafði lítil áhrif á IgA í BALF. Á hinn bóginn olli OVA/BK/c-PGA flókið marktækt IgA seytingu í BALF. Ennfremur var IgG-örvun í sermi marktækt meiri eftir gjöf OVA/BK/c-PGA flókins en eftir gjöf OVA (Mynd 3). Serum IgG er mikilvægt til að koma í veg fyrir versnun sýkinga sem eiga sér stað (Huber o.fl., 2006; Schroeder & Cavacini, 2010). Niðurstöðurnar benda til þess að OVA/BK/c-PGA flókið gæti komið í veg fyrir öndunarfærasýkingar með mikilli IgA örvun í slímhúð og versnun öndunarfærasýkingar með mikilli IgG framkalla í sermi. Ennfremur sást ekki IgE örvun af völdum OVA/BK/c-PGA fléttunnar og þessi niðurstaða gaf til kynna litla hættu á ofnæmisviðbrögðum af völdum OVA/BK/c-PGA fléttunnar.
OVA/BK/c-PGA flókið gæti einnig framkallað ekki aðeins IgG1 og IgG2b heldur einnig IgG2a og IgG3 (Mynd 5). IgG1 og IgG2b eru þekkt sem Th2-gerð immúnóglóbúlín sem miðla húmoral ónæmissvörun, og IgG2a og IgG3 eru þekkt sem Th1-gerð immúnóglóbúlín sem miðla frumuónæmissvörun (Firacative o.fl., 2018) . Þess vegna gæti OVA/BK/c-PGA flókið framkallað bæði húmor og frumu ónæmissvörun. Þessar niðurstöður benda til þess að þetta kerfi gæti verið gagnlegt fyrir bóluefni gegn sýkingum sem og krabbameinum. Meta skal fyrirbyggjandi áhrif, mótefnavaka-framkallaða Th1- og Th2-gerð frumtýkínsvörun í framkallanlegum BALT, Treg þýði og IL-10 örvun með því að nota raunverulega mótefnavaka frá sýkingum eða krabbameinum í framtíðinni nám.
Hin sterka örvun OVA/BK/c-PGA samstæðunnar á ónæmissvöruninni hlýtur að stafa af mikilli varðveislu fléttunnar í lungum og skilvirkri afhendingu OVA inn í APC í lungnaslímhúðinni. Niðurstöður okkar staðfestu þetta með því að sýna að 6 dögum eftir gjöf var Alexa647-OVA/BK/c-PGA flókið eftir í lungum og sýndi marktækt hærra flúrljómun en Alexa647- OVA (Mynd 2). Fléttumyndunin gæti komið í veg fyrir útbreiðslu OVA og verndað OVA gegn niðurbroti af völdum próteasa í lungnaslímhúðinni. Ennfremur gat OVA/BK/c-PGA flókið skilað OVA á áhrifaríkan hátt inn í RAW264.7 átfrumnafrumur og DC2.4 dendritic frumur (Mynd 1). Þessar niðurstöður bentu til þess að OVA/BK/c-PGA flókið yrði tekið upp af APC í lungnablöðrum og framkallaði háa ónæmissvörun eftir gjöf í lungum. Greint hefur verið frá því að c-PGA-húðaðar nanóagnir hafi verið teknar upp af gamma-glútamýl transpeptidasa-miðluðum innfrumuleið (Du o.fl., 2015). Við staðfestum einnig að c-PGA-húðuðu nanóagnirnar voru teknar upp af c-PGA-sértæku innfrumuleiðinni (Kurosaki o.fl., 2009). OVA/BK/c-PGA flókið gæti verið tekið upp af APC í lungum með sömu aðferðum. Hins vegar er enn ekki ljóst hvaða frumur eru ábyrgar fyrir OVA upptöku og síðari mótefnavakakynningu í framkalli sértæks ónæmis. Frekari rannsóknir á nákvæmum ónæmisörvunaraðferðum ættu að fara fram í framtíðinni.


Mörg hjálparefni hafa verið þróuð til að auka virkni bóluefna; þó hefur verið greint frá því að hjálparefni valdi bólguviðbrögðum á stungustað (Tamura o.fl., 1988; McKee o.fl., 2007). Þess vegna gæti gjöf hjálparefna í lungun valdið alvarlegum aukaverkunum, svo sem lungnabólgu. Eftir lungnagjöf á OVA/BK/c-PGA fléttunni jókst LDH gildi í BALF ekki (Mynd 7) og vefjafræðileg frávik komu ekki fram í HE-litaða hlutanum (Mynd 8). Að sögn er c-PGA lífsamrýmanleg og niðurbrjótanleg fjölliða sem sýnir ekki ónæmisbólguviðbrögð (Prodhomme o.fl., 2003; Ye o.fl., 2006). BK er öruggt fjórðungs ammoníumefnasamband sem hefur verið mikið notað klínískt sem sýklalyfjaaukefni (Marple o.fl., 2004). Þessar skýrslur styðja einnig öryggi OVA/BK/c-PGA samstæðunnar. Á hinn bóginn sáust hærra LDH gildi 3 klst. eftir lungnagjöf en 24 klst., jafnvel í samanburðarhópnum. Þessar niðurstöður gefa til kynna að lítilsháttar erting hafi stafað af lungnagjöf. Frekari öryggisrannsókna er þörf áður en OVA/BK/c-PGA flókið er notað klínískt.
Í þessari rannsókn sýndum við fram á mikla örvun ónæmiskerfis í slímhúð með nýrri bóluefnisafhendingarferju sem er smíðaður með mótefnavakapróteini, BK og c-PGA eftir gjöf í lungum. Kerfið er hægt að nota fyrir bóluefni gegn ýmsum öndunarfærasýkingum.

Yfirlýsing um upplýsingagjöf
Ekki var greint frá hugsanlegum hagsmunaárekstrum af höfundi/höfundum.
Fjármögnun
Þessi vinna var studd af Japan Society for the Promotion of Science (JSPS) KAKENHI undir styrkjum [JP20K12649 og JP20K07156].
Heimildir
1.Ainai A, Suzuki T, Tamura SI, o.fl. (2017). Innrennslisgjöf heils óvirkjuðs inflúensuveirubóluefnis sem efnilegur inflúensubóluefnisframbjóðandi. Veiruimmunól 30:451–62.
2.Amorij JP, Saluja V, Petersen AH, et al. (2007). Lungnagjöf á inúlín-stöðuguðu inflúensu-undireiningarbóluefni sem er búið til með úða-frystiþurrkun framkallar kerfisbundin, slímhúðarhúmors- og frumumiðlað ónæmissvörun í BALB/c músum. Bóluefni 25:8707–17.
3.Bienenstock J. (1980). Berkjutengdur eitilvefur og uppspretta frumna sem innihalda immúnóglóbúlín í slímhúðinni. Environ Health Perspect 35:39–42.
4.Chen JR, Liu YM, Tseng YC, o.fl. (2020). Betri inflúensubóluefni: sjónarhorn iðnaðarins. J Biomed Sci 27:11.
5. Du X, Xiong L, Dai S, o.fl. (2015). c-PGA-húðaðar mesoporous kísil nanóagnir með samgildum tengdum forlyfjum fyrir aukna frumuupptöku og innanfrumu GSH-svarandi losun. Adv Healthc Mater 4: 771–81.
6. Firacative C, Gressler AE, Schubert K, o.fl. (2018). Auðkenning T-hjálpar (Th)1- og Th2-tengdra mótefnavaka cryptococcus neoformans í múslíkani af lungnasýkingu. Sci Rep 8:14.
7. Giri PK, Sable SB, Verma I, o.fl. (2005). Samanburðarmat á bólusetningarleið í nef og undir húð fyrir þróun slímhúðarbóluefnis gegn tilraunaberklum. FEMS Immunol Med Microbiol 45:87–93.
8. Horiguchi M, Oiso Y, Sakai H, o.fl. (2015). Lungnagjöf á fosfóínósítíð 3-kínasahemli er læknandi meðferð við langvinnri lungnateppu með endurnýjun lungnablöðru. J Control Release 213:112–9.
9. Huber VC, McKeon RM, Brackin MN, o.fl. (2006). Sérstakt framlag bóluefnis-framkallaðs immúnóglóbúlíns G1 (IgG1) og IgG2a mótefna til verndar ónæmis gegn inflúensu. Clin Vaccine Immunol 13: 981-90.
10. Ito R, Ozaki YA, Yoshikawa T, o.fl. (2003). Hlutverk and-hemagglutinin IgA og IgG mótefna á mismunandi stöðum í öndunarvegi bólusettra músa við að koma í veg fyrir banvæna inflúensulungnabólgu. Bóluefni 21:2362–71.
11.Kopf M, Schneider C, Nobs SP. (2015). Þróun og virkni átfrumna sem búa í lungum og tannfruma. Nat Immunol 16: 36–44.
12.Kurosaki T, Kitahara T, Fumoto S, o.fl. (2009). Þrír fléttur pDNA, pólýetýlenimíns og gamma-fjölglútamínsýru fyrir genasendingarkerfi. Lífefni 30:2846–53.
13.Kurosaki T, Kitahara T, Nakamura T, o.fl. (2012). Þróun árangursríks krabbameinsbóluefnis með því að nota miðunarkerfi mótefnavakapróteins til APCs. Pharm Res 29:483–9.
14. Marple B, Roland P, Benninger M. (2004). Öryggisskoðun á bensalkónklóríði sem notað er sem rotvarnarefni í lausnum í nef: yfirlit yfir misvísandi gögn og skoðanir. Otolaryngol Head Neck Surg 130: 131–41.
15.McKee AS, Munks MW, Marrack P. (2007). Hvernig virka hjálparefni? Mikilvægt atriði fyrir ný kynslóð ónæmisglæða. Ónæmi 27: 687–90.
For more information:1950477648nn@gmail.com
