DNA metýlóm og umskrift auðkennd lykilgen og leiðir sem taka þátt í myndun flekkóttra eggjaskelja í öldruðum varphænum
Dec 21, 2023
Ágrip
Bakgrunnur
Gæði eggjaskurn alifugla eru nátengd arðsemi eggjaframleiðslu. Eggskeljarflekkir endurspegla mikilvægan gæðaeiginleika sem hefur áhrif á útlit eggja og óskir viðskiptavina. Hins vegar er aðferðin við myndun flekkja enn illa skilin. Í þessari rannsókn bárum við kerfisbundið saman ónæmis- og andoxunarvísitölur í sermi hjá hænum sem verpa flekkóttum og eðlilegum eggjum. Umskriftar- og metýlómgreiningar voru notaðar til að útskýra hvernig eggjaskurnflögur myndast.

cistanche ávinningur fyrir karla styrkir ónæmiskerfið
Smelltu hér til að skoða Cistanche Enhance Immunity vörur
【Biðja um meira】 Netfang:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Niðurstöður
Niðurstöðurnar sýndu að sjö mismunandi tjáð gen (DEGs) voru auðkennd á milli eðlilegra og flekkóttra hópa. Genasett auðgunargreining (GSEA) leiddi í ljós að tjáðu genin voru aðallega auðguð í kalsíumboðaleiðinni, brennidepli viðloðun og MAPK merkjaleiðinni. Að auki fundust 282 differential methylated gen (DMG), þar af 15 gen sem tengdust öldrun, þar á meðal ARNTL, CAV1 og GCLC. Ferðagreining sýndi að DMGs tengdust T-frumumiðluðu ónæmi, svörun við oxunarálagi og frumuviðbrögðum við DNA-skemmdaörvun. Samþætt greining á umrita- og DNA metýleringargögnum benti á BFSP2 sem eina genið sem skarast, sem var tjáð í litlu magni og vanmetýlerað í flekkhópnum.
Ályktanir
Á heildina litið benda þessar niðurstöður til þess að öldrunar- og ónæmistengd gen og ferlar gegna mikilvægu hlutverki í myndun flekkóttra eggjaskurna og veita gagnlegar upplýsingar til að bæta gæði eggjaskurnanna.

cistanche tubulosa-bæta ónæmiskerfið
Leitarorð
Varphænur, flekkótt egg, transcriptome, DNA metýlering, ónæmi
Bakgrunnur
Alifuglaegg eru ein mikilvægasta próteingjafinn og tiltölulega lágur kostnaður þeirra gerir þau vinsæl meðal neytenda. Undanfarna fjóra áratugi hefur eggjaframleiðsla batnað verulega vegna þróunar sérhæfðra eggjakynja og erfðavals, með það að markmiði að "fæða varphænur í 100 vikur til að framleiða 500 egg" [ 1, 2]. Hins vegar hefur það takmörkuð að ná þessu markmiði vegna hægfara hnignunar á gæðum eggjaskurnanna og lífeðlisfræði sem tengist öldrun hænsna, sem hefur í för með sér aukna eggjaskurnþyngd, ljósari eggjaskurnalit og flekkótta eggjaskurn [3]. Rauðbrúni flekkurinn, mikilvægur gæðaeiginleiki eggjaskurnarinnar, kemur oft fram á beitta enda brúnu eggjaskurnarinnar, sem hefur töluverð áhrif á útlit eggja og óskir viðskiptavina. Hve mikil eggjaskurn er metin með stigaaðferð. Hægt er að meta flekka eftir styrkleika litarefnis, dreifingu og flekastærð [4]. Þar að auki er arfgengi flekkóttra eggjaskurna á bilinu 0,15–0,2, sem gefur til kynna erfðafræðilega ákvörðun [5]. Þar að auki gaf fyrri rannsókn til kynna að eldri hænur væru með hærri tíðni flekkóttra eggjaskurna en yngri hænur og nái 20% eftir 60 vikna aldur [6]. Eggskeljakirtillinn er eggjamyndunarlíffæri sem gegnir mikilvægu hlutverki í uppbyggingu eggjaskurna og litamyndun. Við myndun eggja berst eggjarauðan í gegnum infundibulum, magnum og ísthmus og nær eggjaskurninni, sem seytir miklu magni af kalki, litarefni, naglaböndum og öðrum efnum og myndar fullkomna eggjaskurn og ytri naglaband [7–9 ]. Allar breytingar eða skemmdir á eggjaskeljarkirtlinum hafa áhrif á myndun eggjaskurna og litarefni [10–12]. DNA metýlering er ein elsta þekkta breytingaleiðin og felur í sér flutning metýlhópa á fimmta kolefnisstað cýtósíns til að mynda 5-metýlsýtósín [13]. DNA metýlering gegnir mikilvægu hlutverki í öldrunarferli dýra, stjórnar aldurstengdri genatjáningu og orsök tauga-, ónæmis- og efnaskiptasjúkdóma [14-17]. Að auki getur DNA metýlering ásamt umhverfisþáttum valdið mismunandi svipgerðum við öldrun [18]. Nokkrar flóknar svipgerðir búfjár hafa verið tengdar við DNA metýleringu [19, 20]. Nýlega hefur RNA raðgreining (RNA-seq) verið gagnleg til að sýna genin og leiðirnar sem liggja að baki eiginleikum á umritunarstigi [21-24], svo sem þróun fósturvöðva, skilvirkni fóðurs og gotstærð. Fyrri rannsókn okkar sýndi að þrátt fyrir að tilkoma flekkóttra eggjaskurna hafi ekki áhrif á frammistöðu varphænsna (óbirt gögn), geta blettir haft áhrif á útlit eggja og dregið verulega úr efnahagslegu gildi þeirra. Þar að auki eru sameindaleiðir myndun flekkóttra eggja illa skildir. Þess vegna miðar þessi rannsókn að því að skýra hvernig myndun flekkóttra eggjaskurna er með því að nota transcriptomic og DNA metýleringartækni. Þar sem flekkótt eggjaskurn er arfgeng og aldurstengd, notuðum við blöndu af umritunar- og DNA metýleringargreiningum til að kanna lykilgenin og leiðirnar sem taka þátt í myndun flekkóttra eggjaskurna. Gert er ráð fyrir að niðurstöður þessarar rannsóknar muni bæta skilning á sameindakerfi myndun eggjaskurnaeiginleika, sem væri gagnlegt fyrir dýrarækt.

Mynd 1 Venjuleg og flekkótt egg úr öldruðum varphænum. A Venjulegt egg, B Flekkótt egg
Tafla 1 Lífefnafræðilegar breytur í sermi fyrir eðlilega og flekkótta hópa

Niðurstöður
Lífefnafræðilegar breytur í sermi
A typical egg and speckled egg are shown in Fig. 1. Serum antioxidant and immune indices were measured to determine the physiological status of the laying hens. Serum biochemical parameters are listed in Table 1. Serum levels of immunoglobulin G (IgG) and immunoglobulin A (IgA) are common indicators of humoral immune function. Birds in the normal group had a higher (p = 0.028) IgA content than those in the speckle group. Superoxide dismutase (SOD), catalase (CAT), total antioxidant capacity (T-AOC), glutathione (GSH), and glutathione peroxidase (GSH-PX) are important antioxidant enzymes in the body. MDA is one of the products formed by the reaction of lipids with oxygen radicals, and its content represents the degree of lipid peroxidation. These indices are important in evaluating the oxidative stress process. However, there were no differences (p >0.05) í andoxunarbreytum á milli venjulegra og flekkóttra hópa.
Umskriftarsnið eggjaskurnsins
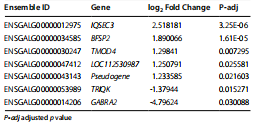
Sex cDNA söfn voru smíðuð úr flekkóttum og eðlilegum hópum. Eftir gæðaeftirlit fengust samtals 615.170.158 óunnin lestur og 604.275.600 hrein lesning (98,22% af hráum lestum). Eftir aðlögun með HISAT2 hugbúnaði var kortlagningarhlutfallið 90,75–93,18% og einstakt kortlagningarhlutfall í öllum sýnum var meira en 73,47% (viðbótartafla S3). Genatjáningarstig eru sýnd með því að nota þyrpingahitakort og aðalhlutagreiningu (PCA). Enginn marktækur munur var á genatjáningarsniðum sýna úr flekkóttum og eðlilegum hópum, þar sem sýnin mynduðu ekki sérstaka klasa (mynd 2A, B). Alls voru sjö mismunandi tjáð gen (DEGs) auðkennd á milli eðlilegra og flekkóttra hópa (p<0.05, |log2 Fold Change|>1), þar á meðal tvö uppstýrð og fimm niðurstýrð gen (tafla 2). Genasett auðgunargreining (GSEA) sýndi að fjórar leiðir auðguðust marktækt af tjáðu genum (viðbótartafla S4). Neikvæð staðlað auðgunarstig (NES) bentu til lægra tjáningarstigs fyrir suma ferla í eðlilega hópnum samanborið við þá sem voru í flekkhópnum, þar sem kalsíumboðaleiðin, taugavirkur bindill-viðtaka víxlverkun, fókusviðloðun og MAPK merkjaferillinn eru leiðirnar með lægsta tjáning (mynd 2C). Tré DEGs (BFSP2, IQSEC, TMOD4) auðkennd með RNA-seq voru staðfest með magnbundinni rauntíma PCR (qRT-PCR). Svipuð tjáning genanna þriggja var augljós með því að nota RNA-Seq og qRT-PCR, og ákvörðunarstuðullinn (R2) náði 0.93 (Mynd 2D), sem gefur til kynna að RNA-seq gögnin hafi verið áreiðanleg.
Tafla 2 Mismunandi tjáð gen (DEGs) á milli hænanna sem verpa flekkóttum og eðlilegum eggjum

Mynd 2 Umskriftarsnið eggjaskurnsins. A Hitakort af tjáningarstigum gena, B Aðalþáttagreining allra gena með því að nota DEseq2 staðlað tjáningargildi, C Þrjú dæmigerð genasett úr niðurstöðum auðgunargreiningar genasamstæðunnar, D qPCR sannprófunarniðurstöður gena sem tjáð eru með mismunandi hætti
DNA metýleringarsnið eggjaskurnsins
A total of 564,415,302 and 581,414,308 clean reads were obtained from the speckle and normal groups, respectively, after quality control (Supplementary Table S5), of which 73–78% were uniquely mapped to the converted chicken reference genome (GRCg6a). The cytosine (C) methylation rate of the six eggshell gland samples was approximately 3.4%, and the cytosine site methylation of CpG ranged from 55.5–to 63.9% in the two groups. The cytosine site methylation of CHH and CHG (H represents A, C, or T) was detected at a low proportion (0.3–0.4%) (Supplementary Table S5). Pearson correlation analysis of the CpG bases suggested that all samples were highly correlated (r>{{0}}.89) (Mynd 3A). PCA sýndi að sýni úr hópunum tveimur voru ekki marktækt ólík, þar sem þau mynduðu ekki aðskilda klasa (mynd 3B). Enginn marktækur munur var á metýlerunarstigum CG, CHG og CHH milli hópanna tveggja (mynd 3C). Hins vegar sýndi flekkhópurinn hærra CG metýlerunarstig en venjulegi hópurinn. Te endurtekið og exon svæði sýndu hæsta CG metýleringarstigið, en 5′ UTR svæðið hafði lægsta CG metýlerunarstigið (mynd 3D). Alls greindust 2788 mismunandi metýleruð svæði (DMR) á milli venjulegra og flekkóttra hópa. DMR-efnin voru aðallega staðsett í introns (47,45%), þar á eftir koma intergenic svæðinu (36,05%), exon (8,29%), promoter (5,95%), 3'-UTR (1,18%) og 5'-UTR ( 0,97%) svæði (4. mynd). Að auki voru 282 mismunandi metýleruð gen (DMGs) auðkennd, þar á meðal 172 ofmetýleruð og 74 vanmetýleruð gen á promotorsvæðinu. Þar að auki fundust 36 DMG í genalíkamanum, þar á meðal 30 ofmetýleruð gen og sex vanmetýleruð gen. Við umbreyttum DMG í réttvísa þeirra manna og fengum 158 genatákn sem voru hlaðið upp í Metascape fyrir virkniskýringar, genaverufræði (GO) og greiningar á ferlum. Genin voru auðguð í 176 GO líffræðilegum ferlum, þar á meðal stjórnun frumusvars við vaxtarþáttarörvun og T-frumumiðlað ónæmi, svörun við oxunarálagi og frumuviðbrögð við DNA-skemmdaörvun.

Mynd 3 Heildarmetýlerunarstig í hænunum sem verpa flekkóttum og eðlilegum eggjum. A Fylgnigreining á metýlerunarstigum milli sýna úr hópunum tveimur. B Aðalþáttagreining á metýleringarstigi allra sýna. C Vefrit um metýlerunarstig cýtósínstaða í hópunum tveimur. D Línurit yfir metýleringarstig mismunandi erfðamengjasvæða. Erfðafræðilegum svæðum hvers gena var skipt í 20 hólf; cýtósínsetur metýleringarstig samsvarandi starfrænna svæða allra gena var síðan meðaltal.

Mynd 4 Vísitarit af skýringu á mismunametýleruðum svæðum (DMR) í erfðafræðilegum virknisvæðum

Mynd 5 A GO skilmálar DMGs. B Tengsl genatjáningar og DNA metýleringarstigs í flekkhópnum. C Samband genatjáningar og DNA metýleringarstigs í eðlilegum hópi. D Venn skýringarmynd af genum sem skarast á milli DEG og DMG
Ferðagreining sýndi að genin auðguðust í 19 Kyoto Encyclopedia of Genes and Genomes (KEGG) ferlum, þar á meðal niðurbroti RNA, stjórnun bólgumiðlara á TRP rásum og TNF merkjaleiðinni. Þar að auki fundust 25 genasett, þar á meðal merkjasendingar frá Rho GTPase, RHO GTPase hringrásinni og CDC42 GTPase hringrásinni. Efstu 20 auðguðu verufræðiklasarnir eru sýndir á mynd 5A. Meðal 158 samhæfra mannagena voru 15 tengd öldrun eða langlífi (viðbótartafla S6). Samþætt greining á bísúlfít raðgreiningu í heilu erfðaefni (WGBS) og RNA-seq gögnum var gerð til að ákvarða sambandið milli DNA metýleringar og genatjáningarstigs (mynd 5B og C). Neikvæð fylgni var á milli DNA-metýleringar og genatjáningarstigs fyrir framan umritunarbyrjunarstaðinn (TSS) og niðurstraums umritunarlokunarstaðarins (TTS); hins vegar var engin fylgni á milli DNA metýleringar og genatjáningarstigs í genalíkamanum. Venn skýringarmyndin sýndi að BFSP2 var eina genið sem skarast á milli DMGs og DEGs (mynd 5D).
Umræða
Rannsóknir í nokkur ár hafa sýnt að myndun flekkja á eggjaskurn er arfgeng og eldri varphænur framleiða meira af flekkóttum eggjaskurnum en yngri hænur [6]. Öldrun varphænna fylgir oft langvinnri bólgu og oxunarálagi [25, 26]. Blóðbreytur dýra endurspegla lífeðlis- og næringarástand þeirra. SOD, GSH-PX, GSH, CAT og T-AOC eru þættir andoxunarvarnarkerfisins. Niðurstöður þessarar rannsóknar benda til þess að ekki hafi verið marktækur munur á andoxunargetu aldraðra hænna milli flekkótta og eðlilegra hópa, sem er andstætt niðurstöðum Moreno og Osorno [27]. Moreno greindi frá því að fuglar sem verpa eggjum með flekkóttum skeljum gætu þjáðst af lífeðlisfræðilegu álagi vegna foroxunarvirkni aðalflöguþáttarins og þola meira oxunarálag [28]. Mismuninn á niðurstöðunum mætti rekja til mismunandi tegunda sem notaðar voru í rannsóknunum.

cistanche tubulosa-bæta ónæmiskerfið
Immúnóglóbúlín eru prótein sem taka þátt í bólgueyðandi ferlum og gegna stjórnunarhlutverki í bólguviðbrögðum [29]. Fyrri rannsókn sýndi að blámeitafuglar sem verpa flekkóttum eggjum sýna lágt heildarmagn immúnóglóbúlína [30]. Að sama skapi sýndu niðurstöður þessarar rannsóknar að fuglar í flekkahópnum höfðu verulega lægri IgA-gildi í sermi samanborið við þau í venjulegum hópi, sem bendir til þess að hænur í flekkahópnum gætu haft minni bólgueyðandi hæfileika, sem er í samræmi við niðurstöður Martínez og Merino [30]. IgA, sem einn af mikilvægu vísbendingunum við að meta húmoral ónæmisvirkni alifugla, hefur veirueyðandi, bakteríudrepandi og andeiturvirkni [31]. Rannsóknir hafa sýnt að fæðubótarefni með ger-glúkani getur aukið IgA innihald í sermi. Aukið IgA innihald getur aukið getu einstaklings til að viðhalda ónæmisjafnvægi, sem leiðir til hugsanlegs heilsubótar [32]. Rannsóknir hafa einnig sýnt að eftir því sem varphænur eldast minnkar viðnám þeirra gegn utanaðkomandi sýkla [33]. Þegar sýklar koma inn í líkama aldraðra varphænna getur slímhúðvarnarkerfi eggjastokkavefsins skemmst vegna samhliða minnkunar á ónæmi [34]. Hins vegar getur hærra magn af IgA aukið getu líkamans til að viðhalda ónæmisjafnvægi, komið í veg fyrir innrás sýkla inn í undirslímhúð eggjastokksins og þannig viðhaldið góðum gæðum eggjaskurnsins. Ennfremur benti RNA-seq greining á sjö DEG á milli flekkóttra og eðlilegra hópa, þar á meðal IQSEC3, BFSP2, TMOD4, LOC112530987, GABRA2, TRIQK og gerviefni. IQSEC3, meðlimur brefeldín A-ónæmra ARF gúanín núkleótíðskiptaþátta (GEFs) fjölskyldunnar [35, 36], stuðlar að þróun hamlandi taugamóta með því að bindast við gefyrín [37]. IQSEC3 er virkni mikilvægur til að viðhalda netvirkni in vivo. IQSEC3 niðurfelling í hippocampal dentate gyrus í nagdýrum dregur úr þéttleika GABAergic taugamóta og eykur næmi fyrir alvarlegum flogum [38]. Hins vegar eru engar rannsóknir á virkni IQSEC3 í alifuglum.
Gamma-amínósmjörsýra (GABA) er helsta hamlandi taugaboðefnið í miðtaugakerfi hryggdýra [39] og getur breytt uppbyggingu viðtaka og jóna gegndræpi samsvarandi viðtaka [40]. GABA getur virkað beint á pípulaga sléttar vöðvafrumur í gegnum GABAA-R eða GABAB-R, sem eru staðsettar á eggjaleiðaraveggnum og taka þátt með því að stjórna pípulaga samdráttarhæfni í kanínum [39], mönnum [41] og rottum [42]. Rannsóknir hafa sýnt að GABRA1 gegnir mikilvægu hlutverki í eggjaframleiðslu. Mikið tjáningarmagn GABRA1 getur hamlað útbreiðslu kyrningafrumna, aukið frumudauða og hindrað myndun og seytingu prógesteróns, sem leiðir til minni eggframleiðslu [43-45]. Eggvarpstaktur varphæna er taugamótandi ferli [46, 47]. Á grundvelli þessara niðurstaðna getum við velt því fyrir okkur að það sé lúmskt samband á milli myndun eggjaskurnflekkja og taugakerfisins, þó að nákvæm tengsl krefjist frekari rannsóknar.
TMOD4, meðlimur fjölskyldu próteina sem lokar oddhvassum endum aktínþráða [48], er tjáð í beinagrindarvöðvum og hjarta [49, 50]. Rannsóknir hafa greint frá því að TMOD4 sé til staðar í fullorðnum kjúklingalinsum, rauðkornum og hröðum beinagrindvöðvaþráðum [51]. TMOD4 hefur reynst taka þátt í samsetningu vöðvafíbríla, vöðvasamdrætti og aðgreiningu [52-54]. Samdráttur eggjastokkavöðvans fær eggið til að snúast í leginu, sem gerir litarefninu kleift að setja jafnt út á yfirborð eggjaskurnsins. Við veltum því fyrir okkur að myndun flekkóttra eggja gæti tengst samdrætti eggjastokkavöðva, en frekari rannsókna er þörf. GSEA var notað til að greina líffræðilega virkni allra tjáðra gena til að forðast tap á einhverjum áhugaverðum genasettum með cutof-free stefnunni. Genin sem tjáðust voru aðallega auðguð á kalsíumboðaleiðinni, brennivídd viðloðun, MAPK merkjaleiðinni og taugavirka bindil-viðtaka samskipti. Greint hefur verið frá því að í ferli steinefnamyndunar eggjaskurna taka gen tengd kalsíumboðaleiðinni þátt í frásogi kalsíum- og karbónatjóna úr blóði og eru flutt til legvökvans um þekjufrumur eggjastokksins til að taka þátt í eggjaskurn steinefnavæðing [46, 55]. Þegar kalsíum- og karbónatjónin halda áfram að steinefna í eggjaskurninni snýst eggið stöðugt í leginu og eggjaskurn litarefni, protoporphyrin-IX, er hægt að setja jafnt á yfirborð eggjaskurnarinnar [56]. Við veltum því fyrir okkur að munur á framboði karbónat- og kalsíumjóna milli hópanna tveggja gæti hafa leitt til ójafnrar dreifingar litarefnis í útfellingarferlinu á yfirborði eggjaskurnarinnar, sem veldur eggjaskelflekkjum.

cistanche tubulosa-bæta ónæmiskerfið
Focal adhesions eru stórsameindabyggingar sem mynda vélrænar tengingar milli innanfrumu aktín umfrymis og utanfrumu fylkishluta [57]. Sýnt hefur verið fram á að brennivídd viðloðun gegnir mikilvægu hlutverki við að viðhalda formgerð og virkni eggjastokksins í kínverskum brúnum froskum [58], á meðan brennivídd viðloðun hefur einnig verið þátt í verkunarháttum eggjaframleiðslumunar hjá Jinghai Yellow kjúklingum og Nandan-Yao heimiliskjúklingar [59, 60]. Í núverandi rannsókn tóku brennidepill viðloðun þátt í myndun eggjaskelflekkja, en sértæka þátttökuaðferðin þarfnast enn frekari rannsóknar. MAPK-ferillinn hefur þrjá áberandi meðlimi: p38 mítógenvirkjaðan próteinkínasa (p38 MAPK), Jun N-terminal kínasa (JNK) og utanfrumuviðbragðskínasa (ERK), sem saman stjórna frumuvöxt, sérhæfingu, frumudauða, bólgu og annað. mikilvæg lífeðlisfræðileg viðbrögð [61]. Sýnt hefur verið fram á að ERK 1/2 MAPK ferillinn gegnir mikilvægu hlutverki í vexti, þroska og aðgreiningu eggjastokka og legs [62]. Wang o.fl. notaði vanadíum til að örva vöxt eggjastokka þekjufrumna og komst að því að MAPK fjölskyldumeðlimir voru virkjaðir, sem leiddi til oxunarálags á eggjastokknum, minni frumuvirkni og frumudauða [63]. Í núverandi rannsókn komumst við að því að MAPK merkjaferillinn í flekkótta hópnum var verulega auðgaður og þess vegna getgátum við að hænurnar sem verpa flekkóttum eggjum gætu hafa upplifað álag, með einhverjum áhrifum á eggjastokkinn. Taugavirkur bindill-viðtaka milliverkanir tengjast myndun sterahormóna í kynkirtlum. Þeir gegna mikilvægu hlutverki í stjórnun eggjaframleiðslu og starfsemi eggjastokka hjá alifuglum [59, 64]. Genið sem tjáð er mismunað, GABRA2, tilheyrir einnig taugavirka bindill-viðtaka víxlverkunarferlinu. Þar sem eggjaskelflögur birtast vegna eggjaframleiðslu og eggjaframleiðsla er taktfast ferli, leiðir mikil auðgun taugavirkra bindil-viðtaka víxlverkana í flekkótta hópnum til þess að við getum velt því fyrir okkur að það gæti verið munur á frammistöðu eggframleiðslu milli hæna sem verpa flekkóttum eggjum. og hænur sem verpa venjulegum eggjum, en þetta krefst frekari könnunar.
Umhverfisþættir geta haft áhrif á genatjáningu með epigenetic breytingum. Sambland af erfðafræðilegum og epigenetic breytingum gæti verið gagnlegt við að útskýra myndunarferli flókinna eiginleika [19, 65]. Sambandið milli DNA-metýleringar um allt erfðamengi og genatjáningar hefur verið rannsakað í mörg ár [66, 67]. Almennt bælir DNA metýlering genatjáningu [68]. Niðurstöður þessarar rannsóknar eru í samræmi við fyrri niðurstöður að því leyti að mikil genatjáning tengist lítilli DNA metýleringu á frumkvöðlasvæðinu [67, 68]. Hins vegar sást engin augljós þróun á genalíkamssvæðinu, sem gæti verið vegna þess að genatjáningarmynstur er einnig stjórnað af öðrum þáttum [69, 70]. Hagnýt auðgunargreining leiddi í ljós að DMG var aðallega auðgað á T-frumumiðluðu ónæmi, svörun við oxunarálagi og frumuviðbrögðum við DNA skemmda áreiti, og flestar leiðirnar eru tengdar öldrun [71-73]. Önnur öldrunartengd gen hafa einnig verið auðkennd, þar á meðal GCLC [74], CAV1 [75] og LYN [76]. Sambland af umritunar- og DNA-metýlerunargögnum sýndu að BFSP2 var eina genið sem skarast og var marktækt tjáð bæði við DNA-metýleringu og umritunarstig. BFSP2 var undirmetýlerað og tjáningarstig þess var lágt í flekkahópnum, sem bendir til þess að genatjáning sé stjórnað af öðrum umritunarþáttum auk metýleringarbreytinga. Ennfremur hefur BFSP2 verið skilgreint sem umsóknargen í meðfæddum drerum [77] og versnandi drersjúkdómi [78]. Þrátt fyrir að sýnt hafi verið fram á að BFSP2 tengist augnþroska hjá kjúklingum [79] eru rannsóknir á öðrum aðgerðum hjá kjúklingum takmarkaðar. Þess vegna eru frekari rannsóknir nauðsynlegar til að skýra hlutverk þess í myndun flekkóttra eggjaskurna.

cistanche ávinningur fyrir karla styrkir ónæmiskerfið
Ályktanir
Að lokum benda ónæmisvísitölur í sermi til þess að IgA innihald í flekkótta hópnum hafi verið umtalsvert lægra en í venjulegum hópi og við getum velt því fyrir okkur að minnkuð ónæmisvirkni sé nátengd myndun eggjaskelflekkja. Transcriptome greining greindist sjö DEG á milli flekkóttra og eðlilegra hópa, þar af IQSEC3, GABRA2 og BFSP2 voru auðkennd sem hugsanlega mikilvæg gen tengd myndun flekkóttra eggja. DNA metýleringargreining greindi DMG sem tengdust T-frumumiðluðu ónæmi, svörun við oxunarálagi og frumuviðbrögðum við DNA-skemmdaörvun. Af 282 DMG sem greind voru tengdust 15 öldrun. Samþætt greining á transcriptome og DNA metýleringu leiddi í ljós að eina genið sem skarast var BFSP2, sem hefur varla verið rannsakað hjá kjúklingum. Gögnin sem kynnt eru hér benda til þess að ónæmis- og öldrunarferlar varphæna geti stuðlað að myndun flekkóttra eggjaskurna, sem bætir skilning okkar á fyrirkomulagi myndunar eggjaskurnótta.
Heimildir
1. Bain MM, Nys Y, Dunn IC. Auka þrautseigju í varp og koma á stöðugleika í gæðum eggja í lengri varplotum. Hverjar eru áskoranirnar? Br Poult Sci. 2016;57(3):330–8.
2. Pottgüter R. Að fóðra varphænur til 100 vikna aldurs. Lohmann Inf. 2016;50:18–21.
3. Molnar A, Maertens L, Ampe B, Buyse J, Kempen I, Zoons J, Delezie E. Breytingar á eiginleikum eggjagæða á síðasta framleiðslustigi: er möguleiki á lengri varplotu? Br Poult Sci. 2016;57(6):842–7.
4. Gosler AG, Higham JP, James Reynolds S. Hvers vegna eru fuglaegg flekkótt? Ecol Lett. 2005;8(10):1105–13.
5. Arango J, Settar P, Arthur J, O'Sullivan N. Tengsl skeljalitar og tíðni flekkja í brúnum eggjalínum. Í: Proc XIIth European Poultry Conference: 2006. 2006. bls. 10–4.
6. Cheng X, Fan C, Ning Z. Gæði freknueggja og áhrifaþættir þess. Kínversk alifuglavísindi. 2019;41(19):6–9 (á kínversku).
7. Hincke MT, Nys Y, Gautron J, Mann K, Rodriguez-Navarro AB, McKee MD. Eggjaskurnin: uppbygging, samsetning og steinefnamyndun. Front Biosci (Landmark Ed). 2012;17(4):1266–80.
8. Samiullah S, Roberts JR, Chousalkar K. Eggskel litur í brúneggja varphænum - umsögn. Poult Sci. 2015;94(10):2566–75.
9. Wilson PW, Suther CS, Bain MM, Icken W, Jones A, Quinlan-Pluck F, Olori V, Gautron J, Dunn IC. Skilningur á myndun fuglaheggs í eggjastokkum: rannsókn á uppruna þess og útfellingu. Biol Reprod. 2017;97(1):39–49.
10 Zhu M, Li H, Miao L, Li L, Dong X, Zou X. Kadmíumklóríð í fæðu dregur úr lífrænni skeljar með því að trufla efnaskipti eggjaskurnsins hjá varphænum. J Anim Sci. 2020;98(2):skaa025.
11. Qi X, Tan D, Wu C, Tang C, Li T, Han X, Wang J, Liu C, Li R, Wang J. Rýrnun eggjaskurnagæða hjá varphænum sem eru tilraunasmitaðar af H9N2 fuglaflensuveiru. Dýralæknir Res. 2016;47:35.
12. Wang J, Yuan Z, Zhang K, Ding X, Bai S, Zeng Q, Peng H, Celi P. Epigallocatechin-3-gallatvarið vanadín-framkallað eggjaskel aflitun með P38MAPK-Nrf2/HO-1 merkjaleið hjá varphænum. Poult Sci. 2018;97(9):3109–18.
13. Avery OT, Macleod CM, McCarty M. Rannsóknir á efnafræðilegu eðli efnisins sem framkallar umbreytingu pneumókokkategunda: framkalla umbreytingu með desoxýríbónsýruhluta sem er einangrað úr pneumókokkategund Iii. J Exp Med. 1944;79(2):137–58.
14. Kochmanski J, Marchlewicz EH, Cavalcante RG, Sartor MA, Dolinoy DC. Aldurstengd DNA-metýlerun og hýdroxýmetýleringu í lengdarblóði músa. Epigenetics. 2018;13(7):779–92.
15. Zhang X, Hu M, Lyu X, Li C, Thannickal VJ, Sanders YY. DNA metýlering stjórnaði genatjáningu í líffæratrefjum. Biochim Biophys Acta Mol Basis Dis. 2017;1863(9):2389–97.
16. Ehrlich M. DNA ofmetýlering í sjúkdómum: aðferðir og klínískt mikilvægi. Epigenetics. 2019;14(12):1141–63.
17. Ling C, Ronn T. Epigenetics í offitu og sykursýki af tegund 2. Cell Metab. 2019;29(5):1028–44.
18. Kaminen-Ahola N, Ahola A, Maga M, Mallett KA, Fahey P, Cox TC, Whitelaw E, Chong S. Etanólneysla móður breytir frumgerð og svipgerð afkvæma í múslíkani. PLoS Genet. 2010;6(1):e1000811.
19 Tan X, Liu R, Xing S, Zhang Y, Li Q, Zheng M, Zhao G, Wen J. Uppgötvun á erfðamengi á lykilgenum og erfðafræðilegum merkjum fyrir fitulifur úr kjúklingi. Int J Mol Sci. 2020;21(5):1800.
20. Hwang JH, An SM, Kwon S, Park DH, Kim TW, Kang DG, Yu GE, Kim IS, Park HC, Ha J, o.fl. DNA metýleringarmynstur og genatjáning tengd gotstærð í Berkshire svínafylgju. PLoS EINN. 2017;12(9):e0184539.
21. Yu C, Qiu M, Zhang Z, Song X, Du H, Peng H, Li Q, Yang L, Xiong X, Xia B, o.fl. Umritunarraðgreining leiðir í ljós gen sem taka þátt í oxunarálagi af völdum kadmíums í kjúklingahjarta. Poult Sci. 2021;100(3):100932. 22. Boo SY, Tan SW, Alitheen NB, Ho CL, Omar AR, Yeap SK. Transcriptome greining á náttúrulegum drápsfrumum kjúklinga innan þekjuvefs sem eru sýktar af mjög illvígri smitandi bursal disease veiru. Sci Rep. 2020;10(1):18348.
23. Ren L, Liu A, Wang Q, Wang H, Dong D, Liu L. Transcriptome greining á þróun fósturvísa vöðva í Chengkou Mountain Chicken. BMC Genomics. 2021;22(1):431.
24. Yang C, Han L, Li P, Ding Y, Zhu Y, Huang Z, Dan X, Shi Y, Kang X. Einkenni og skeifugörn umritagreining á kínverskum nautgripum með ólíkum fóðurhagkvæmni með því að nota RNA-Seq. Framan Genet. 2021;12:741878.
25. Wang J, Jia R, Gong H, Celi P, Zhuo Y, Ding X, Bai S, Zeng Q, Yin H, Xu S, o.fl. Áhrif oxunarálags á eggjastokka kjúklinga: þátttaka örvera og melatóníns. Andoxunarefni (Basel). 2021;10(9):1422.
26. Attia YA, Al-Harthi MA, Abo El-Maaty HM. Magn kalsíums og kólkalsíferóls hjá varphænum á seintímum: Áhrif á framleiðslueiginleika, gæði eggja, lífefnafræði blóðs og ónæmissvörun. Front Vet Sci. 2020;7:389.
27. Moreno J, Osorno JL. Litur fuglaeggja og kynferðisval: endurspeglar litarefni eggjaskeljar kvenkyns ástand og erfðafræðileg gæði? Ecol Lett. 2003;6(9):803–6.
28. Afonso S, Vanore G, Batlle A. Protoporphyrin IX og oxunarálag. Free Radic Res. 1999;31(3):161–70.
29. Schwartz-Albiez R, Monteiro RC, Rodriguez M, Binder CJ, Shoenfeld Y. Náttúruleg mótefni, immúnóglóbúlín í bláæð og hlutverk þeirra í sjálfsofnæmi, krabbameini og bólgu. Clin Exp Immunol. 2009;158(Fylgibréf 1):43–50.
30. Martínez-de la Puente J, Merino S, Moreno J, Tomás G, Morales J, Lobato E, García-Fraile S, Martínez J. Eru eggjaskurn flekkóttur og litavísbendingar um heilsu og ástand í blábrjótum Cyanistes caeruleus? J Avian Biol. 2007;38(3):377–84.
31. Fagarasan S, Honjo T. IgA nýmyndun í þörmum: stjórnun á framlínu líkamsvörnum. Nat Rev Immunol. 2003;3(1):63–72.
32. Zhen W, Shao Y, Wu Y, Li L, Pham VH, Abbas W, Wan Z, Guo Y, Wang Z. Mataræði ger beta-glúkan viðbót bætir eggjaskurn lit og klakhæfni frjósömum eggjum auk þess að auka ónæmisvirkni hjá ræktanda varphænur. Int J Biol Macromol. 2020;159:607–21.
33. Elhamouly M, Nii T, Isobe N, Yoshimura Y. Aldurstengd mótun á meðfædda ónæmisvarnarkerfi í varphænum og legslímhúð. Poult Sci. 2019;98(7):3022–8.
34. Li J, Qin Q, Li YX, Leng XF, Wu YJ. Útsetning fyrir tri-ortho-cresyl fosfati leiðir til lítillar eggjaframleiðslu og lélegrar eggjaskurna með því að trufla þroska eggbús og starfsemi skeljakirtla hjá varphænum. Ecotoxicol Environ Saf. 2021;225:112771.
35. Fukaya M, Kamata A, Hara Y, Tamaki H, Katsumata O, Ito N, Takeda S, Hata Y, Suzuki T, Watanabe M, o.fl. SynArfGEF er gúanín núkleótíðskiptaþáttur fyrir Arf6 og staðsetur sig helst við sérhæfingar eftir taugamótun hamlandi taugamóta. J Neurochem. 2011;116(6):1122–37.
36. Um JW. Synaptic virkni IQSEC fjölskyldu ADP-ríbósýlerunarþáttar gúanín núkleótíðskiptaþátta. Neurosci Res. 2017;116:54–9.
37. Um JW, Choi G, Park D, Kim D, Jeon S, Kang H, Mori T, Papadopoulos T, Yoo T, Lee Y, o.fl. IQ Motif og SEC7 lén sem inniheldur prótein 3 (IQSEC3) hefur samskipti við Gephyrin til að stuðla að hamlandi synapse myndun. J Biol Chem. 2016;291(19):10119–30.
38. Kim S, Kim H, Park D, Kim J, Hong J, Kim JS, Jung H, Kim D, Cheong E, Ko J, o.fl. Tap á IQSEC3 truflar viðhald GABAergic synapse og dregur úr sómatóstatíntjáningu í Hippocampus. Cell Rep. 2020;30(6):1995-2005 e1995.
39. Erdö SL, Riesz M, Kárpáti E, Szporny L. GABAB viðtaka-miðluð örvun á samdráttarhæfni einangraðra eggjastokka kanína. Eur J Pharmacol. 1984;99(4):333–6. 40. Roth FC, Draguhn A. GABA umbrot og flutningur: áhrif á taugamótavirkni. Taugaplast. 2012;2012:805830.
41. Erdő SL, László Á, Szporny L, Zsolnai B. Hár þéttleiki sérstakra GABA bindistaði í eggjaleiðara manna. Neurosci Lett. 1983;42(2):155–60.
42. Erdo SL, Rosdy B, Szporny L. Hærri GABA styrkur í eggjaleiðara en í heila rottunnar. J Neurochem. 1982;38(4):1174–6.
43. Sun X, Chen X, Zhao J, Ma C, Yan C, Liswaniso S, Xu R, Qin N. Transcriptome samanburðargreining á eggbúum í eggjastokkum leiðir í ljós lykilgenin og merkjaleiðir sem tengjast framleiðslu hænsnaeggja. BMC Genomics. 2021;22(1):899.
44. Chen X, Sun X, Chimbaka IM, Qin N, Xu X, Liswaniso S, Xu R, Gonzalez JM. Umskriftargreining á eggbúum í eggjastokkum leiðir í ljós hugsanleg lykilgen sem tengjast aukinni og minni hraða framleiðslu kjúklingaeggja. Framan Genet. 2021;12:622751.
45. Luan X, Liu D, Cao Z, Luo L, Liu M, Gao M, Zhang X. Umritunarsnið auðkennir mismunandi tjáð gen í eggjastokkum Huoyan gæsa milli varptíma og stöðvunartímabils. PLoS EINN. 2014;9(11):e113211.
46. Cui Z, Zhang Z, Amevor FK, Du X, Li L, Tian Y, Kang X, Shu G, Zhu Q, Wang Y, o.fl. Circadian miR-449c-5p stjórnar Ca(2+) flutningi í legi meðan á kölkun eggjaskurn stendur hjá hænsnum. BMC Genomics. 2021;22(1):764.
47. Mishra SK, Chen B, Zhu Q, Xu Z, Ning C, Yin H, Wang Y, Zhao X, Fan X, Yang M, o.fl. Transcriptome greining leiðir í ljós mismunandi tjáð gen sem tengjast háum hraða eggjaframleiðslu í undirstúku kjúklinga heiladinguls-eggjastokka ás. Sci Rep. 2020;10(1):5976.
48. Cox PR, Siddique T, Zoghbi HY. Erfðafræðileg skipulagning Tropomodulins 2 og 4 og óvenjuleg innbyrðis og intraexonic splicing YL-1 og Tropomodulin 4. BMC Genomics. 2001;2:7.
49. Cox PR, Zoghbi HY. Raðgreining, tjáningargreining og kortlagning á þremur einstökum tropomodulin genum og músum þeirra. Erfðafræði. 2000;63(1):97–107.
50. Yamashiro S, Gokhin DS, Kimura S, Nowak RB, Fowler VM. Tropomodulins: prótein sem stýra aktínþráðum í ýmsum frumugerðum. Frumubeinagrind (Hoboken). 2012;69(6):337–70.
51. Almenar-Queralt A, Lee A, Conley CA, Ribas de Pouplana L, Fowler VM. Auðkenning nýs tropomodulin ísóforms, beinagrindar tropomodulin, sem lokar aktín þráðum oddhvassum endum í hröðum beinagrindarvöðvum. J Biol Chem. 1999;274(40):28466–75.
52. Ren T, Li Z, Zhou Y, Liu X, Han R, Wang Y, Yan F, Sun G, Li H, Kang X. Röð og lýsing á lncRNAs í brjóstvöðva Gushi og Arbor Acres hænsna. Erfðamengi. 2018;61(5):337–47.
53. Xu L, Zhao F, Ren H, Li L, Lu J, Liu J, Zhang S, Liu GE, Song J, Zhang L, o.fl. Samtjáningargreining á fósturþyngdartengdum genum í beinagrindsvöðvum sauðfjár á miðjum og síðbúnum þroskastigum fósturs. Int J Biol Sci. 2014;10(9):1039–50.
54. Wu Y, Wang Y, Yin D, Mahmood T, Yuan J. Transcriptome greining leiðir í ljós sameindaskilning á nikótínamíði og natríumbútýrat á kjötgæðum kjúklinga undir miklum þéttleika. BMC Genomics. 2020;21(1):412.
55. Zhang F, Yin ZT, Zhang JF, Zhu F, Hincke M, Yang N, Hou ZC. Að samþætta umrit, prótein og QTL gögn til að uppgötva virkni mikilvæg gen fyrir eggjaskurn og myndun albúms. Erfðafræði. 2020;112(5):3687–95.
56. Nys Y, Gautron J, Garcia-Ruiz JM, Hincke MT. Steinefnamyndun fuglaeggjaskeljar: lífefnafræðileg og hagnýt einkenni fylkapróteina. CR Palevol. 2004;3(6–7):549–62.
57. Chen CS, Alonso JL, Ostuni E, Whitesides GM, Ingber DE. Frumuform veitir alþjóðlega stjórn á fókusviðloðun samsetningu. Biochem Biophys Res Commun. 2003;307(2):355–61.
58 Su H, Zhang H, Wei X, Pan D, Jing L, Zhao D, Zhao Y, Qi B. Comparative Proteomic Analysis of Rana chensinensis Oviduct. Sameindir. 2018;23(6):1384.
59. Zhang T, Chen L, Han K, Zhang X, Zhang G, Dai G, Wang J, Xie K. Transcriptome greining á eggjastokkum í tiltölulega stærri og minni egg sem framleiða Jinghai Yellow Chicken. Anim Reprod Sci. 2019;208:106114.
60. Sun T, Xiao C, Deng J, Yang Z, Zou L, Du W, Li S, Huo X, Zeng L, Yang X. Transcriptome greining sýnir lykilgen og leiðir sem tengjast eggframleiðslu í Nandan-Yao innlendum kjúklingi. Comp Biochem Physiol Part D Genomics Proteomics. 2021;40:100889.
61. Peter AT, Dhanasekaran N. Apoptosis of granulosa cells: endurskoðun á hlutverki MAPK-merkjaeininga. Reprod Domest Anim. 2003;38(3):209–13.
62. Jeong W, Kim J, Ahn SE, Lee SI, Bazer FW, Han JY, Song G. AHCYL1 er miðlað af estrógen-völdum ERK1/2 MAPK frumuboðum og microRNA reglugerð til að hafa áhrif á starfræna þætti fuglaeggjastokksins. PLoS EINN. 2012;7(11):e49204.
63. Wang J, Huang X, Zhang K, Mao X, Ding X, Zeng Q, Bai S, Xuan Y, Peng H. Vanadate oxunar- og apoptotic áhrif eru miðlað af MAPK-Nrf2 ferlinum í lag eggjastokkum magnum þekjufrumum. Málmfræði. 2017;9(11):1562–75.
64. Tao Z, Song W, Zhu C, Xu W, Liu H, Zhang S, Huifang L. Samanburðargreining á háum og lágum egg-framleiðandi önd eggjastokkum. Poult Sci. 2017;96(12):4378–88.
65. Shioda K, Odajima J, Kobayashi M, Kobayashi M, Cordazzo B, Isselbacher KJ, Shioda T. Transcriptomic and Epigenetic Preservation of Genetic Sex Identity in Estrogen-feminized Male Chicken Embryonic Gonads. Innkirtlafræði. 2021;162(1):bqaa208.
66. Huang YZ, Sun JJ, Zhang LZ, Li CJ, Womack JE, Li ZJ, Lan XY, Lei CZ, Zhang CL, Zhao X, o.fl. Erfðamengi-breitt DNA metýleringarsnið og tengsl þeirra við mRNA og microRNA transcriptome í nautgripavöðvavef (Bos taurine). Sci Rep. 2014;4:6546.
67. Tan X, Liu R, Zhang Y, Wang X, Wang J, Wang H, Zhao G, Zheng M, Wen J. Samþætt greining á metýlómi og umskrift kjúklinga með blóðfitulifrarblæðingarheilkenni. BMC Genomics. 2021;22(1):8.
68. Fu Y, Li J, Tang Q, Zou C, Shen L, Jin L, Li C, Fang C, Liu R, Li M, o.fl. Samþætt greining á metýlómi, transcriptome og miRNAome þriggja svínakynja. Epigenomics. 2018;10(5):597–612.
69. Lawrence M, Daujat S, Schneider R. Hliðarhugsun: hvernig histónbreytingar stjórna genatjáningu. Trends Genet. 2016;32(1):42–56.
70. Zhao BS, Roundtree IA, He C. Eftir umritun genastjórnun með mRNA breytingum. Nat Rev Mol Cell Biol. 2017;18(1):31–42.
71. Chakravarti B, Abraham GN. Öldrun og T-frumumiðlað ónæmi. Mech Aging Dev. 1999;108(3):183–206.
72. Camougrand N, Rigoulet M. Öldrun og oxunarálag: rannsóknir á sumum genum sem taka þátt bæði í öldrun og til að bregðast við oxunarálagi. Respir Physiol. 2001;128(3):393–401.
73. Ribezzo F, Shiloh Y, Schumacher B. Systemic DNA skaða viðbrögð við öldrun og sjúkdóma. Semin Cancer Biol. 2016;37–38:26–35.
74. Orr WC, Radyuk SN, Prabhudesai L, Toroser D, Benes JJ, Luchak JM, Mockett RJ, Rebrin I, Hubbard JG, Sohal RS. Oftjáning á glútamat-cysteine lígasa lengir líftíma Drosophila melanogaster. J Biol Chem. 2005;280(45):37331–8.
75. Park DS, Cohen AW, Frank PG, Razani B, Lee H, Williams TM, Chandra M, Shirani J, De Souza AP, Tang B, o.fl. Caveolin-1 núll (-/-) mýs sýna verulega skerðingu á líftíma. Lífefnafræði. 2003;42(51):15124–31.
76. Park JW, Ji YI, Choi YH, Kang MY, Jung E, Cho SY, Cho HY, Kang BK, Joung YS, Kim DH, o.fl. Fjölbreytileiki gena umsækjenda fyrir sykursýki, hjarta- og æðasjúkdóma og krabbamein tengist langlífi hjá Kóreubúum. Exp Mol Med. 2009;41(11):772–81.
77. Jakobs PM, Hess JF, FitzGerald PG, Kramer P, Weleber RG, Litt M. Sjálfstætt ríkjandi meðfæddur drer í tengslum við brottfallsstökkbreytingu í geni BFSP2 með perluþráðaprótíni úr mönnum. Am J Hum Genet. 2000;66(4):1432–6.
78. Conley YP, Erturk D, Keverline A, Mah TS, Keravala A, Barnes LR, Bruchis A, Hess JF, FitzGerald PG, Weeks DE, et al. Unglinga, versnandi drer staðsetning á litningi 3q21-q22 tengist missense stökkbreytingu í perlulaga flament byggingarpróteininu-2. Am J Hum Genet. 2000;66(4):1426–31.
79. Kumar P, Kasiviswanathan D, Sundaresan L, Kathirvel P, Veeriah V, Dutta P. oxíð lagar frávik sem miðlað er af talidomíð með því að sveifla kerfinu aftur í eðlilegt umritamynstur. Biochimie. 2016;121:253–67.
80. Chen S, Zhou Y, Chen Y, Gu J. fastp: ofurfljótur allt-í-einn FASTQ forgjörvi. Lífupplýsingafræði. 2018;34(17):i884–90.
81. Kim D, Paggi JM, Park C, Bennett C, Salzberg SL. Línurit byggð erfðamengi röðun og arfgerð með HISAT2 og HISAT arfgerð. Nat Biotechnol. 2019;37(8):907–15.
82. Li H, Handsaker B, Wysoker A, Fennell T, Ruan J, Homer N, Marth G, Abecasis G, Durbin R, Genome Project Data Processing S. The Sequence Alignment/Map format og SAMtools. Lífupplýsingafræði. 2009;25(16):2078–9.
83. Liao Y, Smyth GK, Shi W. featureCounts: skilvirkt almennt forrit til að úthluta raðlestri á erfðafræðilega eiginleika. Lífupplýsingafræði. 2014;30(7):923–30.
84. Love MI, Huber W, Anders S. Miðlað mat á fold breytingu og dreifingu fyrir RNA-seq gögn með DESeq2. Erfðamengi Biol. 2014;15(12):550.
85. Subramanian A, Tamayo P, Mootha VK, Mukherjee S, Ebert BL, Gillette MA, Paulovich A, Pomeroy SL, Golub TR, Lander ES, o.fl. Auðgunargreining genasetts: þekkingarmiðuð nálgun til að túlka tjáningarsnið um erfðamengi. Proc Natl Acad Sci US A. 2005;102(43):15545–50.
86. Krueger F, Andrews SR. Bismark: sveigjanlegur aligner og metýleringarkall fyrir Bisulfte-Seq forrit. Lífupplýsingafræði. 2011;27(11):1571–2.
87. Jones PA. Aðgerðir DNA metýleringar: eyjar, upphafsstaðir, genalíkama og víðar. Nat Rev Genet. 2012;13(7):484–92.
88. Akalin A, Kormaksson M, Li S, Garrett-Bakelman FE, Figueroa ME, Melnick A, Mason CE. methylKit: alhliða R-pakki til greiningar á DNA-metýleringarferlum um allt erfðamengi. Erfðamengi Biol. 2012;13(10):R87.
89. Zhou Y, Zhou B, Pache L, Chang M, Khodabakhshi AH, Tanaseichuk O, Benner C, Chanda SK. Metascape veitir líffræðingsmiðaða úrræði til að greina gagnapakka á kerfisstigi. Nat Commun. 2019;10(1):1523.
