Hvernig dregur Cistanche fjölsykra úr sortumyndun og dregur úr oxunarálagi?
Mar 14, 2022
Fyrir frekari upplýsingar vinsamlega hafið samband við:Joanna.jia@wecistanche.com
Cistanche deserticola fjölsykra veldur sortumyndun í sortufrumum og dregur úr oxunarálagi
1Húðlækningadeild, þriðja Xiangya sjúkrahúsið, Central South University, Changsha, Kína
2Department of Urology, Third Xiangya Hospital, Central South University, Changsha, Kína
3Medicine Experimental Center, Third Xiangya Hospital, Central South University, Changsha, Kína

Cistanchedeserticolahefur mörg áhrif, smelltu hér til að vita meira
Ágrip: Sem meginhluti litarefnaraskana eru húðaflitunarsjúkdómar eins og skjaldkirtil og achromic naevus mjög algengir og fá meiri athygli núna. Meingerð depigmentation felur í sér truflun á starfsemi sortufrumna og tap, sem hugsanlega stafar af erfðum, sjálfsofnæmi og oxunarálagi. Meðal þeirra,oxunarálaggegnir lykilhlutverki; þó, fáar klínískar meðferðir geta tekist á við oxunarálag. Eins og greint var frá,Cistanchedeserticola fjölsykra(CDP) er áhrifaríkt andoxunarefni; byggt á því, metum við hlutverk þess í sortufrumum og afhjúpuðum aðferðirnar frekar. Í þessari rannsókn komumst við að því að CDP gæti stuðlað að sortumyndun í húðþekju sortufrumum (HEM) og sortuæxli í músum B16F10 frumum, það framkallaði einnig litarefni í sebrafiskum. Ennfremur gæti CDP virkjað mítógenvirkjaðan próteinkínasa (MAPK) merkjaferilinn, síðan uppstýrt tjáningu á umritunarþætti sem tengist míkróphthalmia (MITF) og niðurstreymis genum TYR, TRP1, TRP2 og RAB27A. Annars komumst við að því að CDP gæti dregið úr H2O2-framkölluðum frumueiturhrifum og frumudauða í sortufrumum. Frekari sannanir leiddu í ljós að CDP gæti aukið NRF2/HO-1 andoxunarferil og hreinsað innanfrumu ROS. Í stuttu máli, CDP getur stuðlað að sortumyndun og komið í veg fyrir að sortufrumur verði fyrir oxunarálagsmeiðslum, sem bendir til þess að CDP hjálpi til við að viðhalda eðlilegu ástandi sortufrumna. Þannig getur CDP verið nýtt lyf til að meðhöndla aflitunarsjúkdóma.
LYKILORÐ:
Cistanche deserticola fjölsykra, aflitunarsjúkdómur, sortufrumur, sortumyndun, NRF2,oxunarálag
1. INNGANGUR
Húðaflitunarsjúkdómar, eins og vitiligo og achromic naevus, einkennast af flekkóttum eða umfangsmiklum litabreytingum í húð.1 Þó húðskemmdir valdi sjaldan alvarlegum líkamlegum meiðslum, hafa þeir áhrif á útlit sjúklings og skapa alvarlega sálfræðilega byrði, jafnvel geðheilsukvillar.2 Helstu meinafræðilegar breytingar á litarefnabreytingum fela í sér truflun á starfsemi sortufrumna og tap, sem hefur mikil áhrif á myndun og flutning melaníns,3 sem leiðir þannig til ófullnægjandi uppsöfnunar melaníns í húðinni.
Aðferðirnar sem taka þátt í aflitun eru óþekktar eins og er, en rannsóknir hafa bent á nokkra tengda þætti. Annars vegar er virkni sortufrumna að hluta til háð microphthalmia-associated transcription factor (MITF), sem er vel þekktur fyrir að stuðla að tjáningu á sortufrumnatengdum genum, þar á meðal tyrosinasa (TYR), tyrosinasa-tengt prótein 1 (TRP1), tyrosinasa-tengt. prótein 2 (TRP2), ras-tengt prótein Rab-27a (RAB27A) og fascin actin-bundling protein 1 (FSCN1).4 Meðal þessara gena gegnir TYR lykilhlutverki í melanínmyndun með því að oxa l-dopa í dópakínón.5 Á hinn bóginn benda rannsóknir til samsetningar nokkurra þátta sem gætu verið ábyrgir fyrir tapi sortufrumna, þar á meðal erfðir, umhverfi, sjálfsofnæmi og oxunarálag.6-9 Meðal þessara þátta er oxunarálag talin mikilvægasti .
Aðgerðirnar áoxunarálagsem veldur litabreytingum hefur að hluta komið í ljós; ofhleðsla viðbragðs súrefnistegunda (ROS) er einn lykilþáttur.10 ROS ofhleðsla í aflitun felur í sér ójafnvægi á milli for- og andoxunarefnakerfa.11 Einn af þáttunum sem taka þátt í þessu ójafnvægi er kjarnaþáttur rauðkorna 2-tengt þáttur 2/andoxunarefnissvörunarþáttur (NRF2/ARE) skerðing á andoxunarferil.12 Ferlið samanstendur af NRF2 og andoxunarensímum eins og heme súrefnisasa-1 (HMOX-1, HO-1) , katalasa (CAT), glútaþíon peroxidasi 1 (GPX1) og NAD(P)H kínón dehýdrógenasa 1 (NQO1).13 Þegar sortufrumur verða fyrir óhóflegu ROS getur NRF2 færst yfir í kjarnann og tengst hinum varðveittu ARE, síðan stuðlað að tjáningu andoxunarensíma. Hins vegar, í sumum aflitunarsjúkdómum, eins og vitiligo, getur skert NRF2/ARE andoxunarferill ekki hreinsað ROS á áhrifaríkan hátt.14 Klínískar meðferðir sem almennt eru notaðar við aflitun fela í sér staðbundna eða almenna barkstera, calcineurin hemla, þröngband útfjólublátt B (NBUVB; 3111) , 308-nm excimer ljós, eigin húðþekjuígræðsla og meðferð með hefðbundinni kínverskri læknisfræði (TCM). Barksterar og calcineurin hemlar geta dregið úr óeðlilegri ónæmisvirkjun,15 á meðan ljósameðferð er notuð sem fyrsta meðferðarúrræði; einkum, NBUVB örvar fjölgun sortufrumna og eyðingu T-frumna,16 á meðan 308-nm excimer ljós veldur frumudauða T-frumna.17 Að auki tengjast áhrif TCM meðferða við að stuðla að sortumyndun.18 Að vissu marki eru þessar aðferðir eru gagnlegar til að bæta aflitamyndun, en það er enn krefjandi að stjórna framgangi sjúkdómsins. Nauðsynlegt er að þróa nýjar meðferðir, sérstaklega við oxunarálagi, sem áður var vanrækt.
Cistanche deserticolaer þekkt sem „eyðimerkurginseng“.19 Íhlutir þess eru gagnlegir við lifrarskaða af völdum etanóls og ofvöxt í þörmum; það er einnig hægt að nota sem hvarfefni gegn þreytu, bólgueyðandi og æxli.20-22 Nýlega greindu Guo o.fl.Cistanche deserticola fjölsykra(CDP), einn af aðalþáttum þess, hafði andoxunarefni og lifrarverndandi virkni20; aðrar tvær rannsóknir auðkenndu hlutverk þess við að vernda frumur gegn meiðslum í súrefnis-glúkósasviptingu/endurflæði og beinþynningu.23,24 Hins vegar hefur hlutverk CDP í aflitunarsjúkdómum ekki verið skýrt. Hér var stefnt að því að staðfesta hvort CDP coxunarálaggæti haft áhrif á sortumyndun og vernda sortufrumur gegn oxunarálagi.

2.|EFNI OG AÐFERÐIR
2.1|Efni og mótefni
Cistanche deserticolafjölsykra(CDP) og l-dopa voru keypt frá Yuanye Biotec (hreinleiki meiri en eða jafnt og 98 prósent; Shanghai, Kína). Vetnisperoxíð (H2O2), dímetýlsúlfoxíð (DMSO), NaOH, Triton X-100, 4,5-dímetýlþíasól-2-ýl-2,5-dífenýltetrasólíumbrómíð ( MTT), og Annexin V-FITC Apoptosis Detection Kit voru keyptir frá Sigma-Aldrich. 4 prósent hlutlaust paraformaldehýð var keypt frá Biosharp (Hefei, Kína); og ónæmisflúrljómunarlitunarsett (Alexa Fluor 488) og 2,7-díklórflúorljómandi-díasetat (DCFH-DA) var keypt frá Beyotime Biotec (Shanghai, Kína). Fontana-Masson blettasett og kjarnflóðpróteinútdráttarsett voru keypt frá Sloarbio (Beijing, Kína). Vaxtaruppbót fyrir sortufrumur manna (HMGS), Dulbecco's modified Eagle medium (DMEM) og miðill 254 voru keyptir frá Gibco. Fósturnautasermi (FBS) var keypt frá BI (Kibbutz Beit-Haemek, Ísrael). Aðalmótefni fyrir -aktín, TYR, TRP2, RAB27A, FSCN1, ERK, p-ERK, JNK, p-JNK,
p38, p-p38, NRF2 og HO-1 voru keyptir frá Cell Signaling Technology, aðal mótefni fyrir MITF var keypt frá St John's Laboratory, aðal mótefni fyrir p-MITF var keypt frá Affinity Biosciences, aðal mótefni fyrir GAPDH var keypt frá Bioworld og aðal mótefni fyrir TRP1 var keypt frá EMD Millipore.
2.2| Frumuræktun og meðferð
Mús sortuæxli B16F10 frumur voru ræktaðar í miðlungs DMEM bætt við 10 prósent FBS og 1 prósent penicillín-streptomycin sýklalyfjablöndu. Melanocytes frá mönnum (HEM) voru aðskilin frá forhúð manna (sjá fyrri rannsókn okkar25) og ræktuð í miðli 254 ásamt HMGS, 5 prósent FBS og 1 prósent penicillín-streptomycin sýklalyfjablöndu. Allar frumur voru ræktaðar í blautum hitakassa við 37 gráður með 5 prósent CO2. CDP var leyst upp í DMSO og þynnt
með miðli fyrir notkun var lokastyrkur DMSO lægri en 0,1 prósent . H2O2 var þynnt með miðlinum fyrir notkun.
2.3|Ræktun og meðferð sebrafiska
Sebrafiskafósturvísarnir og miðillinn voru keyptir frá EzeRinka Biotech. Tilraunaskráin var samþykkt af siðanefnd Mið-Suður háskólans. Sebrafiskarnir voru ræktaðir í 12-brunnsplötum í 37 gráðu fjarlægð frá ljósi og meðhöndlaðir með mismunandi styrk af CDP. Snúið smásjá var notuð til að fylgjast með og skrá melanín í hausum og hala sebrafiska daglega. Eftir athugun breyttum við miðlinum og bættum CDP við aftur. Melanínþéttleiki í sporum sebrafiska var mældur með mynd J og gildin eru sýnd sem samþætt ljósþéttleiki (IOD).
2.4| Lífvænleiki frumna
Lífvænleiki frumna var mældur með MTT prófi. Til að kanna frumueiturhrif CDP voru HEM og B16F10 frumur græddar í 96-brunnsplötur með þéttleika 2 × 1{{30}}3 frumur/brunn og ræktaðar þar til frumurnar voru festar við plötur. Frumurnar voru síðan meðhöndlaðar með mismunandi styrk (0, 2,5, 5, 10, 20, 40, 80, 160 og 320 ug/mL) af CDP í 24, 48 eða 72 klst. Fyrir mælingu var 20 μL af MTT bætt í hvern brunn og plöturnar ræktaðar við 37 gráður í 4 klst. Eftir það fleygðum við flotinu og bættum 160 μL af DMSO í hvern brunn til að leysa upp formazan kristallana. Gleypigildið við 490 nm var mælt með multimode plötulesara (PerkinElmer). Til að kanna áhrif CDP á H2O2- framkallað frumueiturhrifaástand, voru HEMs og B16F10 frumur settar í 96-brunnsplötur með þéttleikanum 4 × 103 frumur/brunn. Frumurnar voru meðhöndlaðar með mismunandi styrk af CDP (0, 20, 40 eða 80 ug/ml) í 24 klukkustundir, á þeim tímapunkti bættum við H2O2 (endanlegur styrkur: 500 μm fyrir HEMs og 1,0 mm fyrir B16F10 frumur) í hvern brunn. og ræktaði frumurnar í 24 klukkustundir í viðbót. Við settum upp CDP-meðhöndlaða og neikvæða samanburðarhópa (NC). Uppgötvunarskrefin voru þau sömu og áður hefur verið lýst.
2,5|NaOH próf á melaníninnihaldi
Frumurnar voru ræktaðar í {{0}} mm petrískálum og meðhöndlaðar með CDP í mismunandi styrkleika (0, 20, 40 og 80 ug/mL) í 48 klukkustundir, síðan meltaðar með trypsíni og safnað í 1. 5-mL slöngur. Við þvoðum frumurnar tvisvar með tvíeimuðu vatni, blönduðum þær aftur í 1 ml af etanóli og hvöttum þær til að losa melanínið. Við skilgreindum síðan (200 g, 5 mínútur) blönduna og fleygðum flotinu, bættum 1 ml af 10 prósenta DMSO (þynnt með 1 mm NaOH lausn) í hvert túpa og setinu var dreift. Við ræktuðum sviflausnina í vatnsbaði við 80 gráður í 1 klukkustund til að leysa upp melanínið. Að lokum fluttum við 200 μL af vökvanum yfir á 96-brunnsplötu og notuðum multimode plötulesara til að mæla gleypnigildið við 470 nm.
2.6|Tyrosinasa virkni mælingar
Frumurnar voru ræktaðar í {{0}}mm petrískálum og meðhöndlaðar með CDP fyrir mælingu, meltaðar með trypsíni og safnað í 1.5-ml glös og þvegnar tvisvar með fosfat-bufferuðu saltvatni (PBS) ). Við fluttum 106 frumur úr hverju sýni yfir í nýtt glös og fleygðum flotinu eftir skilvindu, bættum síðan 1 ml 0,5 prósent Triton X-100 við frumukúluna og geymdum blanda við 0 gráðu í 15 mínútur. Síðan bættum við 1 ml af l-dopa (1 mm, þynnt með 0.1 M fosfatbuffi) við sem hvarfefni og blanduðum lausnina, færðum 200 μL af blöndunni í 96-brunnsplötu strax, og mældi gleypnigildið (A0) við 475 nm með því að nota multimode plötulesara, og endurtaktu mælinguna eftir 10 mínútur (A10). Týrósínasavirknin var reiknuð út með (A10-A0)/105 og niðurstöðurnar eru gefnar upp sem hundraðshluti (prósent) á móti neikvæðri samanburði.
2.7| Fontana-Masson melanín litun
Frumurnar voru ræktaðar í 12-brunnsplötum þar til þær náðu 50 prósenta þéttleika. Eftir meðferð voru frumurnar festar með 4 prósent hlutlausu paraformaldehýði í 30 mínútur og skolaðar með eimuðu vatni. Við bættum svo 500 μL Fontana ammoníak-silfurlausn í hvern brunn og geymdum plöturnar í myrkri í 16 klukkustundir til að lita melanínið. Næst þvoðum við frumurnar með eimuðu vatni fimm sinnum (1 mínúta í hvert skipti) og lögðum þær í bleyti í 500 μL hyposulphite í 5 mínútur; að lokum fjarlægðum við hyposúlfítið og skoluðum frumurnar aftur með eimuðu vatni í 1 mínútu. Við notuðum síðan öfuga smásjá til að skoða og skrá melanínin.
2.8|RNA útdráttur og megindleg öfug umritun-pólýmerasa keðjuverkun
Frumurnar voru ræktaðar í 6-brunnsplötum. Eftir meðferð voru frumurnar meltar með trypsíni og þeim safnað í 1.5-ml glös. Við þvoðum frumurnar tvisvar með PBS, bættum síðan við 1 ml af lýsisjafnalausn, hringdum blöndunni og settum glösin á ís í 5 mínútur til að lýsa frumurnar alveg. RNA var dregið út með því að nota Total RNA Kit (Omega Bio-Tek) og öfugt umritað (RT) með ReverTra Ace qPCR RT Master Mix (TOYOBO). Megindleg öfug umritun-pólýmerasa keðjuverkun (PCR) var framkvæmd með því að nota KODSYBR qPCR Mix (TOYOBO). Hvarfrúmmál RT blöndunnar var 20 μL, en hvarfmagn PCR blöndunnar var 20 μL (cDNA 1-8 μL, MIX 10 μL, grunnur F 1 μL, grunnur R 1 μL, bætið DEPC H2O við 20 μL ). Tilraunirnar voru gerðar samkvæmt samskiptareglum. Röð frumanna eru skráð í töflu S1.
2.9|Próteinútdráttur og Western blotting/ónæmisflúrljómun
Frumurnar voru ræktaðar í 100-mm petriskálum. Eftir meðferð voru frumurnar meltar með trypsíni og þeim safnað í 1.5-ml glös. Við þvoðum frumurnar tvisvar með PBS, síðan bættum við út í 500 μL af RIPA lýsisbuffi (Thermo Fisher) ásamt 1 mm fenýlmetýlsúlfónýlflúoríði (Thermo Fisher) og 1:100 þynntum fosfatasahemlum (Roche). Kjarna- og umfrymispróteinið var dregið út með því að nota Nucleoplasmic Protein Extraction Kit í samræmi við siðareglur framleiðanda. Við settum rörin á ís í 30 mínútur og hvirluðum þau á 5 mínútna fresti til að ljósa frumurnar alveg. Við skilgreindum frumunum (200 g, 4 gráður, 15 mínútur), færðum ofanvatnið í nýtt rör og mældum styrk heildarpróteinsins með BCA próteingreiningarsetti (KeyGEN Biotec). Við soðum próteinin með 5x hleðslubuffi (Beyotime Biotec, Kína) við 100 gráður í 10 mínútur, geymdum þau síðan við -80 gráður. Pólýakrýlamíð gel rafdráttaraðferð (PAGE) var notuð í Western blotting og 20 ug af próteini úr hverjum hópi voru aðskilin og flutt yfir á pólývínýlíden flúoríð himnu. Eftir mótefnavakablokkun ræktuðum við himnuna í 1:1000 þynntu aðalmótefni í 16 klukkustundir við 4 gráður, þvoðum síðan himnuna með PBST og ræktuðum hana í 1:10 000 þynntu flúrljómandi aukamótefni í 1 klukkustund við 37 gráður . Flúrljómunarstyrkurinn var greindur með því að nota Odyssey CLx Imaging System (LI-COR). Ónæmisflúrljómun var framkvæmd með því að nota Immunofluorescence Staining Kit (Alexa Fluor
488) með 1:100 þynningu af aðal mótefninu.
2.10|Mæling á frumudapósu
Frumurnar voru ræktaðar í {{0}}mm petrískálum og meðhöndlaðar með mismunandi styrk (0, 20, 40 og 80 ug/mL) af CDP í 24 klukkustundir og H2O2 var bætt við ( endanlegur styrkur: 500 μm fyrir HEM, 1,0 mm fyrir B16F10 frumur) í hvern brunn og ræktaður í 24 klukkustundir í viðbót. Við setjum einnig upp CDP-meðhöndlaða og NC hópa. Eftir meðhöndlun meltum við frumurnar með EDTA-fríu trypsíni og söfnuðum þeim í rör, þvoðum síðan frumurnar tvisvar með PBS og blönduðum þær aftur í 100 μL af PBS. Frumurnar voru litaðar með Annexin V-FITC Apoptosis Detection Kit í samræmi við siðareglur og greindar með frumuflæðismælingu (FCM). FlowJo hugbúnaður var notaður til að greina apoptosis hraða.
2.11| Innanfrumu ROS mæling
Frumurnar voru ræktaðar í {{0}}brunnsplötum og meðhöndlaðar með mismunandi styrk (0, 20, 40 og 80 ug/mL) af CDP í 24 klukkustundir, sem við bættum H2O2 við (endastyrkur: 500 μm fyrir HEM,
1.0 mm fyrir B16F10 frumur) í hvern brunn, ræktaði þær í aðra
24 tíma og setja upp CDP-meðhöndlaða og NC hópa. Eftir meðferð þvoðum við frumur tvisvar með PBS til að fjarlægja allan miðilinn og FBS, þynntum síðan DCFH-DA rannsakann í 1:1000 með miðli og bættum honum við hverja brunn. Við ræktuðum frumurnar við 37 gráður í 30 mínútur og þvoðum þær þrisvar sinnum með sermilausum miðli. Við notuðum an
öfug flúrljómunarsmásjá til að fylgjast með og skrá flúrljómunina, notaði síðan ImageJ til að mæla flúrljómunarstyrkinn.
2.12|Tölfræði og greining
Gögnin í þessari vinnu eru sett fram sem meðaltal ± staðalfrávik (SD), og tölfræðileg greining var framkvæmd með því að nota GraphPad Prism (útgáfa 7.0) eða SPSS (útgáfa 22.0), og nemenda t-próf eða einhliða dreifnigreining (ANOVA) var notuð fyrir samanburð á mörgum hópum. Grágildi WB próteinbandanna var staðlað með GAPDH eða -aktíni. Gildi P < .05="" voru="" talin="" marktæk.="" allar="" tilraunir="" voru="" endurteknar="" að="" minnsta="" kosti="" þrisvar="">

3|NIÐURSTÖÐUR
3.1|CDP framkallaði sortumyndun í HEM og B16F10 frumum
Áður en við byrjuðum notuðum við MTT prófið til að kanna hugsanleg frumudrepandi áhrif CDP á HEM og sortuæxli í músum B16F10 frumum. Frumurnar voru meðhöndlaðar með CDP í mismunandi styrk í 24, 48 eða 72 klst. HEM lífvænleikapróf sýndu að þegar styrkurinn var lægri en 320 ug/mL, hafði CDP engin áhrif á lífvænleika frumna; hins vegar minnkaði lífvænleikinn marktækt þar sem styrkurinn náði 320 ug/ml eftir 24, 48 og 72 klukkustundir (P < 0,05;="" mynd="" 1a).="" lífvænleiki="" b16f10="" frumna="" minnkaði="" einnig="" eftir="" 48="" og="" 72="" klst.="" þegar="" cdp="" náði="" 320="" ug/ml="" (p="">< 0,01)="" en="" engin="" breyting="" sást="" við="" lægri="" styrk="" (mynd="" 1b).="" við="" könnuðum="" síðan="" fyrst="" hlutverk="" cdp="" í="" sortumyndun="" og="" bárum="" saman="" áhrif="" þess="" við="" áhrif="" -melanocyte-örvandi="" hormóns="" (-msh;="" styrkur:="" 20,="" 100="" og="" 400="" nm)="" og="" dmso="" (0,1="" prósent)="" í="" hems.="" niðurstöður="" melanínlitunar,="" týrósínasavirkni="" og="" melaníninnihaldsmælinga="" bentu="" til="" þess="" að="" cdp="" væri="" sambærilegt="" við="" -msh="" til="" að="" stuðla="" að="" sortumyndun,="" á="" meðan="" 0,1="" prósent="" dmso="" meðferð="" skipti="" engu="" (mynd="">
Við betrumbætum könnun okkar enn frekar í samræmi við það. HEM voru meðhöndluð með CDP í mismunandi styrkleika (20, 40 og 80 ug/mL) í 48 klukkustundir; Melanín litun, melanín innihald og týrósínasa virkni mælingar voru gerðar og allar sýndu marktæka aukningu eftir CDP meðferð á styrkleikaháðan hátt sem náði hámarki í 80 ug/mL hópnum (P < 0,05,="" mynd="" 2a-c)="" .="" við="" mældum="" síðan="" mrna="" og="" próteinmagn="" gena="" sem="" tengjast="" sortumyndun="" (mitf,="" tyr,="" trp1,="" trp2,="" rab27a="" og="" fscn1).="" cdp="" jók="" marktækt="" mrna="" gildi="" þessara="" gena="" í="" hems="" (p="">< 0,05;="" mynd="" s2a).="" að="" auki="" jókst="" magn="" mitf,="" tyr,="" trp1="" og="" rab27a="" próteina,="" sem="" og="" hlutfall="" fosfórýleraðs="" mitf="" og="" heildar="" mitf="" (p=""><.05), en="" trp2="" og="" fscn1="" sýndu="" engan="" mun="" (mynd="" 2d,="" e).="" niðurstöðurnar="" gáfu="" til="" kynna="" að="" cdp="" geti="" stuðlað="" að="" sortufrumum="" og="" aukið="" tjáningu="" gena="" sem="" tengjast="" sortufrumum="" í="" sortufrumum="">
Ennfremur staðfestum við áhrif CDP aftur með B16F10 frumum og komumst að því að melaníninnihald B16F10 frumna jókst verulega (P <.01; mynd="" s2b).="" að="" auki,="" cdp="">
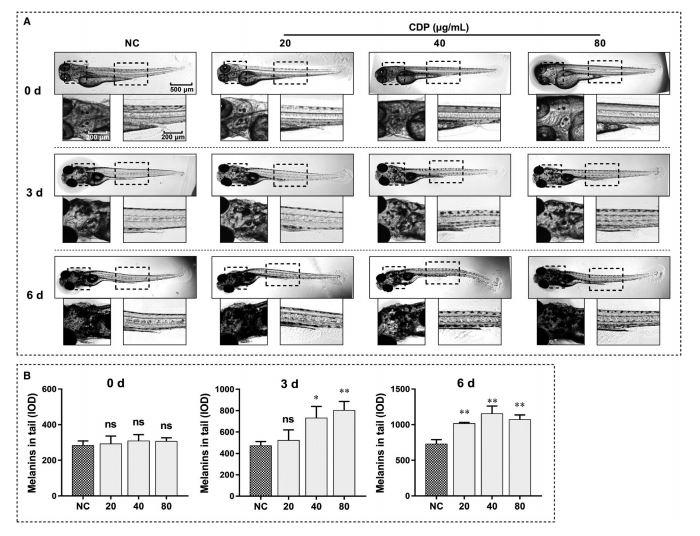
3.2|CDP stuðlaði að sortumyndun í sebrafiskum
Til að kanna hvort CDP gæti stuðlað aðsortumyndunin vivo notuðum við sebrafiskafósturvísa. Sebrafiskafósturvísunum var skipt í fjóra hópa og stöðugt meðhöndlaðir með miðli einu sér (NC) eða CDP í mismunandi styrkleika (20, 40 og 80 ug/mL); þéttleiki og dreifing melanínkorna var fylgst með og skráð á hverjum degi. Þegar sebrafiskafósturvísarnir stækkuðu komumst við að því að melanínþéttleiki jókst smám saman í hausum og hala. Á 3. degi var greinanleg millihópamunur og munurinn hélt áfram að aukast þar til við lauk tilrauninni á 6. degi (Mynd 3A). Við notuðum mynd J til að mæla melanínþéttleika í hala sebrafiska; melanínþéttleiki í CDP-meðhöndluðu hópunum var marktækt hærri en í samanburðarhópnum (P < 0,05;="" mynd="">
3.3|CDP virkjaður MAPK merkjaferill í HEM og B16F10 frumum
Til að sýna hvernig CDP kynntisortumyndun, meðhöndluðum við HEMs með CDP í mismunandi styrk (20, 40 og
80 ug/mL) í 48 klukkustundir og rannsakað síðan fosfórýlerað og heildarmagn ERK, JNK og p38 próteina í MAPK boðleiðinni. Eins og mælt var með Western blotting, hækkuðu p-ERK, p-JNK og p-p38 gildi eftir CDP meðferð (P < 0,05),="" á="" meðan="" heildarmagn="" þeirra="" breyttist="" ekki="" (mynd="" 4a,="" b).="" tilraunirnar="" voru="" endurteknar="" með="" b16f10="" frumum="" og="" fosfórýlerað="" magn="" erk,="" jnk="" og="" p38="" próteina="" var="" aukið="" (p="">< 0,05),="" en="" heildarmagn="" mapk="" breyttist="" ekki="" (mynd="" 4c,="" d),="" í="" samræmi="" við="" niðurstöður="" í="" hems="">
3.4|CDP veiklað H2O2-framkallað
frumueiturhrif og frumudauði í HEM og B16F10 frumum
Við notuðum H2O2 til að líkja eftiroxunarálagumhverfi og kannaði frekar hlutverk CDP í sortufrumum undiroxunarálag. Lokastyrkur H2O2 sem notaður var í HEM var 500 μm, en í B16F10 frumum var 1,0 mm. Til að kanna áhrif CDP á H2O2-framkallað frumueiturhrif, formeðhöndluðum við HEM og B16F10 frumur með CDP í mismunandi styrk (20, 40 og 80 ug/mL) í 24 klukkustundir, bættum síðan H2O2 við og héldum áfram að meðhöndla þær í 24 klukkustundir áður en athugun og MTT próf er framkvæmt.
H2O2 olli augljósri himnublæðingu og frumusamdrætti í HEMs, í CDP-formeðhöndluðu hópunum var ástandið létt. Meðferð með CDP einu sér hafði engin áhrif (Mynd 5A). MTT prófið sýndi svipaða niðurstöðu að því leyti að H2O2 meðferð minnkaði lífvænleika HEM, en CDP bætti verulega úr þessum skaðlegu áhrifum


3,5|CDP hreinsað H2O2-örvaði innanfrumu ROS í HEM og B16F10 frumum
Til að rannsaka aðferðir CDP til að minnka H2O2-framkallað frumueiturhrif og frumudauða, fundum við frekar innanfrumu ROS í HEMs og B16F10 frumum með DCFH-DA flúrljómun

4|UMRÆÐA OG NIÐURSTÖÐUR
Í þessari rannsókn könnuðum við hlutverk CDP í HEM og B16F10 frumum. Í fyrsta skipti fundum við að CDP gæti kynntsortumynduní sortufrumum og stuðla að litarefni í sebrafiskum. Síðari tilraun sýndi að MAPK boðleiðin var virkjuð við CDP meðferð. Við könnuðum frekar hlutverk þess íoxunarálagog komst að því að CDP gæti dregið úr H2O2- af völdum frumueiturhrifa og frumudauða í sortufrumum; á meðan gæti CDP virkjað NRF2/HO-1 andoxunarferilinn og hreinsað innanfrumu ROS undiroxunarálagskilyrði.
Mítógenvirkjaður próteinkínasi er mikilvæg leið sem tekur þátt í stjórnun MITF, lykilumritunarþáttar sem stuðlar að tjáningu ásortumyndun-tengd gen og hefur í kjölfarið áhrif á myndun og flutning melaníns.26,27 Í rannsókn okkar jókst virkjun ERK, JNK og p38 í sortufrumum marktækt eftir CDP meðferð; á meðan, tjáning MITF/p-MITF og MITF-drifið TYR, TRP1, TRP2 og RAB27A
voru settar upp í samræmi við það. Þannig leggjum við til að CDP geti
stuðla aðsortumyndunmeð því að virkja MAPK ferlið, en hvernig CDP virkjar MAPK er enn óþekkt. Samkvæmt nýlegum rannsóknum er toll-like receptor 4 (TLR4) mjög tjáður í sortufrumum og tekur þátt í sortumyndun.28,29 TLR4 er mikilvægt yfirhimnuprótein sem getur sérstaklega bundið lípópólýsykru (LPS)30; rannsóknir greindu frá því að LPS getur framkallað sortumyndun.29 Athyglisvert er að nokkrirfjölsykrurunnin úr plöntum eða sveppum sem sagt er að virkjað TLR og niðurstreymis boðleiðir eins og MAPK og kjarnaþátt kappa beta (NF-κB).31,32 Þess vegna grunar okkur að CDP geti verið þekkt og bundið af TLR, virkjar síðan niðurstreymis MAPK merki- lengja leið og stuðlar aðsortumyndun. Ennfremur er vitað að núkleótíðbindandi fáliðunarsvæðislíkir viðtakar (NLR) þekkja innanfrumu bindla og knýja fram virkjun MAPK og NF-KB boðleiða.33,34 Eins og greint hefur verið frá geta fjölsykrur sem eru dregin úr Ganoderma lucidum og Astragalus farið inn í frumur og hafa áhrif á NLR.35,36 Þannig er mögulegt að CDP geti farið inn í sortufrumur og stjórnað MAPK-boðaleiðinni í gegnum NLR. Hins vegar er þörf á frekari rannsóknum til að sannreyna þessa tilgátu.
Sumar rannsóknir hingað til greindu frá notkun náttúrulyfjafjölsykrurí sortumyndun til að hamla melanínframleiðslu.37,38 Hins vegar, í þessari rannsókn, stuðlaði CDP að sortumyndun í

sortufrumur, og þessi áhrif voru enn staðfest eftir samanburð við -MSH. CDP er líka eins konarfjölsykraunnin úr jurtum, grunar okkur að öfug áhrif CDP geti tengst byggingarmun á CDP og öðrumfjölsykrur. Fjölsykrur myndast við fjölliðun á einsykrum en eru breytilegar í einsykru gerð, einsykrum samsetningu, glýkósíðtengi, hliðarkeðju uppbyggingu og mólmassa39,40; þessir þættir eru taldir ákvarða líffræðilega virkni þeirra.41 Núverandi rannsóknir hafa lagt til uppbyggingu CDP og bent til þess að CDP uppbygging hafi í kjölfarið áhrif á virkni þess.42 Því þarf fleiri sannanir til að skilja CDP að fullu og staðfesta tilgátu okkar.
Melanogenese er mikilvægur verndarbúnaður til að standast
útfjólubláar skemmdir og viðhalda jafnvægi líkamans43; á sama
tíma, verða sortufrumur auðveldlega fyrir óhagstæðu umhverfi eins og ROS ofhleðslu.11 Það er vitað að ROS taka þátt í að eflasortumyndun, einn af aðferðunum er að virkja MAPK.44 En rannsóknir leiddu einnig í ljós að þessi áhrif eru aðeins til staðar innan ákveðins ROS-stigs, á meðan ROS-ofhleðsla skerðir sortumyndun verulega.45 Sambandið milli ROS, MAPK og sortumyndunar er breytilegt við mismunandi aðstæður, þannig, jafnvægið á milli for- og andoxunarkerfa er augljóslega mikilvægt. Í aflitunarsjúkdómum eins og vitiligo, mun ójafnvægi andoxunarefnakerfis og óviðráðanlegt ROS ofhleðsla skaða sortufrumur og minnka lífvænleika frumna.11,46 Í þessari rannsókn notuðum við mismunandi styrk H2O2 til að líkja eftir ROS ofhleðslu í frumum, og HEM sýndu lakara þol gagnvart H2O2 en B16F10 frumur. Þegar sortufrumur voru látnar fara í H2O2 meðferð versnaði lífvænleiki þeirra og frumufrumutíðni, en
CDP formeðferð gæti að hluta snúið þróuninni við. Á sama tíma var ROS sótthreinsað. Eins og greint hefur verið frá er virkjun NRF2/ARE andoxunarferla mikil aðferð til að hreinsa ROS í húðfrumum.14 Í tilraunum okkar var próteinmagn NRF2 og HO-1 í sortufrumum stillt upp eftir H2O2 meðferð án CDP; þetta þýðir að H2O2-framkallaðoxunarálaggetur virkjað NRF2/HO-1 brautina, en hún er ófullnægjandi til að viðhalda redoxjafnvægi og vernda frumuna gegn meiðslum. Hins vegar, CDP formeðferð jók NRF2/HO-1 andoxunarferlið og endurheimti jafnvægið. Þannig leggjum við til að CDP geti verndað sortufrumur fyrir oxunarálagsmeiðslum með því að virkja NRF2/HO-1 andoxunarferlið og hreinsa ROS.
Við komumst að því að CDP meðferð ein og sér hefur engin áhrif á ROS eða NRF2/HO-1 í sortufrumum. Þessi niðurstaða bendir til þess að CDP geti haft áhrif á redoxjafnvægi við oxunarálag, en ekki eðlilegar aðstæður. Þar að auki er NRF2/HO-1 andoxunarferillinn að sögn stjórnað af PI3K, NF-KB og MAPK boðleiðum.47,48 Í rannsókn okkar tókst CDP að virkja MAPK boðleiðina. Það er mögulegt að CDP geti virkjað NRF2/HO-1 leiðina í gegnum MAPK sem uppstillir. Eins og Slominski greindi frá eru sortufrumur streituskynjarar sem taka þátt í eftirlitsneti og virkni þeirra getur breyst hratt til að bregðast við umhverfinu.49 Við leggjum til að hlutverk CDP sé undir áhrifum af stöðu sortufrumna, það getur stuðlað að sortumyndun án þess að hafa áhrif á andoxunarefnið kerfi við venjulegar aðstæður en endurheimta redox jafnvægi undiroxunarálagskilyrði. Þess vegna er hægt að viðhalda starfsemi sortufrumna og lifun á tvo mismunandi vegu með CDP. CDP hjálpar sortufrumum að viðhalda samvægi, sem er einnig mikilvægt hlutverk sortumyndunar.50,51
Að lokum getur CDP stuðlað aðsortumyndunaf sortufrumum
með því að virkja MAPK boðleiðina. CDP getur bætt lifun sortufrumna með því að virkja NRF2/HO-1 andoxunarferilinn og hreinsa innanfrumu ROS við oxunarálag. Niðurstöður okkar eru þýðingarmiklar vegna þess að þær sýna fram á að CDP getur bæði stuðlað aðsortumyndunog verja sortufrumur fráoxunarálagáverka, sem hugsanlega er ábyrgur fyrir truflun á starfsemi sortufrumna og tapi. Niðurstöður þessarar rannsóknar benda til þess að CDP gæti verið nýtt lyf í meðhöndlun á litabreytingarsjúkdómum.

VIÐTAKNINGAR
Þessi vinna var studd af National Natural Science Foundation of China (nr. 81703101), New Xiangya Talent Projects of Third Xiangya Hospital of Central South University (nr. JY201623 og nr. 20170301), Natural Science Foundation of Hunan Province ( nr. 2018JJ3788 og nr. 2018JJ3793) og Heilbrigðisnefnd Hunan (nr. C2019173). Dr. Yibo Hu framkvæmdi meginhluta rannsóknarinnar og skrifaði handritið; Prófessor Jing Chen og Qinghai Zeng hönnuðu rannsóknina og stýrðu handritaskrifunum; Prófessor Jinhua Huang, Lihua Huang og Hong Xiang veittu tæknilega aðstoð og greindu gögnin; Dr. Yixiao Li, Ling Jiang, Yujie Ouyang, Yumeng Li, Lun Yang og Xiaojiao Zhao lögðu sitt af mörkum til hluta tilraunanna.
HAGSMUNAÁREKSTUR
Höfundar staðfesta að ekki sé um hagsmunaárekstra að ræða.
YFIRLÝSING UM AUKA gagna
Gögnin sem styðja niðurstöður þessarar rannsóknar eru fáanlegar frá samsvarandi höfundi gegn sanngjörnu beiðni.
HEIMILDIR
1. Bleuel R, Eberlein B. Meðferðarstjórnun skjaldkirtils. J Dtsch Dermatol Ges. 2018;16:1309-1313.
2. Taieb A, Meurant JM. Eigum við að forgangsraða sálfræðilegum inngripum í meðhöndlun skjaldkirtils? J Eur Acad Dermatol Venereol. 2018;32:2053-2054.
3. Picardo M, Dell'Anna ML, Ezzedine K, o.fl. Vitiligo. Nat Rev Dis Primers. 2015;1:15011.
4. Slominski A, Tobin DJ, Shibahara S, Wortsman J. Melanin litarefni í húð spendýra og hormónastjórnun þess. Physiol Rev. 2004;84:1155-1228.
5. Slominski A, Zmijewski MA, Pawelek J. L-týrósín og L-díhýdroxýfenýlalanín sem hormónalíkir eftirlitsaðilar sortufrumna. Litarfrumu sortuæxli Res. 2012;25:14-27.
6. Spritz RA. Sameiginleg erfðatengsl sem liggja til grundvallar almennum skjaldkirtilssjúkdómi og sjálfsofnæmissjúkdómi í skjaldkirtli. Skjaldkirtill. 2010;20:745-754.
7. Lin X, Tang LY, Fu WW, Kang KF. Barnaskjaldbólga í Kína: klínísk snið og ónæmisfræðilegar niðurstöður í 620 tilfellum. Am J Clin Dermatol. 2011;12:277-281.
8. Boehncke WH, Brembilla NC. Sjálfvirkar T-eitilfrumur í bólgusjúkdómum í húð. Framan Immunol. 2019;10:1198.
9. Iannella G, Greco A, Didona D, o.fl. Vitiligo: Meingerð, klínísk afbrigði og meðferðaraðferðir. Autoimmun Rev. 2016;15:335-343.
10. Forrester SJ, Kikuchi DS, Hernandes MS, o.fl. Hvarfandi súrefnistegundir í efnaskipta- og bólguboðum. Circ Res. 2018;122:877-902.
11. Denat L, Kadekaro AL, Marrot L, o.fl. Sortfrumur sem hvatar og fórnarlömb oxunarálags. J Invest Dermatol. 2014;134:1512-1518.
12. Qiu L, Song Z, Setaluri V. Oxunarálag og vitiligo: the Nrf2-ARE
merkjatengingu. J Invest Dermatol. 2014;134:2074-2076.
13. Hayes JD, Dinkova-Kostova AT. Nrf2 eftirlitsnetið veitir tengi milli redox og milliefnaskipta. Trends Biochem Sci. 2014;39:199-218.
14. Marrot L, Jones C, Perez P, Meunier JR. Mikilvægi Nrf2
leið í (mynd)-oxandi streituviðbrögðum í sortufrumum og keratínfrumum í húðþekju manna. Litarfrumu sortuæxli Res. 2008;21:79-88.
15. van Geel N, Speeckaert R, Mollet I, et al. In vivo skjaldkirtilsörvun og meðferðarlíkan: tvíblind, slembiraðað klínísk rannsókn. Litarfrumu sortuæxli Res. 2012;25:57-65.
16. Nicolaidou E, Antoniou C, Stratigos A, Katsambas AD. Mjóbanda útfjólubláa B ljósameðferð og 308-nm excimer leysir í meðhöndlun á vitiligo: endurskoðun. J Am Acad Dermatol. 2009;60:470-477.
17. Novak Z, Bonis B, Baltas E, o.fl. Xenon klóríð útfjólublá B leysir
er áhrifaríkara við að meðhöndla psoriasis og til að framkalla frumudauða T-frumu en þröngband útfjólublátt B. J Photochem Photobiol B Biol. 2002;67:32-38.
18. Xu P, Su S, Tan C, o.fl. Áhrif vatnskenndra útdrátta af Eclipse herba, Polygoni multiflora radix preparator og Rehmanniae radix preparator á sortumyndun og flutning sortufrumna manna. J Etnopharmacol. 2017;195:89-95.
19. Wang T, Zhang X, Xie W.Cistanche deserticolaYC Ma, "Desertginseng": umsögn. Am J Chin Med. 2012;40:1123-1141.
20. Guo Y, Cao L, Zhao Q, o.fl. Bráðabirgðalýsingar, andoxunarefni og lifrarverndandi virknifjölsykrafráCistanche deserticola. Int J Biol Macromol. 2016;93:678-685.
21. Cai RL, Yang MH, Shi Y, o.fl. Þreytueyðandi virkni fenýletanóíðríks þykkni úrCistanche deserticola. Phytother Res. 2010;24:313-315.
22. Zhang H, Xiang Z, Duan X, o.fl. Æxlis- og bólgueyðandi áhrif fásykra fráCistanche deserticolaútdráttur á mænuskaða. Int J Biol Macromol. 2019;124:360-367.
23. Liu Y, Wang H, Yang M, o.fl.Cistanche deserticola fjölsykrurvernda PC12 frumur gegn OGD/RP-völdum meiðslum. Biomed Pharmacother. 2018;99:671-680.
24. Song D, Cao Z, Liu Z, o.fl.Cistanche deserticola fjölsykradregur úr beinþynningu og beinupptöku með því að hindra RANKL boð og hvarfgjörn súrefnisframleiðslu. J Cell Physiol. 2018;233:9674-9684.
25. Fu C, Chen J, Lu J, o.fl. Niðurstilling á TUG1 stuðlar að sortumyndun og UVB-völdum sortumyndun. Exp Dermatol. 2019;28:730-733.
26. Johannessen CM, Johnson LA, Piccioni F, o.fl. Melanocyte ætternisáætlun veitir ónæmi gegn hömlun á MAP kínasa ferli. Náttúran. 2013;504:138-142.
27. Vachtenheim J, Borovansky J. "Umritunarlífeðlisfræði" litarefnamyndunar í sortufrumum: aðalhlutverk MITF. Exp Dermatol. 2010;19:617-627.
28. Yu N, Zhang S, Zuo F, o.fl. Ræktaðar sortufrumur úr mönnum tjá virka tolllíka viðtaka 2-4, 7 og 9. J Dermatol Sci. 2009;56:113-120.
29. Ahn JH, Park TJ, Jin SH, Kang HY. Melanocytar manna tjá virkan Toll-eins viðtaka 4. Exp Dermatol. 2008;17:412-417.
30. Reed SG, Carter D, Casper C, o.fl. Fylgni virkni GLA fjölskyldu hjálparefna. Semin Immunol. 2018;39:22-29.
31. Guo MZ, Meng M, Feng CC, o.fl. Skáldsagafjölsykrafengin frá Craterellus cornucopioides eykur ónæmisbælandi virkni í ónæmisbælandi múslíkönum með stjórnun á TLR4-NF-kappaB ferlinu. Mataraðgerð. 2019;10(8):4792-4801.
32. Wei W, Xiao HT, Bao WR, o.fl. TLR-4 gæti miðlað merkjaleiðum AstragalusfjölsykraRAP framkallaði cýtókíntjáningu RAW264.7 frumna. J Etnopharmacol. 2016;179:243-252.
33. Chen H, Yang D, Han F, o.fl. T6SS bakteríur áhrifavaldurinn EvpP kemur í veg fyrir NLRP3 bólgueyðandi virkjun með því að hindra Ca(2 plús )-háða MAPK-Jnk ferli. Cell Host Microbe. 2017;21:47-58.
34. Levy M, Shapiro H, Thaiss CA, Elinav E. NLRP6: margþættur in-Nate ónæmisskynjari. Trends Immunol. 2017;38:248-260.
35. Chen YS, Chen QZ, Wang ZJ, Hua C. Bólgueyðandi og lifrarverndandi áhrif Ganoderma lucidumfjölsykrurgegn koltetraklóríði af völdum lifrarskaða í Kunming músum. Lyfjafræði. 2019;103:143-150.
36. Tian Z, Liu Y, Yang B, o.fl. Astragalusfjölsykradregur úr ristilbólgu í músum með hömlun á NLRP3 inflammasome. Planta Med. 2017;83:70-77.
37. Jiang L, Huang J, Lu J, o.fl. Ganoderma lucidumfjölsykradregur úr sortumyndun með því að hindra paracrine áhrif keratínfrumna og trefjafruma með IL-6/STAT3/FGF2 ferli. J Cell Physiol. 2019;234:22799-22808.
38. Cai ZN, Li W, Mehmood S, et al. Áhrif affjölsykraFMP-1 frá Morchella esculenta um sortumyndun í B16F10 frumum og sebrafiskum. Mataraðgerð. 2018;9:5007-5015.
39. Zhang C, Li Z, Zhang CY, o.fl. Sameindaeiginleikar og lífvirknifjölsykrurúr alfalfa (Medicago sativa L.). Næringarefni. 2019;11:1181.
40. Coconi Linares N, Di Falco M, Benoit-Gelber I, et al. Tilvist snefilefna víkkar verulega sameindasvörun Aspergillus niger við gúargúmmíi. Ný líftækni. 2019;51:57-66.
41. Ma H, Zhang K, Jiang Q, o.fl. Einkenni plantnafjölsykrurfrá Dendrobium officinale með margvíslegum litskiljunar- og massagreiningaraðferðum. J Chromatogr A. 2018;1547:29-36.
42. Dong Q, Yao J, Fang JN, Ding K. Byggingareinkenni og ónæmisfræðileg virkni tveggja köldu vatni sem hægt er að vinna úrfjölsykrurfráCistanche deserticolaYC Ma. Kolvetni Res. 2007;342:1343-1349.
43. Slominski AT, Zmijewski MA, Plonka PM, et al. Hvernig UV ljós snertir heilann og innkirtlakerfið í gegnum húðina og hvers vegna. Innkirtlafræði. 2018;159:1992-2007.
44. Schalke S. Ný gögn um oflitunarsjúkdóma. J Eur Acad Dermatol Venereol. 2017;31(Viðauki 5):18-21.
45. Glassman SJ. Vitiligo, hvarfgjarnar súrefnistegundir og T-frumur. Clin Sci. 2011;120:99-120.
46. Ristow M. Að afhjúpa sannleikann um andoxunarefni: mítóhormesis útskýrir heilsufarsávinning af völdum ROS. Nat Med. 2014;20:709-711.
47. Balogun E, Hoque M, Gong P, o.fl. Curcumin virkjar hem súrefnisasa-1 genið með stjórnun á Nrf2 og andoxunarefnasvöruninni. Biochem J. 2003;371:887-895.
48. Paine A, Eiz-Vesper B, Blasczyk R, Immenschuh S. Signaling to
hem súrefnisasa-1 og bólgueyðandi meðferðarmöguleika þess.
Biochem Pharmacol. 2010;80:1895-1903.
49. Slominski A, Paus R, Schadendorf D. Sortfrumur sem "skyn-" og stjórnfrumur í húðþekju. J Theor Biol. 1993;164:103-120.
50. Slominski RM, Zmijewski MA, Slominski AT. Hlutverk melanín litarefnis í sortuæxlum. Exp Dermatol. 2015;24:258-259.
51. Slominski A, Kim TK, Brozyna AA, o.fl. Hlutverk sortumyndunar í stjórnun sortuæxlahegðunar: sortumyndun leiðir til örvunar á HIF-1alfa tjáningu og HIF-háðum fylgiferlum. Arch Biochem Biophys. 2014;563:79-93.
