Árleg endurskoðun lyfjafræði og eiturefnafræði 1. hluti
Jul 28, 2023
Leitarorð
Krabbamein, hjarta- og æðakerfi, innkirtla, estrógen, ónæmi, efnaskipti.
Ágrip
Aðgerðir estrógena og skyldra estrógensameinda eru flóknar og margþættar hjá báðum kynjum. Fjölbreytt úrval af náttúrulegum, tilbúnum og lækningasameindum miða á ferli sem framleiða og bregðast við estrógenum. Margir viðtakar dreifa þessum viðbrögðum, þar á meðal klassískir estrógenviðtakar kjarnahormónaviðtakafjölskyldunnar (estrógenviðtakar og ), sem virka að miklu leyti sem bindillvirkjaðir umritunarþættir, og 7-transhimnu G próteintengi estrógenviðtakinn, GPER, sem virkjar fjölbreytt úrval af merkjaleiðum.
Estrógen er eitt af mikilvægu hormónunum í kvenlíkamanum, sem gegnir mikilvægu hlutverki í tíðahringnum, meðgöngu og tíðahvörfum. Hins vegar hafa rannsóknir á undanförnum árum einnig leitt í ljós að estrógen getur einnig haft áhrif á ónæmi.
Í fyrsta lagi getur estrógen aukið ónæmissvörun líkamans. Sumar rannsóknir hafa leitt í ljós að á tímabilum með hærra estrógenmagni í tíðahring kvenna er ónæmiskerfi kvenna einnig sterkara og betur í stakk búið til að berjast gegn sýkla. Að auki leiddi rannsóknin einnig í ljós að estrógen getur aukið framleiðslu og virkni T-frumna, sem gerir bólgusvörun öflugri og verndar þannig líkamann gegn sýkingum á áhrifaríkan hátt.
Að auki getur estrógen einnig verndað ónæmiskerfið gegn áhrifum öldrunar. Með aldrinum mun ónæmiskerfi líkamans smám saman hrörna, viðkvæmt fyrir sjúkdómum. Og sumar rannsóknir hafa leitt í ljós að estrógen getur hægt á öldrun ónæmiskerfisins, bætt virkni þess og gert líkamann ónæmari fyrir sjúkdómum. Að lokum getur estrógen einnig haft verndandi áhrif gegn ákveðnum sjálfsofnæmissjúkdómum. Sem dæmi má nefna að MS, sjálfsofnæmissjúkdómur sem hefur áhrif á taugakerfið, hefur fundist í sumum rannsóknum draga úr einkennum hjá konum á meðgöngu, hugsanlega vegna verndaráhrifa estrógens.
Þess vegna, frá ofangreindum þáttum, hefur estrógen jákvæð áhrif á friðhelgi okkar. Auðvitað er ekki þar með sagt að meira estrógen sé betra, því of mikið estrógen getur valdið öðrum vandamálum. Aðeins með því að viðhalda góðri heilsu og eðlilegri stjórn á estrógenmagni getum við sannarlega náð sterku ónæmi og góða heilsu. Frá þessu sjónarhorni þurfum við að bæta friðhelgi. Cistanche getur verulega bætt ónæmi vegna þess að fjölsykrurnar í kjötinu geta stjórnað ónæmissvörun ónæmiskerfis mannsins, bætt streitugetu ónæmisfrumna og aukið bakteríudrepandi áhrif ónæmisfrumna.

Smelltu cistanche tubulosa kostir
Lyfjafræði og virknihlutverk GPER í lífeðlisfræði og sjúkdómum sýna mikilvæg hlutverk í svörun við bæði náttúrulegum og tilbúnum estrógenefnasamböndum í fjölmörgum lífeðlisfræðilegum kerfum. Þessar aðgerðir hafa áhrif á meðhöndlun á ótal sjúkdómsástæðum, þar á meðal krabbameini, hjarta- og æðasjúkdómum og efnaskiptasjúkdómum. Þessi úttekt fjallar um flókna lyfjafræði GPER og dregur saman helstu lífeðlisfræðilegu virkni GPER og meðferðaráhrif og áframhaldandi notkun GPER-miðaðra efnasambanda.
KYNNING
Estrógen kalla fram margs konar áhrif um allan líkamann í nánast öllum líffærum, vefjum og lífeðlisfræðilegum kerfum. Þrátt fyrir að það sé aðallega viðurkennt sem kvenkyns kynhormónið, sem stjórnar kynþroska á kynþroskaskeiði, tíðahringnum og meðgöngu á æxlunarárunum, og, með því að myndun þess hættir, tíðahvörf, hefur estrógen einnig mikilvæg og fjölbreytt hlutverk í hjarta- og æðakerfi, efnaskiptum og taugafræðilegar aðgerðir sem og í mörgum öðrum kerfum.
Vegna mikilvægra virkni þess í æxlunarvef (aðallega í legi en einnig brjóstum), er estrógen og afleiður þess notað í getnaðarvarnarlyfjum, hormónauppbótarmeðferðum við tíðahvörf og meðferð á hormónasvarandi (þ.e. ER-jákvæðum) brjóstum. krabbamein. Hið fjölbreytta hlutverk estrógens er ef til vill best lýst með einkennum og lífeðlisfræðilegum breytingum sem konur upplifa eftir tíðahvörf, þar á meðal tíðablæðingar, þurrkur í leggöngum, þvagleka, missi brjóstafyllingar, hitakóf/kuldahrollur/nætursviti, svefnerfiðleikar, skapbreytingar, þyngdaraukning/hægt efnaskipti, þynnt hár og þurr húð (1).
Hins vegar koma viðbótarhlutverk estrógens í ljós vegna aukinnar hættu eftir tíðahvörf og minni hættu eftir hormónaskipti á fjölmörgum sjúkdómum, þar á meðal hjarta- og æðasjúkdómum (td kransæðasjúkdómum, háþrýstingi, heilablóðfalli), beinþynningu, offitu og blóðfituhækkun, sykursýki og taugafræðilegar breytingar (td þunglyndi og heilabilun) (2, 3).
Estrógen gegnir einnig mikilvægu hlutverki í um 80 prósent brjóstakrabbameins, þar sem æxlisvöxtur er örvaður af og oft háður estrógeni. Þessi estrógenfíkn hefur leitt til margvíslegra lækningaaðferða til að meðhöndla brjóstakrabbamein sem felur í sér að hindra framleiðslu á estrógeni í gegnum ensímið arómatasa og miða á einn af viðtökum þess (ER ) með annað hvort hömlun eða niðurbroti (4, 5).

Lyfjafræðin í kringum estrógenviðtaka er fjölbreytt og flókin (6, 7). Auk margvíslegra forma estrógens sem framleitt er í mannslíkamanum [aðallega estróni (E1), 17 -estradíóls (E2), estríóls (E3) og esttróls (E4) (8)], kalla fram náttúruleg og manngerð xenoestrogen estrógenvirkni (9, 10).
Skilgreiningin á örvandi áhrifum í legi (ígangur og fjölgun sem staðlaðir endapunktar), eins og E2 gerir, er hagnýt en vanrækir víðtækari áhrif, með lítið tillit til aðgerða í öðrum vefjum. Náttúruleg jurta- eða sveppaafleidd og manngerð xenoestrógen, einnig nefnd umhverfisestrógen eða innkirtlatruflandi efnasambönd, eru alls staðar nálæg í umhverfinu og mataræði og hafa áhrif á líffræði og heilsu manna (9, 11).
Lyf sem miða að estrógenmagni/myndun og viðtakavirkni gegna hlutverki við meðferð margra sjúkdóma og sjúkdóma (12, 13), einkum krabbameins (5, 14). Þess vegna er mikilvægt að skilja verkunarmáta varðandi marga estrógenviðtaka. Í þessari umfjöllun lýsum við lyfjafræði og meðferðaráhrifum þessara fjölbreyttu efnasambanda með sérstakri tilvísun til virkni þeirra í gegnum 7-transhimnu G próteintengt estrógenviðtakann (GPER).
ESTROGENVITALAR: ER / OG GPER
Tvær aðskildar viðtakafjölskyldur miðla fjölbreyttri umritunarvirkni estrógens (þ.e. erfðafræðileg) og hröðum boðefnastarfsemi (þ.e. nongenomic) starfsemi (6, 7). Þrátt fyrir að snemma tilraunir hafi bent á hraðboð af völdum estrógena [td hringlaga adenósín mónófosfat (cAMP) framleiðslu og Ca2 plús upptöku], var umritunarvirkni ER fljótlega ráðandi á sviðinu.
Áframhaldandi fregnir af hröðum verkun estrógens og annarra stera leiddu til tilgátunnar um himnutengd form ER á tíunda áratugnum (15). Árið 1996 var viðtaki sem var einsleitur ER klónaður og sýndur á virkni að hann væri annað ER, sem leiddi til núverandi flokkunarkerfis ER og ER (16, 17), en samhliða munaðarlausu 7- G-próteintengt yfirhimnu viðtakinn (GPCR) var klónaður og kallaður GPR30 (18).
Árið 2000 var sýnt fram á að GPR30 miðlaði hraðri virkjun utanfrumumerkjastýrðs kínasa (ERK) sem svar við estrógeni, sem gaf fyrstu vísbendingar um virkni þess sem virkan estrógenviðtaka (19). Þessari uppgötvun var fylgt eftir með því að sýna fram á sértæka estrógenbindingu, þar sem bæði tritiated (20) og flúrljómandi afleiður (21) voru notaðar árið 2005, sem leiddi til opinberrar útnefningar GPR30 sem GPER af International Union of Basic and Clinical Pharmacology árið 2007 (22) .
Sýning á virkni þess sem klassískt GPCR var veitt með áhrifum gúanósíns-5 -þrífosfats (GTP) (sérstaklega GTP S, með virkjun og sundrun heterótrímerískra G próteina) á að draga úr bindilbindingu með því að breyta viðtakanum í lægri sækniástand sem og með aukinni GTP S bindingu í viðurvist estrógens (20).
Sem GPCR, aðal staður GPER fyrir undirfrumustaðsetningu, eru endoplasmic reticulum og Golgi tæki (21) óvenjulegt þó ekki einstakt (23). Í sumum frumum er greinanlegt GPER að finna í plasmahimnunni, þó að jafnvel í slíkum frumum sé flest til staðar í innanfrumuhimnum í jafnvægi (23).
Þar sem estrógen eru gegndræp fyrir frumum (24, 25) og virkja ER innanfrumu, og þar sem flest ER er staðbundið í kjarnanum við stöðugt ástand (26), benda rannsóknir með gegndræpum og ógegndræpum estrógenafleiðum til þess að GPER merki aðallega frá innanfrumustað(um) (27). Rannsóknir á viðtakasölu benda til þess að GPER sem tjáð er á frumuyfirborði sé innbyrðis innbyrðis á bindilóháðan hátt, í samræmi við meirihluta viðtaka sem sést innanfrumu við jafnvægi (23).
Merkjasending sem GPER hefur frumkvæði að eiga sér stað í gegnum fjölmargar leiðir. Tenging á sér stað með mörgum heterótrímerískum G próteinum, fyrst og fremst G s (28) og Gi (21), auk G-miðlaðra boðefna (19). Þar að auki, mikið ef ekki öll boð sem koma af stað með GPER virkjun felur í sér umvirkjun á húðþekjuvaxtarþáttarviðtaka (EGFR) (19), leið sem lýst er fyrir marga GPCR (29).
Þessi leið felur í sér G-miðlaða virkjun á Src, sem leiðir til 5 1 nýliðunar og matrix metalloproteinase (MMP)-miðlaðrar losunar á heparan-bindandi EGF-líkum vaxtarþáttum, sem síðan umvirkjar EGFR, með í kjölfarið virkjun á mörgum viðbótarferlum, ss. sem ERK og PI3K/Akt (29). Meðan ERK virkjun leiðir til fjölgunarboða og Elk-1- miðlaðrar umritunarstjórnunar (30), leiðir Akt virkjun til fosfórunar á bæði eNOS (31), sem leiðir til NO framleiðslu, og Foxo3 (32), sem leiðir til prosurvival merki.
GPER virkjun leiðir einnig til virkjunar adenýlýlsýklasa, sem framleiðir cAMP, sem aftur virkjar prótein kínasa A (PKA), og umritunartilvik með cAMP svörun frumefnisbindandi próteini (CREB) (33, 34). Þannig að þrátt fyrir að almennt sé talið að merkjasendingar um GPER miðli hröðum boðefnum sem ekki eru erfðafræðilegar, þá fela niðurstreymisviðburðir þessara snemma merkjaatburða í sér víðtæka erfðafræðilega stjórnun, eins og ER-miðluð merkjasending felur í sér hraða atburði til viðbótar við klassíska umritunarstjórnun.

GPER LIGANDS OG LYFJAFRÆÐI
Lausalaus bindillbinding með mörgum mismunandi byggingarflokkum og fjölbreyttri lyfjafræði eru einkenni bæði klassísks (kjarna) ER / og GPER. Öflugasta estrógenhormónið, E2, er fitusækið fenól, og efnasambönd sem hafa þessa virkni eru oft krossviðbragðsbindlar.
Greining og einkenni lyfjafræðilega virkra GPER bindla voru ítarlega endurskoðuð árið 2015 (7), og nýleg þróun og uppgötvanir sem geta haft áhrif á heilsu manna og klínískar notkunar eru í brennidepli þessarar endurskoðunar.
Umfang efnasambanda með viðurkennd líffræðileg áhrif í gegnum GPER heldur áfram að vaxa og felur í sér lyf og efni sem eru tekin inn í matvæli, fæðubótarefni og önnur umhverfisáhrif sem eru samþykkt af bandarísku matvæla- og lyfjaeftirlitinu (FDA). Það er mikilvægt að viðurkenna að bindlar með mjög ólíka GPER-bindandi skyldleika geta stjórnað fjölbreyttum boðleiðum sem ekki eru erfðafræðilegar sem að lokum hafa áhrif á erfðafræðilegar niðurstöður.
Þessi atburðarás býður upp á áskoranir við að túlka genatjáningu og eiturefnafræðileg áhrif sem gætu komið fram í skömmtum sem eru verulega lægri en mæld skyldleiki eða starfsemi myndi spá fyrir um, í takt við athuganir á því að innkirtlatruflanir sýna oft ekki eintóna skammta-svörunartengsl (35).
GPER lyfjafræði með náttúrulegum sterum og afleiðum
Competitive binding assays with radiolabeled or fluorescent probes revealed that E2 has the highest GPER binding affinity (3–6 nM) and greater than 1,000-fold selectivity compared to other steroid hormones such as progesterone, testosterone, and cortisol (20). Whether and how aldosterone may act in concert with or through GPER remain a complex and controversial question (36, 37), particularly given the demonstrated lack of binding (38). The physiologically relevant estrogen E1 has a much lower affinity for GPER (>10 μM) (20).
The 16α-hydroxy analog E3 (20) and the catechol metabolite 2-hydroxy-17β-estradiol (39) have relatively low GPER binding affinities (>1 μM og 0.1–1 μM) en virka sem veikir andstæðingar (Mynd 1). Aftur á móti sýnir fitusækna umbrotsefnið 2-metoxýestradíól tiltölulega mikla sækni (10 nM) og virkar sem örvandi (40–44). Nýlega hefur verið sýnt fram á að oxýsteról 27-hýdroxýkólesteról bindur GPER (með sækni upp á um það bil 1 μM) og virkar sem örvandi í ER-neikvæðum brjóstakrabbameinsfrumum (45).
The 17β-d-glucuronide metabolite of E2 has low GPER binding affinity (>50 μM) og tilkynnt um virkni örva (46), en túlkun á niðurstöðum úr þessum tegundum samtengda eru flóknar vegna næmis fyrir efna- eða ensímvatnsrofi sem losar E2. Svipaðar varúðarreglur eru viðeigandi með því að nota dehýdróepíandrósterón (DHEA) í frumum og sérstaklega in vivo rannsóknir þar sem lífmyndun til að framleiða E2 getur átt sér stað (47). Hin tilbúna estrógenafleiða fulvestrant [sértækur estrógenviðtaka niðurstýring/niðurbrotsstýring (SERD)] virkar sem hreinn ER mótlyf en veldur einnig ER niðurbroti vegna formbreytinga sem orsakast af útvíkkuðum 7 viðauka í bindilbundinni uppbyggingu. Þetta lyf er FDA-samþykkt fyrir langt gengnu ER-jákvæðu brjóstakrabbameini en virkar einnig sem GPER örvandi (19), sem sýnir þörfina á að taka GPER með þegar sniðið er að sértækni viðtaka til að þróa sértækari lyf með færri hugsanleg áhrif utan markmiðs.
ER- og GPER-binding, virknisvörun og staðsetning bindils á E2-samböndum með flúrljómandi litarefnum eða klólötum hafa verið notuð til að magngreina, einkenna og sjá bindingu og virkni bindilsins á undirfrumu/frumu- (21, 27) og lífverustigi (48), í sömu röð. Próteolysis-miðaða chimeras (PROTAC), byggðar á litlum sameindum tengdum E3 ubiquitin ligasa bindli sem brýtur niður markið, eru í mati sem stefna fyrir þróun nýrra krabbameinslyfja (49), með kjarnaviðtökum sem bjóða upp á mikilvægt skotmark (50 ).
Estrógenchimera (E2-PROTACs), sem fyrst var lýst árið 2005 (51), hefur nýlega verið greint frá því að þeir bindi bæði GPER og ER með tiltölulega mikilli sækni (~30 nM og 10–20 nM, í sömu röð), sem leiðir til niðurbrot á ER / sem og GPER í MCF7 og SKBR3 frumulínum án þess að hafa áhrif á magn prógesterónviðtaka (52). PROTACs veita aðra nálgun til að miða á plasmahimnu og innanfrumu estrógenviðtaka sem gætu gert viðtakasértækt niðurbrot byggt á sértækum viðtakabindlum.

Xenoestrogens sem GPER bindlar
Það er vaxandi viðurkenning á hlutverki GPER í innkirtlaröskun með útsetningu fyrir náttúrulegum og tilbúnum xenoestrógenum sem koma frá fæðuinntöku, heilsu og fæðubótarefnum og umhverfisáhrifum fyrir landbúnaðar- og iðnaðarefnasambönd, þar með talið fjölliður og niðurbrotsafurðir þeirra.
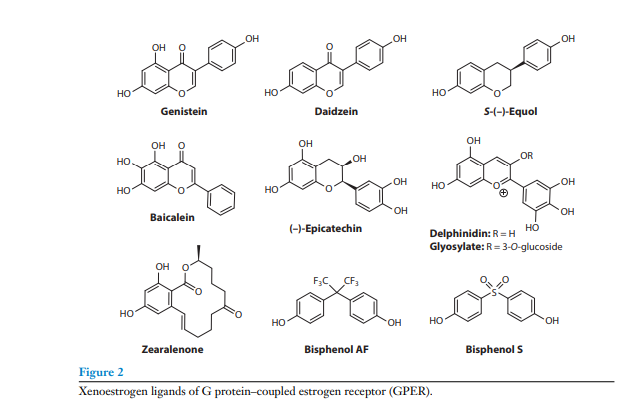
Fjöldi viðurkenndra xenoestrógena er yfirþyrmandi og þó fyrri rannsóknir hafi fyrst og fremst beinst að ER / , virkja mörg þessara efnasambanda GPER, með hugsanlegum afleiðingum á taugafrumuferli (53), og krabbamein í brjóstum (54), blöðruhálskirtli (55), og meltingarfæri (56). Breidd mögulegra GPER bindla kom í ljós með rannsókn sem sýndi nánast gagnagrunn með 30.926 náttúrulegum vörum og auðkenndu 500 efnasambönd, sem tákna fjölbreytta byggingarflokka sem innihéldu flavonoids, isoflavonoids, chalcones, coumestan, stilbenes, lignans, ginsenocids, and tetra57hydrofurandiol ( ). Tilvist fenóls og vatnsfælna vinnupalla er einkennandi eiginleiki margra xenoestrogen efnasambanda.
Ísóflavónin genistein og daidzein eru plöntuestrógen sem eru mikið neytt beint úr sojaafurðum og eru oft tekin sem fæðubótarefni í þeim tilgangi að draga úr tíðahvörfseinkennum, bæta efnaskipti, draga úr hjarta- og æðasjúkdómum eða koma í veg fyrir ákveðin hormónatengd krabbamein (Mynd 2). Þessi efnasambönd eru með fenólhóp í 3-stöðu 4H-chromen-4-eins kjarnans og bindast GPER með mikilli sækni. Kristallað natríumsalt tvíhýdrat af genisteini, nefnt AXP107-11, næmdur gemcitabine krabbameinslyfjameðferð í briskirtilkrabbameini í briskirtilkrabbameini sem er af sjúklingum afleiddum xenografts á samverkandi hátt með virkjun GPER og mítógenvirkjaður próteinkínasa (MAPK) merkja (58). ,
GPER hefur verið bendlað við rannsóknir sem sýna fram á að genistein dregur úr bólgu í líkani af Parkinsonsveiki, hindrar örvun örvera og verndar dópamínvirkar taugafrumur (59); verndar gegn oxunarálagi í lifrarfrumum (60); og bætir glúkósaþol og hitamyndun hvíts fituvef (61).

Daidzein er umbreytt í S-(−)-equol af bakteríum í þörmum spendýra og einstakar efnaskiptabreytingar leiða til víðtækrar útsetningar. S-equol miðaði á GPER til að stuðla að insúlínseytingu af völdum glúkósa frá brisfrumum og koma í veg fyrir seytingu glúkagonlíks peptíðs -1 frá innkirtla L frumum (62); virkjað GPER boð, með áhrifum á sléttar vöðvafrumur í æðum (63); hamlaði framleiðslu nituroxíðs og minnkaði tjáningu á framkallanlegum NO syntasa í lípópólýsykru-örvuðum stjarnfrumum (64); og framkallaði frumufjölgun og flæði í stjarnfrumum sem voru veikt af GPER mótlyfinu G15 en ekki af SERD/GPER örva fulvestrant (65). Genistein, daidzein og S-(-)-equol jók flutning glial frumna með því að virkja GPER boð og rannsóknir á sameindatengingu benda til þess að þessi þrjú efnasambönd geti tengst GPER í sömu stöðu og E2 (65).
For more information:1950477648nn@gmail.com
