Áætluninni um vefjamyndun í nýrum er stjórnað af MicroRNA sem stjórnar oxunarefnaskiptum
Mar 29, 2022
Tengiliður:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Vernica Miguela,*, Ricardo Ramos, Laura García-Bermejob, Diego Rodríguez-Puyolc, d.
Santiago Lamesa,**
a Program of Physiological and Pathological Processes, Centro de Biología Molecular "Severo Ochoa" (CSIC-UAM), 28049, Madríd, Spáni
b Genomic Facility, Parque Científico de Madrid, Madrid, Spáni
c Meinafræðideild, Hospital Universitario "Ramn y Cajal", IRYCIS, Madríd, Spáni
d Læknadeild og sérgreinar lækna, Rannsóknastofnun háskólasjúkrahússins "Príncipe de Asturias," IRYCIS, Universidad de Alcala´, Alcala´ de Henares, Madrid, Spáni
Lykilorð: MicroRNAS, nýrnatrefjun, fitusýruoxun, utanfrumu fylki, CPT1A, Hvatberar

cistanche líkamsbygging er mjög góð fyrir nýrnastarfsemi
A B S T R A C T
Óhófleg uppsöfnun utanfrumufylkis (ECM) er einkenni trefjasjúkdóma. Í nýrum er það síðasta algeng leið algengra sjúkdóma, sem leiðir til langvarandi nýrnabilunar. Þó að cýtókín eins og TGF- gegni grundvallarhlutverki í umbreytingu vöðvafíbróblasta, hefur nýleg rannsókn sýnt að truflun á starfsemi hvatbera og gölluð fitusýruoxun (FAO), sem skerða aðalorkugjafa nýrnapípla þekjufrumna, hefur verið lagt til grundvallarþátttöku. við þróun og framgang bandvefsmyndunar í nýrum. Greint hefur verið frá því að ör-RNA (miRNA), sem stjórna tjáningu gena eftir umritun, stjórni trefjamyndun í nýrum. Til að bera kennsl á miRNA sem taka þátt í efnaskiptatruflunum á bandvefsmyndun í nýrum, gerðum við miRNA fylkisskimun í músarlíkani af einhliða þvagteppu (UUO). MiR-150-5p og miR-495-3p voru valdir fyrir tengsl þeirra við meinafræði manna, hlutverk þeirra í umbrotum hvatbera og miðun þeirra á fitusýruflutningsensímið CPT1A. Við fundum 2- og 4-falt uppstillingu á miR-150-5p og miR-495-5p, í sömu röð, bæði í UUO og fólínsýru-framkölluðum nýrnakvilla (FAN) líkaninu , á meðan TGF- 1 hækkaði tjáningu þeirra í nýrnapípluþekjufrumulínu úr mönnum HKC-8. Þessi miRNA sameinuðust TGF- varðandi trefjavirk áhrif þess með því að auka bandvefstengdu merkin Acta2, Col1 1 og Fn1. Líforkurannsóknir sýndu lækkun á FAO-tengdri súrefnisnotkun (OCR) í HKC-8 frumum í viðurvist beggja miRNA. Stöðugt minnkaði tjáningarstig hvatberatengdra markgenanna CPT1A, PGC1 og hvatbera umritunarþáttar A (TFAM), um helming í nýrnaþekjufrumum sem verða fyrir þessum miRNA. Aftur á móti fundum við ekki breytingar á massa hvatbera og getu yfirhimnu (ΔѰm) eða framleiðslu hvatbera ofuroxíðs róttækra anjóna. Gögnin okkar styðja að miR-150 og miR- 495 geti stuðlað að vefjamyndun í nýrum með því að versna efnaskiptabilunina sem er mjög mikilvæg í pípulaga þekjufrumum, sem að lokum leiðir til bandvefsmyndunar.
1. Inngangur
Langvinnur nýrnasjúkdómur (CKD) er klínískt ástand þar sem skert nýrnastarfsemi er viðhaldið. Það er almennt talið vera óafturkræft og framsækið. Það táknar mikilvægt lýðheilsuvandamál sem getur haft áhrif á 12-14 prósent almennings [1]. Það getur verið til staðar hjá um það bil 30-40 prósentum sjúklinga með mjög algenga sjúkdóma eins og sykursýki og háþrýsting, þar sem það stuðlar að því að segja til um þróun og horfur. Burtséð frá orsökum sjúkdómsins leiðir versnun langvinnan nýrnasjúkdóms til píplu-millivefs- og gauklatrefjunar [2]. Tubulo-interstitial fibrosis felur í sér stækkun á bilinu milli pípulaga grunnhimnu og peritubular capillaries með útfellingu fylkispróteina (ECM) (aðallega kollagen tegund I og III og fibronectin) í tengslum við bólgufrumur, píplufrumuvökva og uppsöfnun vöðvafíbroblasta. [3].
Umbreytandi vaxtarþáttur- (TGF-) er talinn afgerandi alls staðar nálægur pro-fibrotic cýtókín og aðalstjórnandi aðgreiningar vöðvafíbróblasta í bandvefsmyndun [4]. Nýlegar rannsóknir hafa sýnt að alþjóðlegur galli í fitusýruoxun (FAO), sem leiðir til málamiðlunar á aðalorkugjafa fyrir pípulaga þekjufrumna, gegnir mikilvægu hlutverki í þróun nýrnatrefjunar [5,6]. TGF- bælir FAO á SMAD3- og PGC1A háðan hátt og hefur þar af leiðandi áhrif á umritunarstýringar á fitusýruupptöku og oxun, þar á meðal CPT1A [5]. Breytingar á FAO leiða að lokum til fitusöfnunar innan frumu og ATP tæmingu, sem leiðir til bandvefs [5,7]. Þannig geta aðferðir sem miða að því að endurheimta efnaskiptatruflanir sem starfa við langvinnan nýrnasjúkdóm veitt meðferðarmöguleika [8].
MicroRNAs (miRNAs) hafa komið fram sem mikilvægir eftirlitsaðilar fyrir tjáningu gena með virkni þeirra á stjórnun eftir umritun. Í nýrum hefur verið sýnt fram á að miRs gegna mikilvægu hlutverki í nýrnamyndun, samvægi og sjúkdómum [9]. MiRNA eru einnig fær um að stjórna trefjaferli og hafa verið kölluð „trefjamyndun“ [10]. Þar að auki, vegna skorts á árangursríkri meðferð til að koma í veg fyrir eða afturkalla trefjamyndun í nýrum [11], hefur meðhöndlun á tjáningu miRNA með in vivo afhendingu miRNA líkja eða hemla verið lögð til sem efnileg meðferðaraðferð fyrir langvinnan nýrnasjúkdóm [12]. Að auki geta miRNA í blóðrás verið greiningar- og jafnvel forspár lífvísar [13].
MiRNA-miðluð stjórnun á bandvefsmyndun nýrna á sér aðallega stað með því að stjórna TGF- 1 merkjum á frumuháðan og samhengisháðan hátt, með því að nota Smad leiðina sem eitt af aðalmarkmiðunum [14]. Í fyrri vinnu höfum við greint nokkur miRNA sem hafa áhrif á bandvefsmyndun í nýrum með því að stjórna ákveðnum efnaskiptaferlum [15,16]. Oftjáning miR-9-5p kemur í veg fyrir aðgreiningu nýrnafruma í pípulaga þekjuvef og endurforritar vefjagigtartengda efnaskiptatruflun [16], en tap á starfsemi miR-33, annað hvort erfðafræðilega eða lyfjafræðilega, leiðir til aukinnar FAO og koma í veg fyrir fitusöfnun í pípulaga þekjufrumum. Þetta tengist auknu orkuframboði, bættri líforku hvatbera og fyrirbyggjandi tilraunabundinni nýrnatrefjun [15]. Þannig eru miRNA sem stjórna líforku frumna einnig fær um að stjórna trefjamyndun í nýrum. Í þessari rannsókn höfum við beitt miRNA fylki byggðri stefnu í einhliða þvagrásarstíflu (UUO) líkaninu fyrir langvarandi nýrnaskaða til að bera kennsl á miRNA sem taka þátt í nýrnatrefjasvipgerðinni með breytingum á efnaskiptaferlum. Með því að velja nokkur gen sem tengjast starfsemi hvatbera (CPT1A, TFAM, PGC1A), auðkenndum við bæði miR-150 og miR-495 sem miRNA sem geta dregið úr FAO-tengdri súrefnisnotkun (OCR) og stuðlað að TGF{ {21}}örvaði trefjamyndandi umbreytingu í nýrnapípluþekjufrumulínu úr mönnum HKC-8. Niðurstöður okkar undirstrika mikilvægi miRNA sem efnaskiptastýringar hvatbera sem taka þátt í trefjamyndun í nýrum.

2. Efniviður og aðferðir
Frumulínur og ræktunarskilyrði. Nærpípulaga þekjufrumur úr mönnum (HKC-8) voru ræktaðar í DMEM/F12 (Dulbecco's modified Eagle's medium 1:1 (v/v)) (Corning, New York, NY) bætt við 15 mM HEPES, 5 prósent (rúmmál/rúmmál) nautgripasermi fósturs (FBS)
(HyClone Laboratories, Logan, UT), 1x Insulin-Transferrin-Selenium (ITS) (Gibco, Rockville, MD), 0.5 ug/ml hýdrókortisón (Sigma, St. Louis, MO), 50 einingar/ mL penicillíns og 50 ug/mL streptómýsíns (Gibco, Rockville, MD) við 37◦ C og 5 prósent CO2. Þessi frumulína var góðfúslega útveguð af rannsóknarstofu Dr. Susztak (Philadelphia, Pennsylvania, Bandaríkjunum). Meðferðir með raðbrigða 10 ng/ml TGF- 1 úr mönnum (R&D Systems, Minneapolis, MN) voru framkvæmdar eftir sermislausa hungursneyð á HKC-8 frumum í 12 klst.
Transfection aðferð. Frumum var sáð í 60 mm ræktunarskál til að ná 70 prósenta samruna. Þau voru sýkt með 40 nM af annaðhvort mirVana™ miRNA líkingu af miR-150, miR-495 eða mirVana™ miRNA líkja neikvæðri stjórn (Ambion fyrirtæki, Bandaríkjunum) með því að nota lipofectamine 2000 (Invitrogen, Carlsbad, CA) . Frumur voru ræktaðar með lipofectamine-pre-miRNA 37 ◦ C í 6 klst. Í kjölfarið var 5 ml af ferskum miðli sem innihélt 10 prósent FBS bætt við ræktunardiskana og frumunum var haldið í ræktun í 6 klst þar til þær voru notaðar í síðari tilraunir. Ef um var að ræða samhliða meðferð með TGF- 1 var henni borið á frumurnar eftir oftjáningu miRNAs samkvæmt fyrri hluta.
Ónæmisblóð. Frumur voru þvegnar í PBS, einsleitar og ljósaðar í 100 μL RIPA lýsisbuffi sem innihélt 150 mM NaCl, 0,1 prósent SDS, 1 prósent natríumdeoxýkólat, 1 prósent NP-40 og 25 mM Tris– HCl pH 7,6, í viðurvist próteasa (Complete, Roche Diagnostics, Mannheim, Þýskalandi) og fosfatasahemla (Sigma-Aldrich, St. Louis, MO) og safnað með skafa. Fjórðungur stykki af hverju nýrnasýni (fengið eftir krufningu í tvennt bæði eftir endilöngu og þversum) var einsleitt í 300 ul RIPA biðminni með 5 mm ryðfríu stáli perlum (Qiagen, Valencia, CA) með því að nota TissueLyser LT (Qiagen, Valencia, CA) titrandi við 50 Hz í 15 mínútur við 4 ◦ C. Sýnin voru hreinsuð með skilvindu við 10,000 g í 15 mínútur við 4 ◦ C. Kúlunni var síðan hent og flotinu var haldið sem próteinlýsi. Próteinstyrkur var ákvarðaður með BCA próteingreiningarsettinu (Thermo Scientific, Rockford, IL) og var mældur í Glomax®-Multi Detection System (Promega, Madison, WI). Jafnt magn af próteini (10–50 ug) úr heildarútdrættinum var aðskilið á 8–10 prósent SDS–pólýakrýlamíð hlaupum og flutt yfir á nítrósellulósablökuhimnur (GE Healthcare, Chicago, IL) við 12 V í 20 mínútur í hálfþurrku Trans-Blot Turbo kerfi (Bio-Rad, Hercules, Kalifornía).
Himnur voru lokaðar með ræktun í 1 klst með 5 prósent fitulausri mjólk í PBS sem innihélt 0,5 prósent Tween-20 og þeytt yfir nótt með sérstökum mótefnum: CPT1A (Ab128568, Abcam; 1:1{ {26}}; 4 ◦ C yfir nótt), -SMA (sc-32251, Santa Cruz líftækni; 1:1000; 4 ◦ C yfir nótt), GAPDH (MAB374, Millipore; 1:15000; 1 klst., stofuhiti ). Eftir ræktun með IRDye 800 geit-and-kanínu og IRDye 600 geit-and-mús (1:15.000, LI-COR Biosciences, Lincoln, NE) aukamótefni, voru himnur teknar í þrígang með Odyssey Infrared Imaging System (LI-COR Biosciences, Lincoln, NE). Bandþéttnimæling var framkvæmd með því að nota ImageJ 1.48 hugbúnaðinn (http://rsb.info.nih.gov/ij) og hlutfallsleg próteintjáning var ákvörðuð með því að staðla í GAPDH. Brotbreytingar voru staðlaðar að gildum viðmiðunarástands.
RNA útdráttur. Heildar-RNA var dregið úr HKC-8 frumum eða músarnýrum með því að nota miRNeasy Mini Kit (Qiagen, Valencia, CA) samkvæmt leiðbeiningum framleiðanda. RNA magn og gæði voru ákvörðuð við 260 nm með Nanodrop-1000 litrófsmæli (Thermo Scientific, Rockford, IL).
Greining á mRNA tjáningu. Öfug umritun (RT) var framkvæmd með 500 ng af heildar-RNA með því að nota iScript™ cDNA Synthesis Kit (Bio-Rad, Hercules, CA). qRT–PCR var framkvæmt með iQ™SYBR Green Supermix (Bio-Rad, Hercules, CA), með því að nota 96-brunn Bio-Rad CFX96 RT–PCR kerfi með C1000 Thermal Cycler (Bio-Rad, Hercules, CA) samkvæmt leiðbeiningum framleiðenda. Ct gildi var fengið úr hverri mögnunarferil með því að nota CFX96 greiningarhugbúnað frá framleiðanda. Hlutfallsleg mRNA tjáning var ákvörðuð með 2 - ΔΔCt aðferðinni [17]. 18S genið var notað í staðsetningartilgangi. Grunnraðirnar sem notaðar voru við magngreiningu mRNA voru: CPT1A (FW: TGCTTTACAGGCGCAAACTG, RV: TGGAATCGTGGA TCCCAAA), ACTA (FW: TTCAATGTCCCAGCCATGTA, RV: GAAGGAA- TAGCCACGCTCAG), COL1A1 (FACCTTTGGGTGGA: CGATTTGGTGGTW: CGATTTGGTGGA, GGGGAATG, húsbíll: CCAATGCCACGGCCATAGCAGTAGC), PGC1A (FW: TGCCCTGGATTGTTGACATGA, húsbíll: TTTGTCAGGCTGGGGGGTAGG), TF AM (FW: CATCTGTCTTGGCAAGTTGTCC, húsbíll: CCACTCCGCCCCCTA- TAAGCATCTCTA- TAAGCATCTATCTGGA: GCCATCATCTGGA, AGGTCATCTCTGGA, AGGTCATCTCTGGA). Brotbreytingar voru staðlaðar að gildum viðmiðunarástands.
Magngreining á tjáningu miRNA. Mæling á tjáningu miRNAs var framkvæmd með því að nota miRCURY Locked Nucleic Acid (LNA) miRCURY LNA RT Kit (Exiqon, Feedback, Danmörk). Eftir RT var cDNA sniðmátið magnað upp með því að nota microRNA-sértæka LNA grunna fyrir þroskað miR150-5p eða miR-495-3p (Exiqon, Feedback, Danmörk). qRT–PCR var framkvæmt í 96-brunn Bio-Rad CFX96 rauntíma PCR kerfi með C1000 Thermal Cycler með iQ™ SYBR Green Supermix (Bio-Rad, Hercules, CA) samkvæmt leiðbeiningum framleiðenda. . Ct gildi fyrir þrítekna brunna var fengið úr hverri mögnunarferil með því að nota CFX Manager Bio-Rad hugbúnaðinn (Bio-Rad, Hercules, CA). Ct gildi voru staðlað í innræna samanburðar 5S rRNA. Plasma miRNA gildi voru staðlað í miR-103a-5bls. Hlutfallsleg miRNA tjáning var ákvörðuð með 2 - ΔΔCt aðferðinni [17]. Brotbreytingar voru staðlaðar að gildum viðmiðunarástands.
Múslíkön af bandvefsmyndun í nýrum. Mýs voru geymdar í dýraaðstöðunni sem er laus við sérstakar sýkla (SPF) hjá CBMSO í samræmi við reglugerðir ESB um allar aðgerðir. Dýr voru meðhöndluð í samræmi við leiðbeiningar um umhirðu og notkun tilraunadýra sem er að finna í tilskipun Evrópuþingsins 2010/63/ESB. Samþykki var veitt af staðbundinni siðaskoðunarnefnd Centro de Biología Molecular "Severo Ochoa" í Madríd, siðanefndinni hjá CSIC og eftirlitseiningunni um dýratilraunaaðferðir frá Comunidad de Madrid.
Einhliða þvagrásarteppa (UUO): UUO skurðaðgerð var framkvæmd eins og áður hefur verið lýst [18]. Í stuttu máli voru mýs svæfðar með ísóflurani (3-5 prósent fyrir framköllun og 1-3 prósent til viðhalds) og skipt í tvo tilraunahópa: UUO hópinn og sýndaraðgerðahópinn. Í UUO hópnum voru mýs rakaðar vinstra megin á kviðnum, lóðréttur skurður var gerður í gegnum húðina með skurðhnífi og húðin dregin til baka. Annar skurður var gerður í gegnum kviðarholið til að afhjúpa nýrun. Vinstra þvagleggurinn var bundinn tvisvar 15 mm fyrir neðan nýrnamjaðmagrind með skurðaðgerðarsilki og þvagleggurinn var síðan skorinn á milli bandanna tveggja. Síðan var tengt nýra sett varlega aftur í rétta líffærafræðilega stöðu og dauðhreinsuðu saltvatni bætt við til að bæta á vökvatapið. Skurðarnir voru saumaðir og mýsnar settar í búr fyrir sig. Sýndaraðgerðin var framkvæmd á svipaðan hátt en án samtengingar þvagrásar. Búprenorfín var notað sem verkjalyf. Fyrsti skammtur var gefinn 30 mínútum fyrir aðgerð og síðan á 12 klst. fresti í 72 klst., í 0,05 mg/kg skammti undir húð. Í þessu líkani minnkar nýrnablóðflæði og gaukulsíunarhraði marktækt innan 24 klst. og millivefsbólga (hámarki eftir 2-3 daga), píplavíkkun, píplurýrnun og bandvefsmyndun eru augljós eftir 7 daga. Stíflað nýrað nær hámarks vanstarfsemi um það bil 2 vikum eftir aðgerðina. Músum var fórnað með ofskömmtun CO2 og viðmiðunar- og nýrna- og blóðsýni sem voru tekin voru tekin eftir gegnflæði með PBS 3, 5, 7, 10 og 15 dögum eftir UUO.
Nýrnakvilli af völdum fólínsýru (FAN): Í þessu líkani var bandvefsmyndun nýrna framkölluð með inndælingu í kviðarhol (ip) með 25 0 mg af fólínsýru (Sigma-Aldrich, St. Louis, MO) á hvert kg líkamsþyngdar uppleyst í 0.3 M natríumbíkarbónat (fartæki) eins og áður hefur verið lýst [19]. Viðmiðunardýr fengu 0,3 ml af burðarefni (ip). Músum var fórnað með ofskömmtun CO2 og nýru og blóðsýni voru tekin eftir gegnflæði með PBS eftir 15 daga FA gjöf.
microRNA prófílgreiningu. Til að bera kennsl á tiltekin miRNA sem stjórna trefjafræðilegri niðurstöðu var sérsniðin miRCURY LNA míkróRNA fylki (Exiqon, Feedback, Danmörk) valin sem vettvangur fyrir míkróRNA prófílgreiningu. Þessi vettvangur samanstóð af alls 175 einstökum greiningum sem eru sértækar fyrir miRNA músa sem eru til staðar í Sanger miRBase v22.1 (http://microrn a.sanger.ac. Bretlandi). Fyrir hvert microRNA var ríkjandi strengur valinn til greiningar. MiR val var byggt á spáð markgenum sem tengdust bandvefsmyndun í nýrum, umbrotum hvatbera, redoxferlum og dægursveiflu. Þessi greining var gerð með lífupplýsingaverkfærum fyrir raðbundið miRNA markspá, microcosm [20] (www.Ebi.ac. UK/Enright-SRV/microcosm), Targetscan 4.1 [21] (www.targetscan.org /vert{ {9}}/) Pictar I [22] (www.pictar.mdc-berlin.de), miRWalk [23] (www.mirwalk.umm.uni-heidelberg.de/) og miRanda [24] (www.mic rorna.org/microrna/). Eftir RNA-útdrátt úr 7 daga-UUO nýrnasýnum var miRNA-hlutinn sem var til staðar í 20 ng af heildar-RNA undirritaður í öfugri umritun með því að nota miRCURY LNA RT Kit (Exiqon, Feedback, Danmörk) samkvæmt leiðbeiningum framleiðanda. CDNA sem mynduðust voru greind með miRCURY miRNA PCR spjöldum í Roche LightCycler 480 rauntíma PCR kerfi með því að nota miRCURY LNA SYBR Green PCR Master Mix (Exiqon, Feedback, Danmörk). Hvert sýni var greint í tvíriti. Þessi aðferð var framkvæmd í Genomics Facility Fundacion Parque Científico de Madrid (Madrid, Spáni). LC480 hugbúnaðurinn var notaður til að fá Cq gildi (Cq) fyrir hvert miRNA. Delta Ct (ΔCt) gildið var reiknað út með því að staðla Ct gildin við innræna heimilishaldið snRNAU6. Hitakortið var búið til með rauntíma PCR gögnum kynnt sem ΔCt. Stigveldisþyrping var byggð í samræmi við ΔCt gildi. Delta Ct (ΔΔCt) gildið var reiknað út með því að draga ΔCt í viðmiðunarsýnishópnum (viðmiðunarnýra) frá ΔCt hvers stíflaðs nýrnasýnis. Hlutfallsleg magngreining (RQ) eða faltbreyting hvers miRNA var mynduð með 2 - ΔΔCt aðferðinni [17]. Mismunandi tjáð miRNAs voru auðkennd með limma prófinu. Til að taka tillit til margra tilgátanna sem prófaðar voru, voru P-gildi leiðrétt (adj.) með því að nota Benjamini-Hochberg rangar uppgötvunarhlutfall (FDR) leiðréttingu [25]. Niðurstöður voru teknar upp á línuriti fyrir eldfjall.
miRNA greining í blóðvökva frá sjúklingum með langvinnan nýrnasjúkdóm. Magn valinna miRNAs var greint í plasmasýnum úr hópi 100 sjúklinga með langvinna lungnateppu, sem er útskýrt hér að neðan. Blóðblóði í útlægum bláæðum var safnað í EDTA úðahúðuðum ryksugum (BD, Franklin Lakes, NJ). Til að fá plasma var blóð skilið í skilvindu við 400 g í 20 mínútur, flotið var flutt í nýtt rör og skilið í skilvindu við 800 g í 20 mínútur. Plasma var safnað og geymt frosið í deilum við -80 ◦ C. Plasma miRNA var dregið úr blóði með því að nota miRCURYTM RNA Isolation Kit—Biofluids og UniSp2 Spike-in RNA (Exiqon, Vedbaeck, Danmörk). Greiningar á miR-150-gildum í þessum sýnum voru framkvæmdar eins og lýst er í kaflanum um magngreiningu á tjáningu miRNA. Mælingar á súrefnisnotkunarhraða. Fitusýruoxunartengd súrefnisneysluhraði (OCR) (bundinn við oxandi fosfórýleringu) og utanfrumu súrnunarhraði (ECAR) (tengt laktatframleiðslu og glýkólýsu) voru rannsökuð með Seahorse Bioscience efnaskiptagreiningartækinu samkvæmt leiðbeiningum framleiðanda [26]. HKC-8 frumum var sáð í p60 plötu og míkróRNA transfection var framkvæmd eins og lýst er hér að ofan þegar þær náðu 70 prósenta samruna 48 klst. síðar, HKC-8 frumur voru meðhöndlaðar með 10 ng/ml TGF{{ 18}} í 48 klst. Síðan voru frumur sáð með 2 × 104 frumum í hverri brunn í Seahorse Bioscience XFe24 frumuræktar örplötu (Seahorse Bioscience, North Billerica, MA). Eftir viðloðun frumna var vaxtarmiðlinum skipt út fyrir hvarfefnistakmarkaðan miðil, Dulbecco's Modified Eagle Medium (DMEM) bætt við 0,5 mM glúkósa og 1 mM glútamat. Klukkutíma fyrir mælinguna voru frumur ræktaðar með Krebs-Henseleit Buffer (KHB) prófunarmiðli ásamt 0,2 prósent karnitíni við 37 ◦ C án CO2. Fimmtán mínútum fyrir greiningu var CPT1 hemlinum Etomoxir (Eto) (Sigma-Aldrich, St. Louis, MO) 400 μM bætt við samsvarandi brunna og frumur ræktaðar við 37 ◦ C án CO2. Að lokum, rétt fyrir greiningu, var BSA eða 200 μM Palmitate-BSA FAO undirlag (Agilent Technology, Santa Clara, CA, Bandaríkjunum) bætt við. Strax var XF Cell Mito streituprófið framkvæmt í Seahorse XFe24 orkugreiningartæki með því að bæta í röð nokkrum mótum hvatberavirkni. Í fyrsta lagi var ATP synthasa hemill oligomycin (Sigma-Aldrich, St. Louis, MO) (1 μM) notaður í kjölfar grunnmælinga. Þetta dregur úr rafeindaflæði í gegnum ETC, sem leiðir til minnkunar á hvatberaöndun. Því næst var aftengingarefninu sýaníð 4-(tríflúormetoxý) fenýlhýdrasóni (FCCP) (SigmaAldrich, St. Louis, MO) (3 μM), sem hrynur róteindahallann og truflar hvatberahimnugetu bætt við. Fyrir vikið er rafeindaflæði í gegnum ETC óhindrað og súrefnisnotkun flókins IV nær hámarki. Þriðja og síðasta inndælingin er blanda af flóknum III og I hemlum and-mycin/rotenone (Sigma-Aldrich, St. Louis, MO) (1 μM). Þessi samsetning lokar á hvatberaöndun og gerir útreikninga á öndun sem ekki er hvatbera knúin áfram af ferlum utan hvatberanna. Undirlag/hemlar voru útbúin í sama miðli og tilraunin var gerð í og var sprautað sjálfkrafa úr hvarfefnisgöngunum á þeim tímum sem tilgreindir eru. Mælingar voru skráðar í 3-mín. tímabil (á samtals 2 klst. tímabil) og gildi voru staðlað fyrir heildarpróteininnihald. Prótein var dregið úr brunnum með 0,1 prósent NP-40-PBS lausn og magnmælt með BCA próteingreiningu (Thermo Scientific, Rockford, IL). Fjórar holur voru notaðar fyrir hvern tilraunahóp. Sjóhesturinn XFp Cell Mito Stress Test var notað til að ákvarða helstu breytur starfsemi hvatbera: grunnhvatberaöndun, ATP-tengd öndun, róteindaleki (ekki-- ATP-tengd súrefnisnotkun), hámarksöndun, öndun sem ekki er hvatbera. , og vara öndunargetu, eins og áður hefur verið lýst [27].
Lúsiferasa próf. Til að einkenna miRNA-150 og miRNA-495 umsækjendur bindiseta í CPT1A 3'-UTR í mönnum, luciferase reporter próf sem inniheldur CPT1A 3'-UTR (SwitchGear Genomics, Carlsbad, CA, vara ID S814347) var notað. Staðstýrðar stökkbreytingar á fræsvæðum spáðra miR-150 og miR-495 staða innan 3′ - UTR voru mynduð með því að nota Multisite-QuikChange stýrða stökkbreytingarsett (Stratagene, La Jolla, CA) skv. við samskiptareglur framleiðanda. The primer sequences used were for miR-495 PM1 (FW:GCATCATCCAAGCAGGGTAAACTTTTGTTCTAGAAAAA- GAAAAATGTGTTATTCATTGGTGTCCC, RV: GGGACACCAACTTGAA- TAACACATTTTTCTTTTTCTAGAA- CAAAAGTTTACCCTGCTTGGATGATGC) and PM3 (FW: TGTCTTAACGCAGCCATGGTTTGAATCTA- GAATCTTGGGCTGACCGGTGC, RV: GCACCGGTCAGCCCAAGATTCTA- GATTCAAACCATGGCTGCGTTAAGACA) and for miR{{24} } PM2 (FW: CTCATGCGTGTAATCCCAGCACTTCTAGAGGCCAAGGCGGGCGG, RV: CCGCCCGCCTTGGCCTCTAGAAGTGCTGGGATTACACGCATGAG), Öll smíði voru raðgreind fyrir notkun til að staðfesta að þau séu rétt uppbygging. HKC-8 frumum var sáð í ap24-brunnsplötu og voru samsmitaðar tímabundið með 200 ng pLightSwitch_CPT1A_3′-UTR (ósnortinn eða stökkbreyttur byggingu) og 4 ng pGL3-Promoter (eldflugulúsiferasa undir stjórn SV40-hvatarans) (Promega Corporation, Madison, WI, USA) fréttaplasmíð og 40 nM af annaðhvort mirVana™ miRNA líki eftir miR-150, miR -495 eða mirVana™ miRNA líkja eftir neikvæðri stjórn (Ambion fyrirtæki, Bandaríkjunum) með því að nota lipofectamine 2000 (Invitrogen, Carlsbad, CA) þegar þau náðu 70 prósenta samruna eins og lýst er hér að ofan. Fjórar holur voru notaðar fyrir hvern tilraunahóp. Lúsiferasagreiningar voru framkvæmdar 24 klukkustundum síðar með því að nota Dual-Luciferase fréttaritarakerfið (Promega, Madison, WI). Vanillu- og eldflugulúsiferasamerkin voru greind með Glomax fjölskynjunarkerfi (Promega Corporation, Madison, WI, Bandaríkjunum). Virkni renilla luciferasa var staðlað með eldflugu luciferasa virkni.

Hvatberahimnugeta (MMP). Breytingar á MMP voru ákvarðaðar sem munur á tetrametýlródamínmetýlester (TMRM) flúrljómun (Invitrogen, Carlsbad, CA, Bandaríkjunum). Það safnast fyrir í neikvætt hlaðnum skautuðum hvatberum og flúrljómar í appelsínugult. Þegar möguleiki hvatberahimnu hrynur í frumum sem eru undir áhrifum efnaskipta eða frumum sem eru stressaðar af efnaskiptum, dreifist TMRM hvarfefnið um umfrymis frumunnar og flúrljómunarstig lækkar verulega. HKC-8 frumur voru ræktaðar og transsmitaðar eins og lýst er í frumuræktunar- og transfemingaraðferðinni. Næst var vaxtarmiðli skipt út fyrir fenólrauðalausa Hank's Balanced Salt Solution (HBSS) með 10 mM Hepes. Meðferð með oligomycini (5 μM) og FCCP (4 μM) í 5 mínútur voru notuð sem jákvæð og neikvæð viðmiðunarskilyrði. Næst voru frumur litaðar með 250 nM TMRM í 30 mínútur við 37 ◦ C. Frumur voru safnaðar með trypsíni, skildar í skilvindu (3000 snúninga á mínútu, 5 mín.) og kúlunni var dreift aftur í 200 μL HBSS með 1 prósenti Bovine Serum Albumin (BSA) og 5 mM etýlendíamíntetraediksýra (EDTA). Flúrljómunarstyrkur var mældur með frumflæðismælingu með því að nota losunarbylgjulengd 570 nm fyrir TMRM (FL2) [28] í BD FacsCantoTM II kerfi (BD Bioscience, San Jos, CA) og greind með FlowJo 10.2 hugbúnaðinum (FlowJo, LLC, Ashland) , EÐA). Fyrir hvert tilraunaástand voru að minnsta kosti 20.000 eintök greind í þrígangi.
Framleiðsla hvatbera ofuroxíðs róttækra anjóna. Mat á framleiðslu súperoxíðradikala anjóna var framkvæmt með því að nota Mito-SOX™ Red hvatbera súperoxíð radical anjónavísir (Invitrogen, Carlsbad, CA, Bandaríkjunum), mjög sértækt flúorógen litarefni fyrir hvatbera súperoxíð radical anjón í lifandi frumum, samkvæmt framleiðanda leiðbeiningar. HKC-8 frumur voru ræktaðar og transsmitaðar eins og lýst er í frumuræktunar- og transfemingaraðferðinni. Næst var vaxtarmiðli skipt út fyrir fenólrauðalausa Hank's Balanced Salt Solution (HBSS) með 10 mM Hepes. Meðferð með andmycin A (150 μM) og karbónýlsýaníði m-klórfenýlhýdrasóni (CCCP) (50 μM) í 5 mínútur voru notuð sem jákvæð og neikvæð viðmiðunarskilyrði. Næst voru frumur litaðar með 5 μM MitoSOX™ Red í 30 mínútur við 37 ◦ C. Frumur voru safnað eins og lýst er í hvatberahimnukaflanum. Flúrljómunarstyrkur var mældur með frumflæðismælingu með því að nota losunarbylgjulengd 580 nm fyrir MitoSOX™ Red (FL2) í BD FacsCantoTM II kerfi (BD Bioscience, San Jos, CA) og greind með FlowJo 10.2 hugbúnaðinum (FlowJo, LLC, Ashland, EÐA). Fyrir hvert tilraunaástand voru a.m.k. 20,000 stakir greindir í þrígangi.
Hvatbera merking. Mat á innihaldi hvatbera var framkvæmt með því að nota MitoTracker™ græna FM (Invitrogen, Carlsbad, CA, USA), sem dreifist óvirkt yfir plasmahimnuna og safnast fyrir í virkum hvatberum óháð hvatberahimnugetu, samkvæmt leiðbeiningum framleiðanda. HKC-8 frumur voru ræktaðar og transsmitaðar eins og lýst er í frumuræktunar- og transfemingaraðferðinni. Næst var vaxtarmiðli skipt út fyrir fenólrauðalausa Hank's Balanced Salt Solution (HBSS) með 10 mM Hepes. Frumur voru litaðar með 150 nM með MitoTracker™ grænum FM í 30 mínútur við 37 ◦ C. Til greiningar á frumuflæðismælingum voru frumur safnað eins og lýst er í hluta hvatberahimnugetu. Flúrljómunarstyrkur var mældur með losunarbylgjulengd 516 nm fyrir MitoTracker™ græna FM (FL1) í BD FacsCantoTM II kerfi (BD Bioscience, San Jos, CA) og greind með FlowJo 10.2 hugbúnaðinum (FlowJo, LLC) , Ashland, OR). Fyrir hvert tilraunaástand voru a.m.k. 20,000 stakir greindir í þrígangi. Fyrir flúrljómun mynd- aging, voru kjarnar einnig litaðir með DAPI (Sigma, St. Louis, MO) í 5 mínútur við RT. Lifandi frumur voru sýndar með öfugum Zeiss LSM 710 confocal smásjá með frumu sem sést, 63X/1.2 Water C-Apo- chromat Corr UV-VIS-IR M27 hlutlægi og greindar með Zeiss Zen2010B sp1 hugbúnaðinum (Zeiss, Oberkochen, Þýskalandi) .
Ákvörðun hvatbera eintaksnúmers. Erfðafræðilegt DNA var dregið úr HKC-8 frumum með því að nota DNeasy Blood & Tissue Kit (Qiagen, Valencia, CA) samkvæmt leiðbeiningum framleiðanda. Mikið hvatbera var ákvarðað með DNA afritanúmeragreiningarsetti fyrir hvatbera úr mönnum (Detroit R&D, Detroit, MI). Hlutfallslegt mtDNA eintaksnúmer var gefið upp sem hlutfall mtDNA og kjarna DNA.
Sýni úr mönnum með langvinnan nýrnasjúkdóm. Hópur 100 sjúklinga með langvinnan nýrnasjúkdóm (stig 3-4) frá Hospital Principe de Asturias var valinn til greiningar á plasmaþéttni miRNA. Það innihélt tvo mismunandi undirhópa sem flokkaðir voru eftir þróun nýrnastarfsemi þeirra á grundvelli GFR MDRD vísis [29] á 24 mánaða tímabili: 50 sjúklingar sýndu minna en 10 prósent afnýruskert starfsemi á meðan hinir höfðu upplifað að minnsta kosti 40 prósenta skerðingu á nýrnastarfsemi eða byrjaðnýruuppbótarmeðferð (skilun). Við töluðum einnig magn bandvefs ínýruvefjasýni úr öðrum hópi 26 sjúklinga með truflun á ígræðslu í kjölfariðnýruígræðslu frá Ramn y Cajal sjúkrahúsinu. Öll vefjasýni voru metin samkvæmt Banff 2007 viðmiðunum [30].
Tölfræðigreining. Gögnin voru greind með prófum sem ekki eru parametrísk nema þar sem tilgreint er. Munurinn á óháðu hópunum tveimur var skoðaður með Mann-Whitney prófinu en fleiri en tveir hópar voru bornir saman við Kruskall-Wallis prófið. P-gildi 0.05 eða minna var talið tölfræðilega marktækt (*/#: P < 0.05,="" **/##:="" p="">< 0.01,="" ***/###:="" p="">< 0,001).="" gögnin="" voru="" greind="" með="" graphpad="" prism="" 6.0="" (graphpad="" software,="" la="" jolla,="" ca).="" gögn="" eru="" skráð="" sem="" meðaltal="" ±="" staðalvillu="" af="" meðaltal="">
3. Úrslit
miRNA tjáningargögn í trefjaefni af völdum UUOnýru. Til að ráða framlag miRNAs til efnaskiptastjórnunar ánýrutrefjamyndun, 7 daga UUO líkanið var gert í WT músum. RNA var einangrað úr samanburði og trefjaefninýrusýni og miRNA tjáningarsniðið var greint í sérsniðnu microRNA fylki. Val á miRNA var byggt á hugsanlegri miðun þeirra á lykilensím sem taka þátt í umbrotum hvatbera, enduroxunarferlum og dægursveiflu eftir "in silico" greiningu (nánari upplýsingar í kaflanum um aðferðir). Hitakortið leiddi í ljós skýrt greinilegt tjáningarmynstur í sumum miRNA þegar borið var saman trefja- og eftirlitnýrusýni (mynd 1A). Eldfjallasamsærisgreiningin sýndi að 73 af 175 miRNA voru tjáð á mismunandi hátt, 17 upp- og 56 niður-stýrð, í trefjabundnum nýrnasýnum samanborið við viðmiðunarsýnin (mynd 1B, viðbótartafla1). Meðal þeirra voru valin sérstök miRNA sem gætu stjórnað trefjaáhrifum í nýrum með efnaskiptaleiðum. Í þeim tilgangi, í kísilgreiningu á 3'UTR (óþýtt svæði) sérstakra gena sem taka þátt í efnaskipta- og hvatberavirkni, var CPT1A, TFAM, PGC1A framkvæmd með þremur sjálfstæðum spáverkfærum (Targetscan, miRWalk og miRanda). Valviðmið innihéldu einnig tjáningarstig nýrna, nýnæmi markmiða, þekking á efnaskiptaleiðinni og líffræðilega þýðingu. Tenging við meinafræði manna, tjáningarstig nýrnavefs, hlutverk þeirra í umbrotum hvatbera og hugsanleg miðun þeirra á fitusýruflutningsensímið CPT1A hvatti okkur til að einbeita okkur að þremur miRNA, miR-150-5p, miR-495-3p og miR-33-5p, sem frambjóðendur sem geta stjórnað efnaskiptabreytingum sem tengjast trefjamyndun í nýrum (mynd 1C). Athygli vekur að CPT1A 3′-UTR inniheldur eina fræsíðu fyrir miR-150 og tvær fræsíður fyrir miR-495. Við sáum að miR-150 og miR-495 minnkuðu virkni luciferase reporter prófunar sem innihélt CPT1A 3'-UTR um ~15 prósent og 25 prósent, í sömu röð. Þessi lækkun var algjörlega afnumin þegar um var að ræða punktstökkbreytingar (PM) í 3′-UTR CPT1A fyrir miR-150 bindisetið (PM2) og að hluta til fjarverandi á báðum miR-495 bindistöðum (PM1) og PM3) (aukamynd 1A og B). Þessi gögn gefa til kynna bein samskipti CPT1A við miR-150 og miR-495. MiR-33-5p hefur verið viðfangsefni sérstakrar rannsóknar [15]. MiR-150-5p og miR-495-3p voru uppstýrð í trefjabundnum nýrnasýnum samanborið við viðmiðunarsýnin, með 3,69 falda breytingu (P-gildi: 0.012 ) og 1,95 (P-gildi: 0,012), í sömu röð.
MiR-150 og miR-495 auka TGF-svörun í mönnumnýrupípulaga þekjufrumur. Megindleg öfug umritun–pólýmerasa keðjuverkun (qRT–PCR) var framkvæmd til að staðfesta breytingu á miR-150-5p og miR-495-3p tjáningu sem höfðu verið auðkennd með miRNA tjáningarsniði í UUOnýrusýni (mynd 2A og B). Að auki var hreyfihvörf miR-150-5p og miR- 495-3p tjáningar í nýrum 3, 5, 7, 10 og 15 dögum eftir UUO aðferð greind með qRT-PCR. Tjáning þessara miRNAs var verulega aukin með því að 2-falt 5 dögum eftir UUO og hélst hækkuð 15 dögum eftir UUO (mynd 2C og D). Tjáningarstig þessara miRNA var einnig metið í fólínsýru nýrnakvilla (FAN) líkaninu. Við fundum 4- og 2-falt uppstjórnun á miR-495-3p og miR-150-5p, í sömu röð, í trefjafrumumnýrusýni úr FAN líkaninu (mynd 2E). TGF- 1, einn af aðalstjórnendum trefjamyndunar, olli einnig tjáningu miR-150 og miR-495 í HKC-8 frumum meira en 2-falt og {{ 6}} falt, hver um sig, eftir 48 klst, sem styður hugsanlegt hlutverk þessara miRNA í TGF-merkjatengdum atburðum (mynd 3A og B). Til að meta hvort miR-150 og miR-495 hafi átt þátt í umbreytingu á pípulaga þekjufrumum með TGF- 1, var frumulínan HKC-8 úr mönnum flutt með miR -150-5p eða miR-495-3p og meðhöndluð með TGF- 1 fyrir mismunandi tíma. Aukning miR-150-5p og miR-495-3p styrks jók marktækt TGF- 1-framkallaða mRNA stigs tjáningu á bandvefstengdu merkjunum Acta2, Col1 1 og Fn1 ( mynd 3C og D). Á sama hátt minnkaði oftjáning miR-150-5p eða miR-495-3p CPT1A verulega og jók -SMA próteinmagnið (mynd 3E og F). Þessi gögn benda til þess að þessi miRNA geti tekið þátt í meingerðnýrubandvefsmyndun með því að stuðla að TGF- 1-háðri aðgreiningu þekjulaga pípulaga frumna, sem og með því að skerða tjáningu mikilvægs ensíms sem tekur þátt í FAO.
MiR-150 og miR-495 örva líforkubreytingar í hvatberum og draga úr tjáningu gena sem taka þátt í mikilvægri starfsemi hvatbera. Til að öðlast innsýn í efnaskiptaafleiðingar af völdum gjafar miR-150-5p eða miR-495-3p rannsökuðum við líforkusnið mannanýrupípulaga þekjufrumur.
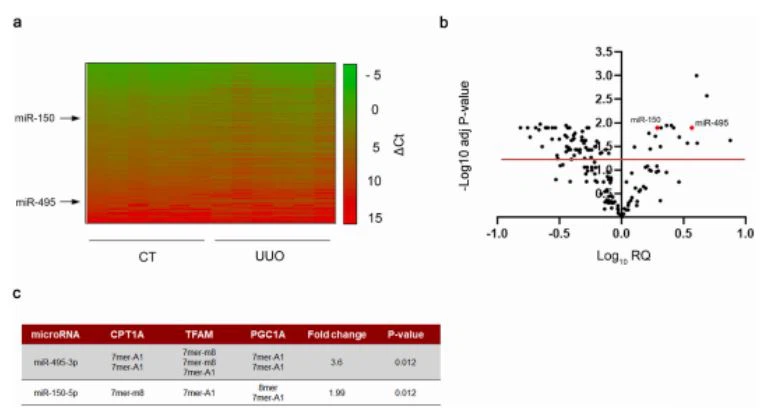
Mynd 1. miRNA tjáningu gögn í UUO-völdum bandvefsmyndun. (A) Hitakort sem sýnir hlutfallslega miRNA tjáningu gagnhliða og hindrunarnýruaf C57/BL6-J músum sem fóru í UUO málsmeðferð í 7 daga (n=6). Kvarðastikan er á bilinu frá grænu til rautt (há til lág tjáning) og tölur tákna ΔCt gildi. Vinstra megin eru sýnd miRNA sem valin voru til rannsóknar. (B) Eldfjallasögugreining á UUO-stýrðum miRNAs. Log10 hlutfallsleg magngreining (RQ) og neikvæð ( − ) log10 leiðrétt (adj.) P-gildi eru teiknuð á x- og y-ás, í sömu röð. Hvert miRNA er táknað með punkti. 73 af 175 miRNA sýndu breytta tjáningu í trefjasýnum (adj. P-gildi Stærra en eða jafnt og 0,05). Valin miRNA til frekari greiningar eru auðkennd. (C) miR-150-5p og miR-495-3p voru valin á grundvelli krafts þeirra fyrir in silico miðun á genunum CPT1A, TFAM og PGC1A. Fyrir hvert valið míkróRNA, varðveitt fræmarksstaði í 3'UTR þessara gena, eru skiptingar þeirra og mikilvægi (adj. P-gildi) tilgreindar.

Mynd 2. Tjáningarstig miR-150-5p og miR-495-5p innýrufrá UUO og FAN módelunum. (A, B) qRT-PCR greining á miR-150-5p (A) og miR-495- 3p (B) tjáningu ínýruúr músum 7 dögum eftir UUO í sýnum sem áður voru greind með microRNA fylkinu. (C–E) qRT-PCR greining á miR-150-5p og miR-495-3p tjáningu eftir FAN líkaninu (C) og 3, 5, 7, 10 og 15 dögum eftir UUO fyrir miR-150-5p (D) og miR{{10}}p (E). Súlurit tákna meðaltal tjáningarstigs brotabreytinga ± sem frá 6 (A, B, E) og 3 (C og D) músum í hverjum hópi. *P < 0.05,="" **p="">< 0.01,="" ***p="">< 0.001="" miðað="" við="" samsvarandi="" viðmiðunarskilyrði;="" #p="">< 0,05,="" ##p="">< 0,01="" miðað="" við="">nýruúr músum með sömu tilraunameðferð.
TGF- 1 var notað sem fyrirmynd cýtókíns sem tekur þátt í breytingum sem tengjast trefjavefjum. Til að ákvarða líforkustöðu þessara frumna var FAO-tengd súrefnisneysluhraði (OCR) og utanfrumu súrnunarhraði (ECAR) HKC-8 frumna mæld við raðmeðferð með efnasamböndum sem stilla virkni hvatbera í nærveru palmitats. , með því að nota Seahorse XF24 Extracellular Flux Analyzer (nánari upplýsingar í kaflanum Aðferðir). Eftir 48 klst. með TGF- 1 sýndu HKC-8 frumur í viðurvist miR-150-5p stöðuga lækkun á grunni, OCR tengdri ATP-myndun, ATP-tengdri öndun og hámarksöndun, sem tengist FCCP-viðkvæmum OCR (mynd 4A). Skerðingin í OXPHOS endurspeglaðist af lækkun á ATP innihaldi í HKC-8 frumum sem oftjáðu miR-150-5p (mynd 4C). Við sáum ekki að þessi miRNA valdi breytileika í ECAR (gögn ekki sýnd). Í samræmi við þetta, mRNA tjáningarstig hvatbera þeirra
skyld markgen CPT1A, PGC1 og hvatbera umritunarþáttur A (TFAM), minnkuðu um helming í frumum sem voru meðhöndlaðar með miR-150 líkingu í samanburði við miRNA líkja eftir NC-meðhöndluðum frumum (mynd 4E). Rannsóknir með sömu tilraunaaðferð með miR-495-3p gáfu svipaðar niðurstöður (mynd 4B, D, F). Hins vegar var hvatberamassi, ákvarðaður af mtDNA afritafjölda og litun hvatbera með MitoTrackerTM grænum FM, ekki marktækt mótaður af miRNA-150 og miRNA- 495 bæði við grunnskilyrði og við TGF-meðferð. Lækkandi tilhneiging í þessari breytu sást í grunninn (viðbótarmynd. 2A, B, C). Á heildina litið styðja þessi gögn að miR-150 og miR-495 stuðla að a
pro-fibrotic virkni í pípulaga þekjufrumum vegna skerðingar á starfsemi hvatbera.
MiR-150 og miR-495 breyta ekki hvatbera yfirhimnugetu (ΔѰm) og hvatbera ofuroxíðradikal


Mynd 3. MiR-150 og miR-495 auka TGF- 1-háð pro-fibrotic svörun í mönnumnýrupípulaga þekjufrumur. (A, B) RT–PCR greining á miR{{0}}p (A) og miR-495-3p (B) tjáningu í HKC-8 frumum sem voru meðhöndlaðar með 1{{24 }} ng/ml TGF- 1 fyrir tilgreinda tíma. (C, D) mRNA magn af alfa-sléttum vöðvaaktíni (-SMA), alfa 1 gerð-1 kollageni (Col1 1), fíbrónektíni (FN) úr frumum sem hafa verið transsýktar með miR-NC og líkja eftir miR -150-5p (C) eða miR-495-3p (D) voru ákvörðuð með qRT-PCR með því að nota Sybr green. Frumur voru meðhöndlaðar með TGF- 1 (10 ng/ml) eftir oftjáningu miRNA þar sem það var gefið til kynna (sjá einnig kafla um aðferðir). (E, F) Ónæmisblettir sem sýna próteinmagn CPT1A og -SMA í frumum sem hafa verið transsmitaðar með miR-NC og líkja eftir miR-150-5p (E) eða miR{{20}}p (F) fyrir tilgreindum tímapunktum. GAPDH var notað í eðlilegum tilgangi. Súlurit (hægri spjaldið) tákna meðaltal faltbreytingatjáningar ± sem úr 3 sjálfstæðum tilraunum. *P < {{30}}.05,="" **p="">< 0.01,="" ***p="">< 0.001="" miðað="" við="" samsvarandi="" viðmiðunarskilyrði;="" #p="">< 0,05,="" ##p="">< 0,01,="" ###p="">< 0,001="" samanborið="" við="" frumur="" meðhöndlaðar="" með="" mir-nc="" með="" sama="">


Mynd 4. MiR-150 og miR-495 auka TGF 1-framkallaða FAO bælingu í HKC-8 frumum. (A, B) Súrefnisneysluhlutfall (OCR) HKC-8 frumna sem eru sýktar með
40 nM miR-NC og líkja eftir miR-150-5p (A) eða miR-495-3p (B) og verða fyrir 10 ng/ml TGF{{5} } eftir oftjáningu miRNA (sjá einnig kafla um aðferðir). Súlurit (hægri spjald) sýna hraða OCR sem tengist grunn-, róteindaleka, ATP-tengdri, hámarks- og varagetu og öndunarstöðu utan hvatbera. Gögn eru táknuð eftir normalization með magni próteina. (C, E) ATP-magn í HKC-8 frumum sem eru umbreyttar með miR-NC og líkja eftir miR-150-5p (C) eða miR-495-3p (E). (D, F) mRNA-gildi CPT1A, PGC1A og TFAM í HKC-8 frumum sem voru transsmitaðar með miR-NC og líkja eftir miR-150-5p (D) eða miR-495-3p (F) voru ákvarðað með qRT-PCR með því að nota Sybr grænn. Súlurit sýna meðaltal ± sem 4 óháðra tilrauna. *P < 0.05,="" **p="">< 0.01,="" ***p="">< 0,001="" miðað="" við="" samsvarandi="" eftirlitsskilyrði;="" #p="">< 0,05,="" ##p="">< 0,01,="" ###p="">< 0,001="" samanborið="" við="" frumur="" meðhöndlaðar="" með="" mir-nc="" með="" sama="">
anjónaframleiðsla. Hvatberahimnugeta (ΔΨm) sem myndast af róteindadælum (samstæður I, III og IV) er nauðsynlegur þáttur í ferli orkugeymslu við oxandi fosfórun. Aukið ΔѰm getur leitt til truflunar á hvatbera redox truflun, á meðan lækkun þess veldur minnkun á ATP framleiðslu, sem skerðir lífvænleika frumna [254]. Superoxide radical anion (O2•− ) er sindurefni sem getur myndast í hvatberum sem afleiðing af rafeindaleka sem getur átt sér stað innan nokkurra þrepa ETC. Myndun O2•− innan hvatbera fylkisins veltur einnig á NADH/NAD plús og CoQH2/CoQ hlutföllum og staðbundnum O2 styrk [255]. Offramleiðsla þess getur leitt til taps á hvatbera redox homeostasis með mismunandi aðferðum, ástand sem hefur verið tengt mörgum meinafræðilegum sjúkdómum þar á meðal AKI og CKD [201]. ΔѰm var skoðað með TMRM litarefninu og súperoxíð róttæka anjónaframleiðslu með MitoSOX litarefni. Í fyrsta lagi staðfestum við þessar prófanir með því að meðhöndla frumur með FCCP og CCCP sem neikvæðum viðmiðunum, fyrir TMRM og MitoSOX, í sömu röð, og Oligomycin og Antimycin A sem jákvæð viðmið, fyrir TMRM og MitoSOX, í sömu röð, í frumulínu manna HKC{{7} }. Þegar um TMRM prófun er að ræða, olli oligomycin meðferð 3-faldri aukningu á flúrljómunarmeðaltali TMRM samanborið við samanburðarlitinn, á meðan FCCP meðferð leiddi til 9-faldrar lækkunar. Andmycin A og CCCP leiddu til 35-faldrar aukningar og 2-faldrar lækkunar, í sömu röð, í MitoSOX prófinu (viðbótarmynd 3A og B). Til að ákvarða hvort miR-150 og miR-495 áhrif á efnaskipti hvatbera hafi kveikt á breytingum á þessum breytum, voru HKC-8 frumur umbreyttar með miR-150-5p eða miR{{17} }p herma eða samsvarandi miR-NC. Enginn tölfræðilega marktækur munur á magngreiningu flúrljómunar TMRM eða MitoSOX rannsakanna fannst á milli meðferðaraðstæðna með völdum miRs og miR-NC (viðbótarmynd 3C).
MiR-150 og miR-495 gildi eru ekki fyrir áhrifum í plasma- og nýrnasýnum frá sjúklingum með langvinnan nýrnasjúkdóm. Við metum tjáningu valinna miRNA í blóðvökva- og nýrnasýnum frá sjúklingum með langvinnan nýrnasjúkdóm. Greining á nýrnasýnum frá 26 sjúklingum (Hospital Ramn y Cajal) sýndi ekki fylgni milli gráðu bandvefsmyndunar og miR-150-5p og miR-495-3p gildi, í sömu röð (viðbótarmynd 4A og B) . Plasmaþéttni miR-150-5p í blóðrásinni, miRNA með hæstu nýrnatjáningu þessara tveggja, var einnig ákvarðað í hópi 100 langvinnandi lungnateppu sjúklinga (Hospital Príncipe de Asturias). Vegna takmarkana á framboði sýna gátum við ekki ákvarðað sermisgildi miR- 495-3p í þessum árgangi. Þessum sjúklingum var áður skipt í tvo undirhópa út frá þróun nýrnastarfsemi þeirra á 24 mánaða tímabili þannig að 50 sjúklingar sýndu minna en 10 prósent af nýrnastarfsemi versnandi en hinir höfðu upplifað að minnsta kosti 40 prósenta skerðingu á nýrnastarfsemi. virka. QRT-PCR magngreining á plasmaþéttni miR-150-5p sýndi ekki skýra tilhneigingu í átt að mismunadrifandi tjáningu í tveimur undirhópum sjúklinga (viðbótarmynd 4C).

4. Umræður
Uppgötvun miRNAs sem lykilstjórnenda meinalífeðlisfræðilegra ferla hefur ýtt undir rannsóknir á notkun þeirra sem lækningalyf í næstum öllum klínískum aðstæðum, þar með talið nýrnasjúkdómum [31]. Bandvefsbólga í nýrum er mjög algeng niðurstaða langvinns nýrnasjúkdóms (CKD) með óháð orsök, og nærvera hans er skýr spá fyrir þróun. Þess vegna hefur verulegu átaki verið varið til að bera kennsl á miRNA sem tengjast nýrnatrefjun [32,33]. Í þessari rannsókn lögðum við áherslu á sífellt mikilvægara hlutverk efnaskiptatruflana ínýruskemmdirog við fundum tvö miRNA, miR-150 og miR-495, sem voru áður óþekktir leikarar í senunni. Ennfremur komumst við að því að þau hafa mikil áhrif á líforku frumna með því að sameinast TGF- og breyta helstu efnaskiptaleiðum sem tengjast fitu.sýru oxun.
Þekjuskemmdir eru samhliða galla í fitusýruoxun, aðalorkugjafi pípulaga þekjufrumna [5]. Það leiðir til þess að aðgreining þeirra veldur skerðingu á starfsemi pípla, kveikir á stöðvun frumuhrings og stuðlar að losun mikilvægra pro-fibrotískra cýtókína sem geta stuðlað að því að virkja millivefs vöðvafíbróblastar [5,34]. MiR-150 og miR-495 tjáning var aukin í mústrefjabundinnnýruog innmannlegur nýruþekjufrumur (HKC-8) eftir meðferð með TGF-, sem bendir til þátttöku þeirra í pro-fibrotískri svörun. Athyglisvert er að í kísilgreiningu á erfðafræðilegum svæðum sem kóða fyrir miR-150 og miR-495 er hægt að bera kennsl á bindistaði fyrir umritunarþætti sem tengjast TGF-merkjasendingum og öðrum leiðum sem taka þátt í UUO skemmdum (leit í genecards.org fyrir miR-150 og miR-495). Bæði miR-150 og miR-495 lækkuðu tjáningarstig markgenanna CPT1A, PGC1 og TFAM, sem endurspeglaðist í lækkuðu grunni, ATP-tengdu og hámarks OCR og ATP innihald eftir meðferð með miR-150 og miR-495. Þessum áhrifum fylgdi aukin TGF-pro-fibrotísk svörun í HKC-8 frumum. Við komumst að því að TGF- minnkaði massa hvatbera og DNA hvatbera. Eftir meðferð með miRNA-150 og miRNA-495 kom fram lækkandi tilhneiging í innihaldi hvatbera við grunnskilyrði, jafnvel þó að það hafi ekki náð marktækum hætti. Þetta bendir til kerfis sem er óháð hlutverki PGC1 eða TFAM og líklega tengist efnaskiptaáhrifum sem tengjast CPT1A niðurstýringu sem aðalbreytan sem hefur áhrif á nærveru miRNAs. Breytingar á líforku hvatbera eru mikilvægar í nýrnasjúkdómum [35]. Í samræmi við það höfum við nýlega sýnt fram á að CPT1A er mikilvægt ensím til að varðveita heilbrigt pípulaga hólf, þar sem oftjáning þess verndar gegn bandvefsmyndun í nýrum [6]. Hins vegar, PGC1
og TFAM gen eru einnig náskyld virkni hvatbera og lífmyndun [36]. Skert tjáning þessara gena tengist langvinnan nýrnasjúkdóm, á meðan varðveisla þess stuðlar að heilleika nýrna eins og sýnt er í nokkrum gerðum af skemmdum. Þannig hafa Han o.fl. komst að því að virkni pípulaga PGC1 verndaði mýs gegn Notch-framkallaðri nýrnatrefjun og sneri við truflunum á hvatbera sem tengist þessu líkani [37]. Á sama hátt kom endurtjáning Tfam í píplufrumum í veg fyrir Notch-framkallaða efnaskipta- og pro-fibrotic endurforritun [38]. Þannig má hugsa sér að minnkuð mRNA tjáning þessara hvatbera gena, framkölluð af miR-150 og miR-495, stuðli einnig að skemmdri þekjusvipgerð.
Lækkunin sem við sáum á OCR sem tengist skemmdum á þekjufrumum er í samræmi við fyrri skýrslur, þar á meðal rannsóknir okkar með miR-33 og miR-9 [15,16]. Þar sem Kang o.fl. greindi einnig frá því að oxun glúkósa væri minni í mönnum og músum af nýrnatrefjun [5], gögn okkar sýna að míkróRNA-miðluð lækkun á OCR veldur ekki í sjálfu sér breytileika í ECAR, sem bendir til þess að stöðvun á sykursýki við trefjasjúkdóma sé líklega háð á trefjaáreiti frekar en á skertri oxandi fosfórun. Nokkur miRNA hafa verið auðkennd sem helstu breytingar á starfsemi hvatbera, þar á meðal erkitýpíska pro-fibrotic miRNA, miR-21 [39]. Bæling á PPAR-tjáningu með miR-21 hefur verið kölluð til sem aðferð þar sem þetta miRNA hefur pro-fibrotic virkni sína. Auk þess að hindra FAO, bentu markgenin fyrir miR-21 til þess að þetta miRNA þaggi niður í margvíslegum hvatberaferlum. Önnur dæmi eru mir-9 [16], miR-33 [15] og miR-30e [40,41]. Hins vegar, að því er við vitum, eru fáar skýrslur sem fjalla um microRNA stjórnun CPT1A, PGC1 og TFAM gena í samhengi við bandvefsmyndun í nýrum. Athyglisvert er að míkróRNA-214 sem stuðlar að þekju-til-mesenchymal umbreytingu (EMT) meðan á nýrnatrefjum stendur, beinist beint að TFAM í ristilkrabbameinsfrumum [42]. Þessi bæling var einnig tilkynnt fyrir miR-590-3p [43]. miR-29 fjölskyldan, einn af best einkennandi eftirlitsaðilum ECM framleiðslu í líffæratrefjum, miðar beint að PGC1 og viðheldur jafnvægi hjartans. Þannig leiðir sjúkleg þöggun á miR-29 til PGC1 uppstýringar, sem veldur djúpstæðum breytingum á lífmyndun hvatbera sem stuðla að hjartasjúkdómum [44]. Þó að gögnin okkar styðji greinilega hlutverk miR-150 og miR-495 í nýrnabandsvefsmyndun, þá væru frekari rannsóknir in vivo nauðsynlegar til að staðfesta þessa fullyrðingu.
Til að meta heilleika hvatbera rafeindaflutningakeðjunnar (ETC), lögðum við áherslu á tvo eiginleika: ΔѰm og súperoxíð róttækan anjónaframleiðslu. Við tókum eftir því að miR-150 og miR-495 breyttu ekki þessum breytum. Stöðugt ΔѰm hefur krafist fyrir lífvænleika frumna og stærð þess er mismunandi eftir frumugerðum [45]. Viðhald þess er stranglega fínstillt þar sem aukning á ΔѰm getur leitt til truflana í redoxástandinu, á meðan lækkun þess veldur minnkun á ATP framleiðslu og getur kallað fram frumudauða. Í rannsókn okkar voru breytingar á ΔѰm magngreindar með katjónískum flúrljómandi litarefninu TMRM, en framleiðsla hvatbera ofuroxíðradikala anjóna var mæld með flúormyndandi litarefninu MitoSOX Red. Notkun þessara verkfæra við aðstæður sem hafa áhrif á nýrnastarfsemi er ekki áberandi í bókmenntum. Engu að síður, í ljósi þess að engin breyting var á rannsókninni okkar, sóttum við ekki ítarlegar aðrar aðferðir til að meta redox hormesis, og þess vegna getum við ekki útilokað að þessi miRNA geti breytt kjarnasæknum tónnum eða virkni nokkurra þátta í frv.
Í klínísku umhverfi hefur verið stungið upp á miR-150 sem pro-fibrotic miRNA í lupus nephritis með því að móta TGF-merkjaboð [46,47], en miR-495 tengdist verndandi hlutverki í hjarta sykursýki bandvefsbólga [48]. Til að komast að hugsanlegri þátttöku þeirra í langvinnri lungnateppu, metum við sermis- og parenchymal gildi þeirra í tveimur mismunandi sjúklingahópum. Styrkur miRNAs í sermi hefur verið lagt til sem hugsanleg lífmerki fyrir framgang langvinnrar nýrnasjúkdóms [49,50]. Þannig er styrkur miR-21 í sermi og magn miR-29c í þvagi í samhengi við bandvefsmyndun í nýrum, sem bendir til hugsanlegs hlutverks þeirra sem lífmerkja [51, 52]. Hins vegar voru miR-150 og miR-495 gildi hvorki mismunandi í plasma- né nýrnasýnum frá sjúklingum með langvinnan nýrnasjúkdóm. Mismunandi míkróRNA tjáningarmynstur meðal tegunda og frumutegunda gæti skýrt þessa fjarveru á mismun á miR-150 og miR-495 stigum í trefjavef [53]. Þó að í sumum tilfellum sem tilkynnt er um plasmaþéttni míkróRNA gæti endurspeglað það sem er í nýrnavef, ætti einnig að íhuga aðra aðferð sem tengist seytingu miRNA í blóðrásarkerfið eða mótvægi þessarar seytingar frá öðrum líffærum [13,54].
Á heildina litið styðja niðurstöður okkar það sem miR-150 og miR-495 stuðla aðnýruþekjuvefklefiaðgreining líklega með orkuskorti, miðlað með bælingu á CPT1A, PGC1 og TFAM hvatbera virknitengdum genum. Þeir veita einnig grundvöll til að sinna hlutverki sínu in vivo, sem og hugsanlega gagnsemi þeirra sem greiningar- eða forspár lífvísar.
Framlög höfunda
SL hugsaði og stýrði rannsóknum. VM hannaði, framkvæmdi og greindi flestar tilraunir. RR aðstoðaði við microRNA fylkisgreininguna. DRP og LGB gerðu rannsóknir á tveimur mismunandi hópum langvinnra nýrnasjúkdóma. Allir höfundar aðstoðuðu við umfjöllun um niðurstöðurnar og SL og VM skrifuðu handritið.
Yfirlýsing um hagsmuni í samkeppni
Höfundar hafa enga hagsmunaárekstra.
Viðurkenningar
Þessi vinna var studd af styrkjum frá spænska vísindaráðuneytinu SAF2015-66107-R og PID2019-104233RB-I00 (SL), PI17/ 01513 (DRP) sem styrkt var af Evrópusambandinu. Byggðaþróunarsjóður, Instituto de Salud Carlos III REDinREN RD12/0021/0009 og RD16/ 0009/0016 (SL og DRP), FIS PI17/00625 (DRP), Comunidad de Madrid "NOVELREN" B2017/BMD3751), (SL og DRP), (SL og DRP), styrkur frá spænska nýrnalækningafélaginu (Fundacin Senefro 2017) til SL og FundacionNýru„Iigo Alvarez de Toledo“ (SL) allir frá Spáni. CBMSO fær stofnanastuðning frá Fundacion "Ramn Areces". VM var stutt af fordoktorsstyrk FPI-áætlunarinnar (BES- 2013-065986) frá spænska vísindaráðuneytinu.
