Viðvarandi frumueitrunarsvörun einkjarna frumna í útlægum blóði frá óbólusettum einstaklingum sem eru lagðir inn á gjörgæsludeild vegna mikilvægs COVID-19 er nauðsynlegt til að forðast banvæna niðurstöðu
Nov 02, 2023
Ágrip: Meginmarkmið þessarar rannsóknar var að ákvarða áhrif frumudrepandi virkni einkjarnafrumna í útlægum blóði (PBMC) á niðurstöðu óbólusettra einstaklinga með mikilvæga COVID-19 innlögn á gjörgæsludeild. Blóðsýnum úr 23 einstaklingum var safnað við innlögn og síðan á 2 vikna fresti í 13 vikur þar til dauða (Exitus hópur) (n=13) eða útskrift (Survival hópur) (n=10). Við fundum ekki marktækan mun á milli hópa í þjóðfélagsfræðilegum, klínískum eða lífefnafræðilegum gögnum sem gætu haft áhrif á banvæna niðurstöðu. Hins vegar minnkaði bein frumueiturhrif PBMC frá einstaklingum úr Exitus hópnum gegn gervigerð SARS-CoV-2-sýktum Vero E6 frumum verulega við innlögn (-2.69-falt; p=0. 0234) og eftir 4 vikur á gjörgæsludeild (−5.58-falt; p=0.0290), í samanburði við einstaklinga sem lifðu af, og það batnaði ekki á sjúkrahúsvist. In vitro, meðhöndlun með IL-15 þessara frumna endurheimti ekki skilvirk frumudrepandi áhrif á neinum tímapunkti fyrr en banvæn útkoma, og aukin tjáning ónæmisþreytumerkja sást í NKT, CD4+ og CD 8+ T frumur. Hins vegar jók IL-15 meðferð á PBMC frá einstaklingum í Survival hópnum marktækt frumueiturhrif í viku 4 (6.18-falt; p=0.0303). Þar af leiðandi gætu ónæmisbætandi meðferðir sem geta sigrast á ónæmisþreytu og framkallað viðvarandi, skilvirka frumueyðandi virkni verið nauðsynlegar til að lifa af meðan á sjúkrahúsinnlögn stendur vegna mikilvægs COVID-19.
Leitarorð: SARS-CoV-2; COVID-19; ónæmissvörun; frumudrepandi svörun; IL-15

cistanche tubulosa-bæta ónæmiskerfið
1. Inngangur
Nokkur tilfelli af óhefðbundinni veirulungnabólgu sem tengdist faraldri á sjávarafurðamarkaði í Wuhan-borg (Hubei-héraði, Kína) greindust í desember 2019. Ný kransæðaveiru sem kallast alvarlegt bráða öndunarfæraheilkenni coronavirus 2 (SARS-CoV-2) hratt dreifðist um heiminn sem olli heimsfaraldri kransæðaveirusjúkdómsins 2019 (COVID-19) [1]. Síðan þá hefur verið tilkynnt um 626 milljónir tilfella af COVID-19 og 6,5 milljón dauðsföllum sem tengjast því um allan heim (uppfært október 2022) [2]. Mismunandi áhættuþættir og fylgisjúkdómar geta haft áhrif á framgang COVID-19 meðal einstaklinga, sem hafði áhrif á samanburð á klínískum gögnum milli viðkomandi landa frá upphafi heimsfaraldursins [3]. Hins vegar var ákveðið að klínísk einkenni COVID-19 gætu verið mismunandi frá einkennalausri sýkingu til bráðrar öndunarerfiðleikaheilkennis (ARDS) [4]. Meðal mismunandi áhættuþátta sem tengdust meiri líkum á að fá alvarlega tegund COVID-19 eru elli, karlkyns og fyrri fylgisjúkdómar eins og sykursýki, háþrýstingur og/eða offita [5,6]. Alvarlegt og alvarlegt COVID-19 hefur einnig verið tengt frumufæð, aðallega CD4+ T eitilfrumna, sem og óhóflegri þreytu á náttúrulegum drápsfrumum (NK) og CD8+ T frumum, sem leiðir til ónæmisbælds ástands sem getur ekki hreinsað sýkinguna, auk þess að þróa alvarlega fylgikvilla eins og frumustorm og segamyndun [7]. Helsta orsök fyrir þróun alvarlegs forms sjúkdómsins og dauða hjá sjúklingum með COVID-19 hefur verið talin óhófleg bólgusvörun sem getur stuðlað að þróun losts og/eða blóðfrumnahækkunar með truflun á fjöllíffærastarfsemi [4]. Þetta heilkenni er þekkt sem cýtókínstormur [8] og það er svipað og hemophagocytic lymphohistiocytosis (sHLH) sjúkdómurinn, sem samanstendur af ofurbólguástandi af völdum veirusýkingar [9,10]. Það getur tengst því að SARS-CoV-2 notar viðtaka angíótensínbreytandi ensíms 2 (ACE2) til að sýkja markfrumurnar. Binding SARS-CoV-2 við ACE2 viðtakann, sem er víða tjáður af frumum mismunandi vefja [11], leiðir til aukningar á angíótensíni II, sem virkjar kjarnaþáttinn-kB (NF-kB). Virkjun þessa ómissandi umritunarþáttar örvar tjáningu bólgueyðandi frumudrepna, kemokína og viðloðunsameinda [12]. Þrátt fyrir þessa óhóflegu bólgusvörun virðist það vera árangurslaust að hreinsa sýkinguna og, vegna virkjunar T-frumu, getur það endað með frumudauða [13]. Þessi frumustormur getur verið ábyrgur fyrir eitilfrumnafæð [12,14] og einnig minnkuðu magni NK og CD8+ T-frumna með útþreyttri svipgerð og aukinni tjáningu hamlandi viðtaka eins og NKG2A í NK-frumum og PD{{47 }} í CD8+ T frumum [15,16]. Þar að auki minnkar tjáning kyrningamerkja eins og CD107a venjulega á yfirborði þessara frumna [15], sem sýnir tilvist skerðingar á getu til að útrýma sýktum frumum hjá einstaklingum með alvarlegan og mikilvægan COVID-19 [17 ]. Þrátt fyrir hröð alþjóðleg viðbrögð við þróun og gjöf áhrifaríkra bóluefna hefur tilkoma nýrra afbrigða sem geta sloppið frá ónæmissvörun af völdum bóluefnis leitt til hröðrar samdráttar í vörn gegn einkennum sjúkdóma [18]. Þar af leiðandi er nauðsynlegt að halda áfram rannsóknum á skilvirkum meðferðum gegn COVID-19. Nokkrar meðferðir hafa verið prófaðar til að bæta stöðu einstaklinga á sjúkrahúsi vegna alvarlegs og alvarlegs sjúkdóms, en engin hefur enn verið sannað að hún sé sértæk til að útrýma sýktum frumum eða draga úr sýkingartíðni [15,19]. Þess vegna er stuðningsmeðferð eins og súrefnis- og vökvameðferð enn meðal mikilvægustu aðferða sem beitt er við stjórnun þessara einstaklinga [2,4,16,20]. Ósértækar meðferðir eins og barksterar hafa einnig verið gagnlegar til að stjórna og draga úr of mikilli bólgusvörun [21,22]. Nýlega hafa nokkur lyf fengið leyfi frá FDA til meðferðar á einstaklingum með væga til miðlungsmikla COVID-19, svo sem molnupiravir, nirmatrelvir og ritonavir, en aðeins í neyðartilvikum fyrir þá einstaklinga sem eru í mikilli áhættu að þróast í alvarlegan sjúkdóm [23-26]. Molnupiravir sýnir breiðvirka veirueyðandi virkni vegna getu þess til að framkalla stökkbreytingu RNA með truflunum á nokkra veiru RNA-háða RNA pólýmerasa (RdRp), þar á meðal RdRp sem SARS-CoV -2 notar til afritunar og umritunar þess. RNA erfðamengi [27]. Einnig hefur verið sýnt fram á að samsetning nirmatrelvirs og ritonavirs geti stöðvað útbreiðslu sýkingarinnar í dýralíkönum með því að hindra aðal veiru próteasa 3CLpro af SARS-CoV-2- 2 [28]. Hins vegar þarf að gefa þessi veirueyðandi lyf í tengslum við aðrar ráðstafanir eins og bóluefni til að koma af stað öflugri frumudrepandi ónæmissvörun sem getur útrýmt sýktum frumum. Flestar frumur með frumudrepandi virkni, eins og CD8+ T eitilfrumur og NK og NKT frumur, krefjast tilvistar interleukin-15 (IL-15) fyrir virkni þeirra og jafnvægisstillingu [29]. IL-15 frumur CD8+ T frumur fyrir virkjun þeirra með sérstökum mótefnavaka og bætir einnig frumueiturhrif og fjölgun NK frumna. Þess vegna getur IL-15 aukið bæði meðfædd og aðlagandi frumuónæmissvörun gegn sýktum frumum [22,25]. IL-15 kemur einnig í veg fyrir að NK- og T-frumur fái frumudauða með því að stýra frumudauðaþætti eins og Bcl-2 og minnka frumudapótóþætti eins og GSK-3 [26], og forðast þannig frumufæð. Í samræmi við það hefur IL-15 verið lagt til sem nýtt ónæmisbætandi frumulyf í krabbameinsónæmismeðferð og hefur verið talið ónæmisglæði í bólusetningaráætlunum [26,30]. 1. stigs klínískar rannsóknir með innrennsli IL-15 (rhIL-15) eða IL-15 ofurörva N-803 úr mönnum hafa sýnt fram á að þetta frumudrep getur valdið marktækri stækkun og/eða virkjun af CD4+, CD8+ og NK áhrifafrumum in vivo, og því hefur það verið notað til að meðhöndla krabbamein eða veirusýkingar eins og HIV [31–35]. Þess vegna gæti notkun ónæmisbætandi efna eins og IL-15 sem geta endurheimt frumudrepandi virkni hjá einstaklingum sem eru lagðir inn á sjúkrahús vegna mikilvægs COVID-19 verið gagnleg til að hjálpa til við að hreinsa veiruna úr lífverunni. Í þessari langvarandi athugunarrannsókn einkenndum við þróun frumudrepandi ónæmissvörunar gegn SARS-CoV-2 í einkjarnafrumum í útlægum blóði (PBMC) einangruðum úr einstaklingum sem greindust með COVID-19 sem voru lagðir inn á gjörgæsludeild umönnunardeild (ICU) vegna alvarlegra fylgikvilla, sem og áhrifa þessarar viðbragðs á lokaniðurstöðu í samanburði við aðra mikilvæga áhættuþætti. Við metum einnig getu þessara frumna til að svara meðferð með IL-15 og auka frumudrepandi veirueyðandi svörun þeirra. Niðurstöðurnar sem fengust í þessari rannsókn gætu stuðlað að betri skilningi á hlutverki frumudrepandi svörunar í banvænum afleiðingum COVID-19 og til að þróast í átt að þróun árangursríkra ónæmisbætandi meðferða sem stuðla að veiruúthreinsun.

cistanche tubulosa-bæta ónæmiskerfið
Smelltu hér til að skoða Cistanche Enhance Immunity vörur
【Biðja um meira】 Netfang:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2. Efni og aðferðir
2.1. Námsgreinar
Tuttugu og þrír einstaklingar með alvarlega COVID-19 sem voru lagðir inn á gjörgæsludeild Hospital Universitario Ramón y Cajal (Madrid, Spáni) frá október 2020 til apríl 2021 voru ráðnir í þessa rannsókn. Þetta tímabil náði yfir bæði aðra og þriðju heimsfaraldursbylgju COVID-19 á Spáni (frá júní til desember 2020 og frá desember 2020 til mars 2021, í sömu röð). Þátttakendur voru teknir af handahófi við sjúkrahúsinnlögn samkvæmt eftirfarandi forsendum: heimild fyrir upplýstu skriflegu eða munnlegu samþykki til þátttöku í rannsókninni, lagðir inn á gjörgæsludeild vegna alvarlegs COVID-19, jákvætt SARS-CoV-2 RT-qPCR próf í nefkokstroki framkvæmt við innlögn á sjúkrahús samkvæmt innri staðfestum samskiptareglum, eldri en 18 ára og óbólusett gegn SARS-CoV-2 við sýkingu. Útlægum blóðsýnum og klínískum gögnum var safnað á 2 vikna fresti í samtals 13 vikur og blóðsýni voru unnin og frystuð þar til greiningin var gerð. Þetta tímabil var reiknað með hliðsjón af því að lengd sjúkrahúsdvalar á Spáni á fyrstu heimsfaraldrinum var áætlað að meðaltali 35 dagar [36], svo við gætum framkvæmt að minnsta kosti tvær heilar umferðir af ráðningu og eftirfylgni. Eftir 13 vikur var þátttakendum skipt í tvo hópa eftir lokaniðurstöðu: banvæn útkoma (n=13), héðan í frá Exitus; eða útskrift frá sjúkrahúsi (n=10), héðan í frá Lifun.
2.2. Siðferðileg yfirlýsing
Einstaklingarnir sem tóku þátt í þessari rannsókn voru ráðnir frá Hospital Universitario Ramón y Cajal (Madrid, Spáni). Allir gáfu þeir upplýst skriflegt samþykki fyrir þátttöku í rannsókninni eða urðu vitni að munnlegu samþykki með skriflegu samþykki fulltrúa til að forðast að meðhöndla menguð skjöl. Núgildandi spænsk og evrópsk persónuverndarlög tryggðu trúnað og nafnleynd allra þátttakenda. Bókun fyrir þessa rannsókn (CEI PI 32_2020-v2) var unnin í samræmi við Helsinki-yfirlýsinguna og áður endurskoðuð og samþykkt af siðanefndum Instituto de Salud Carlos III (IRB IORG0006384) og þátttökusjúkrahússins.
2.3. Frumur
Fimm millilítrum af heilblóði var safnað í EDTA Vacutainer glös (Becton Dickinson, Madrid, Spáni) og unnin strax til að einangra PMBC og plasma með Ficoll-Hypaque (Pharmacia Corporation, North Peapack, NJ, Bandaríkjunum) þéttleikastigsskilvindu, og síðan voru þau frostgeymd fram að greiningu. Lífvænleiki frumna eftir þíðingu var metinn með ljóssmásjá og frumuflæðismælingu. Vero E6 (afrískt grænt apa nýra) frumulína (ECACC 85020206) var vinsamlega útvegað af Dr. Antonio Alcami (CBM Severo Ochoa, Madrid, Spáni), og þessar frumur voru ræktaðar í DMEM bætt við 10% FCS, 2 mM L- glútamín og 100 einingar/ml penicillín og streptómýsín (Lonza, Basel, Sviss).

cistanche ávinningur fyrir karla styrkir ónæmiskerfið
2.4. Gervigerð SARS-CoV-2 sýkingargreining
Frumueitrunarvirkni gegn SARS-CoV-2 PBMC frá þátttakendum var greind með því að nota Vero E6 frumur sýktar af einhrings gervigerða veiru pNL4-3∆env_SARS CoV-2-S ∆19(G614)_Ren. Þessi veira kóðar SARS-CoV-2 topp glýkóprótein með stökkbreytingu D614G innan HIV-1 erfðamengisins, sem og Renilla luciferasa genið sem myndast eins og áður hefur verið lýst [37,38]. Afbrigði af SARS-CoV-2 sem innihélt D614G stökkbreytinguna í spike (S) próteininu byrjuðu að dreifast snemma í heimsfaraldri og urðu hratt ríkjandi á mörgum svæðum [39,40]. Í stuttu máli, einlag af Vero E6 var sýkt af pNL4-3∆env_ SARS-CoV-2-S∆19(G614)_Ren (100 ng p24 Gag/brunnur ) í 48 klst. Síðan voru frumur þvegnar og samræktaðar í 1 klst með PBMC frá þátttakendum (hlutfall 1:1), áður meðhöndlaðar eða ekki með IL -15 (13 ng/ml) í 48 klst. Skammturinn af IL-15 sem notaður var fyrir þessa rannsókn var valinn með hliðsjón af skammtinum sem áður hefur verið lýst sem veldur mestum áhrifum á NK-fjölgun (10–25 ng/ml) [41] og einnig ívilnandi stækkun frumudrepandi minnis. CD8+ T frumur (minna en eða jafnt og 5 ng/ml) [42]. Frumueyðandi virkni PBMCs á einlagi Vero E6 var ákvörðuð eftir að flotið með frumunum í sviflausn var fjarlægt og Vero E6 frumum var sundrað af plötunni með trypsín-EDTA lausn (Sigma Aldrich-Merck, Darmstadt, Þýskalandi) og síðari magngreiningu á virkni kaspasa-3 í aðskildum frumum með ljómun með því að nota Caspase-Glo 3/7 greiningarkerfi (Promega, Madison, WI, USA). Til þess að ákvarða hvaða frumudrepandi frumuhópar voru ábyrgir fyrir þessari virkni, var PBMC safnað úr flotinu og síðan greint með frumuflæðismælingu.
2.5. Flæðisfrumumælingargreining
Til litunar á svipgerðamerkjum frumuyfirborðs voru eftirfarandi samtengd mótefni notuð: CD{{0}}PE, CD8-APC-H7, CD56-FITC og CD1{{24 }}7a-PE-Cy7, keypt af BD Biosciences (San Jose, CA, Bandaríkjunum). Til litunar á þreytumerkjum voru eftirfarandi samtengd mótefni notuð: CD3-BV510, CD8-APC-H7, CD56-FITC og PD1-BV650, keypt frá BD Biosciences, sem og CD4-PE, keypt frá Immunostep SL (Salamanca, Spáni) og TIGIT-AlexaFluor700 keypt frá Thermo Fisher (Waltham, MA, Bandaríkjunum). Sýni voru tekin með því að nota BD LSRFortessa X-20 flæðifrumumæli með FACS Diva hugbúnaði v 6.0 (BD Biosciences, Franklin Lakes, NJ, Bandaríkjunum) og síðan greind með FlowJo hugbúnaði v10.0.7 (Tree Star Inc., Ashland, OR , BANDARÍKIN).
2.6. Greining á SARS-CoV-2 RNAemia
Heildar-RNA var dregið úr plasmasýnum með því að nota QIAamp MinElute Virus Kit (Qiagen Iberia, Madrid, Spáni) í sjálfvirkum útdráttarbúnaði QIAcube (Qiagen, Hilden, Þýskalandi). SARS-CoV-2 RNA uppgötvun var framkvæmd með RT-qPCR prófun með markmiðum í hjúp (E) og núkleókapsíð (N) genum, eins og áður hefur verið lýst [43], sem er hluti af bráðabirgðaleiðbeiningum Alþjóðaheilbrigðismálastofnunarinnar Stofnun (WHO) fyrir greiningarprófun á SARS-CoV- 2 [44]. Sýni voru talin jákvæð fyrir greininguna þegar gildi mælingalota (Cq) var undir 45 lotum.

cistanche ávinningur fyrir karla styrkir ónæmiskerfið
2.7. Tölfræðigreining
Allar tölfræðilegar greiningar og grafík voru gerðar með GraphPad Prism hugbúnaðarútgáfu 8.4.3 (GraphPad Software Inc., San Diego, CA, Bandaríkjunum). Hópsamanburður var gerður með Mann–Whitney U-prófi, Wilcoxon matched-pairs signed rank test, einstefnu ANOVA og Tukey's multiple comparison test. Nákvæmt próf Fisher var notað til að meta mun á klínískum eiginleikum hópanna tveggja. Gildi p < 0.{{10}}5 (tvíhliða) voru talin tölfræðilega marktæk. Meðaltal og staðalfrávik voru notuð til að reikna út Cohen's d tölfræði með því að nota Excel áhrifastærðarreiknivél [45]. Áhrifastærð 0.2, 0.5, 0.8 eða Stærri en eða jöfn 1.2 var vísbending um litla, miðlungs, stóra og mjög stóra áhrifastærð, í sömu röð [46].
3. Úrslit
3.1. Einkenni þátttakenda
Þessi langtímarannsókn náði til 23 sjúklinga sem greindust með COVID-19 sem voru lagðir inn á gjörgæsludeild vegna alvarlegra fylgikvilla. Blóðsýni voru tekin á 2ja vikna fresti í samtals 13 vikur eða þar til lokaniðurstaðan var tekin. Ekki var greint frá því að enginn þátttakenda í þessari rannsókn væri bólusettur gegn COVID-19 á þeim tíma sem sýkingin og sjúkrahúsinnlögn átti sér stað. Helstu þjóðfélagsfræðilegir og klínískir eiginleikar allra þátttakenda eru teknir saman í töflu 1.
Tafla 1. Lýðfræðileg og klínísk gögn allra þátttakenda úr Exitus hópnum og Survival hópnum sem voru ráðnir í þessa rannsókn.
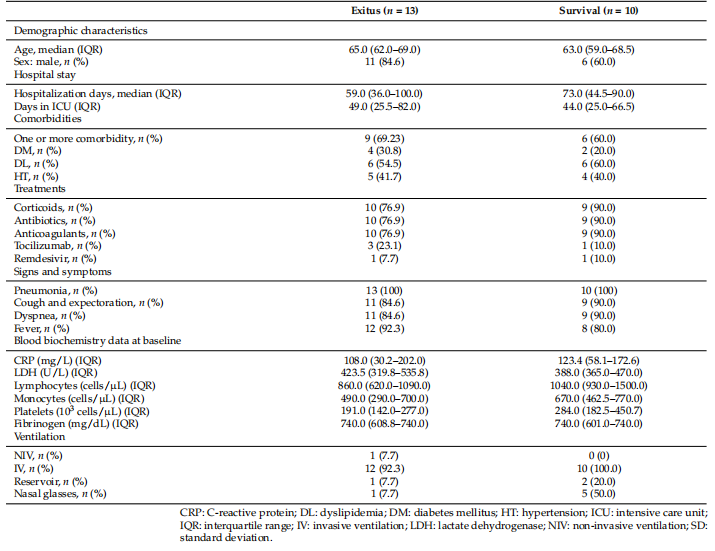
Miðgildi aldurs Exitus hópsins var 65.0 ár (IQR 62.0–69.0), en miðgildi aldurs Survival hópsins var 63.{{7} } ár (IQR 59.0–68.5). Flestir þátttakendur (73,9%) voru karlar og 65,2% höfðu að minnsta kosti einn fylgisjúkdóm. Helstu fylgisjúkdómar voru blóðfituhækkun (52,2%), háþrýstingur (39,1%) og sykursýki (26,1%). Flestir sjúklingar fengu barklyf (82,6%), sýklalyf (82,6%) og segavarnarlyf (82,6%) sem staðlaða meðferð. Þeir fengu einnig aðra meðferð eins og tocilizumab (17,4%) og remdesivir (8,7%). Algengustu einkennin voru lungnabólga (100%), hósti og upplosun (87.0%), mæði (87.0%) og hiti (87.0%). Á meðan á dvöl þeirra stóð á gjörgæsludeild þurftu 12 sjúklingar (92,3%) úr Exitus hópnum og 10 sjúklingar (100%) úr Survival hópnum ífarandi vélrænni öndun. Við fundum ekki marktækan mun á milli beggja hópa í félagslýðfræðilegum og klínískum gögnum. Við greindum einnig lífefnafræðilegar upplýsingar í blóði við grunnlínu (fyrsta sýni) milli beggja hópa, og við fundum ekki marktækan mun á milli hópa heldur. Ítarlegri upplýsingar um klínískar upplýsingar, sjúkrahúsvist og blóðlífefnafræðilegar upplýsingar hvers þátttakanda eru sýndar í viðbótartöflum S1 og S2.
3.2. Lengd dvalar á sjúkrahúsi og gjörgæsludeild
Miðgildi legutíma var 59.0 (IQR 36.0–100.0) dagar í Exitus hópnum og 73. 0 (IQR 44.5–90.{{20}}) dagar í lifunarhópnum (Mynd 1A). Miðgildi legu á gjörgæsludeild var 49,0 (IQR 25,5–82,0) dagar í Exitus hópnum og 44,0 (IQR 25,0–66,5) dagar í Survival hópnum (Mynd 1B). Enginn marktækur munur fannst á þessum breytum á milli beggja hópa.
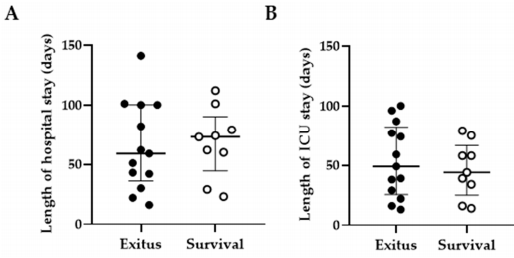
Mynd 1. Lengd sjúkrahúss og gjörgæsludeildar. Lengd dvalar á sjúkrahúsi (A) og gjörgæsludeild (B) (dagar) hjá einstaklingum með mikilvægan COVID-19 sem var skipt í tvo hópa í samræmi við lokaniðurstöðu: banvæn útkoma, brottfararhópur (fylltir punktar); eða bati og útskrift frá sjúkrahúsi, Lifunarhópur (eyðir punktar). Hver punktur samsvarar einum einstaklingi og lóðréttar línur tákna meðaltal ± staðalvillu meðaltalsins (SEM). Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu.
3.3. Magn eitilfrumna í útlægum blóði
Einstaklingar úr Exitus hópnum sýndu eitilfrumnafæð (<1000 cells/mm3 ) only at the time of hospitalization (t = 0), but at Week 2, all participants showed levels of lymphocytes above the threshold for lymphopenia (Figure 2). Lymphocyte count was 1.54 (p = 0.0318; Cohen's d = 1.00)- and 1.71 (p = 0.0030; Cohen's d = 3.17)-fold higher in patients from the Survival group in comparison with the Exitus group at baseline and after 4 weeks of hospitalization, respectively. Although both groups showed an increase in the levels of lymphocytes in peripheral blood during hospitalization, they remained on average 1.54-fold higher in individuals of the Survival group in comparison with the participants of the Exitus group for at least 10 weeks. In the Survival group, the lymphocyte counts steadily increased until Week 6 of hospitalization and then decreased until Week 10.
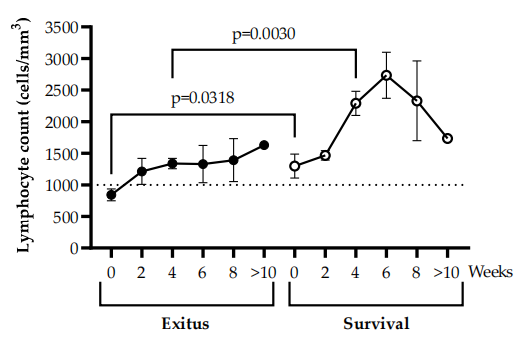
Mynd 2. Fjöldi eitilfrumna í útlægum blóði meðan á sjúkrahúsvist stendur vegna mikilvægs COVID-19. Eitilfrumufjöldi (frumur/mm3) var ákvarðaður á 2 vikna fresti í samtals 13 vikur eða þar til lokaniðurstaða í blóðsýnum frá þátttakendum Exitus (fylltir punktar) og Lifun (eyðupunktar) hóparnir. Þröskuldurinn fyrir eitilfæð er sýndur við 1000 frumur/mm3 með punktalínu. Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu og innan hópa var Wilcoxon U-prófið notað.
3.4. PBMC frumueitrunarvirkni gegn Vero E6 frumum sýktar af gervigerð SARS-CoV-2
Við metum frumudrepandi virkni PBMC sjúklinga á sjúkrahúsi í lengdarsýnum með því að magngreina caspasa-3 virkjun í einlagi af Vero E6 frumum sem sýktar eru af gervigerð SARS-CoV-2 eftir samræktun í 1 klst. hlutfall 1:1). Frumueyðandi getu PBMC sem einangruð voru úr einstaklingum úr Exitus hópnum breyttist ekki marktækt á sjúkrahúsinnlögninni og hélst stöðugt lág þar til banvænni afleiðingin varð (mynd 3). Þessi frumueyðandi virkni jókst ekki marktækt þegar þessar frumur voru örvaðar með IL-15 í 48 klst. Í Survival hópnum jókst frumudrepandi virkni PBMC 2.69-falt (p=0.0234; Cohen's d=1.12) í grunnsýninu (t {{17} }) í samanburði við Exitus hópinn og jókst það jafnt og þétt fram að 6. viku sjúkrahúsvistar. Þessi aukning sýndi tölfræðilega marktekt í samanburði milli hópa í viku 4 (5.58-falt; p=0.0290; Cohen's d=1.28). Frá og með 6. viku minnkaði frumudrepandi virkni í Survival hópnum fram að útskrift frá sjúkrahúsi, sem var í samræmi við hnignun eitilfrumnafjölda í sömu viku innlagnar (sjá mynd 2). Meðferð með IL-15 jókst 2.30-föld að meðaltali frumudrepandi virkni PBMCs einstaklinga úr Survival hópnum í öllum sýnum meðan á eftirfylgni stóð. Eftir 4 vikna sjúkrahúsinnlögn jókst frumudrepandi virkni af völdum IL-15- 6.18-falt (p=0.0303; Cohen's d=1.05) í PBMC einstaklingar úr Survival hópnum.

Mynd 3. Bein frumueiturhrif PBMC einangruð frá sjúklingum á sjúkrahúsi með mikilvæga COVID-19. Frumueyðandi getu PBMC frá einstaklingum úr hópnum Exitus (fylltir punktar) og Survival (eyðir punktar) var mæld með því að mæla kaspasa-3 virkni í einlagi af Vero E6 frumum sem sýktar voru af gervigerð SARS-CoV-2 eftir samræktun (1:1) í 1 klst. við grunnskilyrði (gráar línur) eða eftir meðferð með IL-15 í 48 klst. (svartar línur). Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu og innan hópa var Wilcoxon U-prófið notað.
3.5. Stig NK og NKT frumna
Magn frumna með frumudrepandi svipgerð var greind í PBMC sem voru samræktaðar með Vero E6 frumum sýktar með gervigerð SARS-CoV-2. Við fundum ekki marktækan mun á magni frumna með NK svipgerð (CD3-CD56+) milli beggja hópa einstaklinga, jafnvel eftir meðferð með IL-15 (Mynd 4A). Tjáning afkornunarmerkja CD107a á yfirborði þessara frumna hélst óbreytt hjá einstaklingum úr Exitus hópnum. Þrátt fyrir að þessi tjáning hafi aukist jafnt og þétt frá viku 4 og fram að útskrift á sjúkrahúsi í Survival hópnum náði þessi munur ekki tölfræðilega marktekt í samanburði við Exitus hópinn (Mynd 4B). Meðferð með IL-15 breytti ekki tjáningu CD107a í þessum frumum marktækt. Frá viku 4 sýndu PBMC frá einstaklingum úr báðum hópum aukningu á magni frumna með NKT svipgerð (CD3+CD56+) sem var 4.17-falt hærra í PBMC frá einstaklinga í Exitus hópnum í viku 6, þó að þessi munur hafi ekki náð marktækni (p=0.0571; Cohen's d=3.15) (Mynd 5A). Þessi aukning var örlítið meiri þegar frumur voru meðhöndlaðar með IL-15 í báðum hópum, þó að gögn hafi ekki náð tölfræðilegri marktekt heldur (Mynd 5A). Tjáning CD107a breyttist ekki marktækt milli beggja hópa eða eftir meðferð með IL-15 (Mynd 5B).

Mynd 4. Magn NK-frumna í PBMC frá einstaklingum á sjúkrahúsi með mikilvægan COVID-19. (A) Heildarmagn NK-frumna (CD3-CD56+) og (B) tjáning á afkornunarmerkinu CD107a í þessum frumum var metið í PBMC við grunnskilyrði (gráar línur) eða eftir meðferð með IL-15 í 48 klst (svartar línur) eftir samræktun (1:1) með Vero E6 frumum sýktar af gervigerð SARS-CoV-2 í 1 klst. Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófi og innan hópa var Wilcoxon U-próf notað.

Mynd 5. Stig NKT frumna í PBMC frá einstaklingum á sjúkrahúsi með mikilvægan COVID-19. Heildarmagn NKT frumna (CD3+CD56+) (A) og tjáning afkornunarmerkinu CD107a í þessum frumum (B) var metið við grunnskilyrði (gráar línur) eða eftir meðferð með IL{ {5}} í 48 klst (svartar línur) eftir samræktun (1:1) í 1 klst með Vero E6 frumum sýktar af gervigerð SARS-CoV-2. Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu og innan hópa var Wilcoxon U-prófið notað.
3.6. Stig CD8+ T fruma
CD8-fjöldi var aukinn 2.07-falt (p=0.0409; Cohen's d=0.94) í grunnsýni (t=0) í Exitus hópnum í samanburði með Survival hópnum, og þessi stig hélst stöðug þar til banvæn útkoma (Mynd 6A). IL-15 hafði ekki marktæk jákvæð áhrif á magn þessa frumuþýðis. Í Survival hópnum voru CD8+ T frumur minnkaðar 1.51-falt að meðaltali í samanburði við Exitus hópinn (Mynd 6A). Tjáning CD107a minnkaði 1.53-falt (p=0.0313) í viku 4 í CD8+ T-frumum frá einstaklingum í Exitus hópnum og hélst óbreytt þar til banvænt útkoma. Meðferð með IL-15 sýndi örlítinn ávinning í tjáningu þessa afkornunarmerkis, en þessi munur var ekki marktækur (Mynd 6B). Í Survival hópnum var einnig minnkun á tjáningu CD107a í CD8+ T-frumum í viku 4, og síðan var aukning áfram, en engin þýðing náðist fyrir eða eftir meðferð með IL{{26 }} (Mynd 6B).

Mynd 6. Magn CD8+ T-frumna í PBMC frá einstaklingum á sjúkrahúsi með mikilvægan COVID-19. (A) Heildarmagn CD8+ T-frumna (CD3+CD8+) og (B) tjáningu á afkornunarmerkinu CD107a í þessum frumum var metið í PBMC við grunnskilyrði (gráar) línur) eða eftir meðferð með IL-15 í 48 klst (svartar línur) eftir samræktun (1:1) með Vero E6 frumum sýktar af gervigerð SARS-CoV-2 í 1 klst. Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu og innan hópa var Wilcoxon U-prófið notað.
3.7. Stig þreytumerkja
Tjáningarmagn ónæmisþreytingarmerkjanna PD-1 (Programmed cell death protein) og TIGIT (T cell immunoreceptor with Ig and ITIM domains) voru greind með frumuflæðisgreiningu í CD4+ T frumum og frumudrepandi frumum frá allir þátttakendur. Sýni sem fengust við innlögn á sjúkrahús (t=0) fram að 6. viku sjúkrahúsvistar voru greind, vegna skorts á sýnum tiltækum eftir þann tíma. CD4+ og CD8+ T frumur frá einstaklingum úr Exitus hópnum sýndu magn PD-1 sem var marktækt aukið um 1,72 (p=0.0095; Cohen's d {{ 11}}.87)- og 2.92-falt (p=0.0317; Cohen's d=2.07) eftir 4 vikna sjúkrahúsinnlögn, í sömu röð, í samanburði við einstaklinga frá Lifunarhópur (Mynd 7A, B, línurit til vinstri). Í NKT frumum jókst þéttni TIGIT marktækt frá innlögn á sjúkrahús þar til 6 vikna sjúkrahúsvist hjá einstaklingum úr Exitus hópnum og þessi þéttni jókst 1.76-falt (p=0.0357 ; Cohen's d=0.33) eftir 2 vikna sjúkrahúsinnlögn, í samanburði við Lifun hópinn (Mynd 7C, hægra línurit).
Enginn marktækur munur sást á milli hópa á tjáningarstigum þessara þreytumerkja í NK frumum (Mynd 7D).

Mynd 7. Tjáningarstig þreytumerkja í PBMC frá einstaklingum á sjúkrahúsi með mikilvægan COVID-19. Tjáningarstig PD-1 og TIGIT í CD4+ T frumum (A), CD8+ T frumum (B), NKT frumum (C) og NK frumum (D). Hver punktur samsvarar meðaltali gagna og lóðréttar línur tákna SEM. Tölfræðileg marktekt milli hópa var reiknuð út með Mann–Whitney U-prófinu og innan hópa var ANOVA notað.
3.8. Magngreining á SARS-CoV-2 RNAemia í plasma
Tilvist RNA frá SARS-CoV-2 var greind í blóðvökva allra einstaklinga í grunnsýni (t=0), og engar jákvæðar niðurstöður fengust hjá neinum þátttakendum, með Cq gildi undir mörkum af jákvæðri greiningu á 45 lotum.
4. Umræður
SARS-CoV-2 sýking getur valdið nokkrum klínískum birtingum COVID-19, allt frá einkennalausri sýkingu til alvarlegs, alvarlegs eða jafnvel banvæns sjúkdóms [4]. Þrátt fyrir að almenn bólusetning íbúanna hafi dregið mjög úr alvarlegum tegundum sjúkdómsins, eykur tilkoma nýrra afbrigða af SARS-CoV-2 fjölda einstaklinga sem fá alvarlega COVID-19 og þurfa að lögð inn á sjúkrahús vegna gegnumbrotssýkinga [47,48]. Þess vegna er það enn forgangsverkefni að þróa fyrirbyggjandi og meðferðaraðferðir sem gætu komið í veg fyrir þróun mikilvægra tegunda COVID-19 og banvæna afleiðinga hjá sjúklingum á sjúkrahúsi. Því hefur verið lýst að eldra fólk með fylgisjúkdóma sé í meiri hættu á að fá alvarlega og alvarlega COVID{{1{{30}}}} [49]. Á Spáni eru mikilvægustu óháðu spádómarnir um dauða af völdum COVID-19 karlmenn eldri en 50 ára með tilheyrandi fylgikvilla eins og háþrýsting og sykursýki [36]. Í rannsókn okkar sýndu flestir þátttakendur beggja hópa þessa eiginleika, án marktæks muns á milli þeirra í félagsfræðilegum, klínískum eða lífefnafræðilegum gögnum sem geta haft áhrif á alvarleika sjúkdómsins eða banvæna niðurstöðu. Reyndar sýndu báðir hóparnir aukið magn lífefnafræðilegra þátta sem hafa tengst meiri hættu á slæmri niðurstöðu COVID-19, eins og C-reactive protein (CRP) og laktat dehýdrógenasa (LDH) [50–56 ]. Á hinn bóginn, þó að greint hafi verið frá því að einstaklingar með alvarlega COVID-19 gætu verið með greinanlegt SARS-CoV-2 RNAnemia [54], sem hefur tengst aukinni hættu á dánartíðni [55], enginn þátttakenda í rannsókn okkar sýndi greinanlegt RNA í sermi, svo við gátum ekki staðfest fylgni á milli greinanlegrar veiruhvarfs og banvæns útkomu. Að lokum sýnir COVID-19 lengri legutíma á sjúkrahúsi og dánartíðni í samanburði við aðra smitsjúkdóma sem krefjast innlagnar á gjörgæsludeild, svo sem lungnabólga (CAP) eða blóðsýkingu [56], og það var áætlað í 35. daga að meðaltali fyrir þá einstaklinga sem voru lagðir inn á sjúkrahús á Spáni á fyrstu heimsfaraldrinum [36]. Í rannsókn okkar var miðgildi legutíma á sjúkrahúsi svipuð hjá bæði Exitus og Survival hópnum (59,0 og 73,0 dagar, í sömu röð) og 50% allra þátttakenda dvöldu lengur en 40 daga á gjörgæsludeild. Þess vegna þarf að huga að öðrum mismunaþáttum til að skýra banvæna niðurstöðu í Exitus hópnum og bata í Survival hópnum.

Kostir cistanche tubulosa-styrkja ónæmiskerfið
Eitilfæð er einnig talin áhættuþáttur fyrir alvarleika sjúkdómsins sem hefur tengst lengri legutíma [57]. Í rannsókn okkar sýndu 73,9% þátttakenda í bæði Exitus og Survival hópnum lága eitilfrumnafjölda. Hins vegar var magn heildareitilfrumna hærra að meðaltali hjá þátttakendum Survival hópsins, samanborið við Exitus hópinn. Þetta er í samræmi við fyrri athugun að þeir einstaklingar sem dóu af völdum COVID-19 fá alvarlegri eitilfæð með tímanum samanborið við þá sem lifa af [58] og að þessar eitilfrumur sýna venjulega útþreytta svipgerð, sem leiðir til hægfara ónæmisbrest [15,16]. Vegna þess að áhrifarík frumudrepandi veirueyðandi svörun er nauðsynleg til að hafa stjórn á veirusýkingum, þar á meðal SARS-CoV-2 [17], er ónæmisuppbygging mikilvæg fyrir bata frá COVID-19. Hröðun þessarar ónæmisuppbyggingar veltur að miklu leyti á útlægri útþenslu eitilfrumna, sem getur verið góð aðferð til að bæta árangur einstaklinga sem eru lagðir inn á sjúkrahús vegna alvarlegs COVID-19-19 [58]. IL-15 er frumufrumur sem er nauðsynlegt fyrir virkni og samvægi CD8+ T-frumna, NK og NKT frumna [29], og það hefur verið lagt til sem ný ónæmisbælandi meðferð við nokkrum sjúkdómum eins og krabbameini og HIV sýkingu [26,30,35,59]. Þess vegna, í þessari rannsókn, metum við hvort meðferð in vitro með IL-15 gæti bætt frumudrepandi svörun í PBMC einstaklinga á sjúkrahúsi með alvarlegan og alvarlegan COVID-19 eftir því sem sýkingin þróaðist, til að ákvarða réttmæti hennar sem frambjóðandi til að örva ónæmisuppbyggingu meðan á COVID-19 stendur. Þegar skammturinn var mældur sáum við heildaraukningu á frumudrepandi svörun gegn markfrumum sem sýktar voru af gervigerð SARS-CoV-2 í PBMC þeirra einstaklinga sem lifðu COVID-19 eftir 44 daga að meðaltali eftir sjúkrahúsinnlögn kl. gjörgæsludeild. Þessi frumudrepandi svörun jókst í raun 2.3-falt að meðaltali við meðferð með IL-15 í öllum sýnum sem safnað var meðan á eftirfylgni stóð, þar sem 6. viku sjúkrahúsinnlagnar var vendipunkturinn þar sem bæði eitilfrumur teljast og frumudrepandi virknin fór að minnka þar til útskrift var útskrifuð. Þrátt fyrir að deila svipuðum þjóðfélagsfræðilegum, klínískum og lífefnafræðilegum eiginleikum og hafa verið lagður inn á sjúkrahús í næstum jafnlangan tíma (alls 59 dagar, þar af 49 dagar á gjörgæsludeild), hópur einstaklinga sem lifði ekki COVID af{{34} } sýndu PBMC sem svöruðu ekki í nærveru sýktu markfrumna, jafnvel þegar þær voru örvaðar með IL-15. Heildarmagn eitilfrumna var yfir viðmiðunarmörkum eitilfæðingar hjá einstaklingum úr þessum hópi frá 2. viku sjúkrahúsvistar. Hins vegar jukust þessi gildi ekki marktækt á meðan á sjúkrahúsinnlögn stóð og engin áhrifarík veirueyðandi svörun greindist, jafnvel í nærveru IL-15 við greindan skammt. Engu svari við IL-15 hefur verið lýst fyrir aðrar langvarandi sýkingar eins og ónæmisbrestsveiru (HIV), lifrarbólgu C veiru (HCV), lifrarbólgu B veiru (HBV) og manna T eitilfrumuveiru (HTLV), þar sem þreyta ónæmiskerfisins getur haft áhrif á tjáningu sértæks viðtaka IL-15, CD122, í CD8+ T-frumum [60], sem gerir það að verkum að þær bregðast ekki við þessu homeostatic áreiti. Ónæmisþreytingin sem er einkennandi fyrir COVID-19 hefur ekki aðeins sést í CD8+ T-frumum heldur einnig í öðrum frumueyðandi frumugerðum eins og NK- og NKT-frumum [15,16]. Þess vegna gæti fjarvera á svörun við IL-15 í PBMC frá Exitus hópnum tengst aukinni ónæmisþreytu sem ekki var hægt að vinna bug á með IL-15 meðferð einni og sér í greindum skammti. Þetta hefur einnig komið fram í I. stigs klínískum rannsóknum þar sem einlyfjameðferð með IL-15 var árangurslaus þrátt fyrir mikla stækkun frumudrepandi frumna [31,32]. Þar af leiðandi væri önnur samörvandi meðferð nauðsynleg til að framkalla árangursríka svörun hjá þessum einstaklingum, svo sem ónæmisfræðilegir eftirlitsstöðvarhemlar eða einstofna mótefni sem miða að sýktum frumum, til að auka mótefnaháð frumueiturhrif (ADCC).
Við ákváðum einnig frumugerðirnar sem áttu aðallega þátt í þróun þessarar auknu frumudrepandi svörunar í hópi einstaklinga sem lifðu COVID af-19. Sýnt hefur verið fram á að tilvist virkra CD8+ T-frumna er nauðsynleg til að vernda dýralíkön gegn þróun alvarlegs COVID-19 [61,62]. Ennfremur hefur skortur á skilvirku 8-miðlaðri frumudrepandi svörun verið tilnefnd sem mikilvægur þáttur í auknu næmi aldraðra fyrir að þróa með sér alvarlegt eða alvarlegt COVID-19 [63]. Það kemur á óvart að magn CD8+ T-frumna var 2.07-falt (p=0.0409) hærra í Exitus-hópnum á sjúkrahúsinnlögn (t=0) , og þeir héldust auknir þar til banvænni afleiðingin var, í samanburði við Survival hópinn. Þrátt fyrir að einstaklingar úr Exitus hópnum sýndu eitilfrumnafjölda örlítið yfir viðmiðunarmörkum eitilfæð, hélst þessi gildi nánast óbreytt allan þann tíma sem þeir voru á sjúkrahúsi. Ennfremur hefur því verið lýst að eitilfrumnafæð gæti leitt til samhliða bælingar og virkjunar þar sem útlægt tap er á T-frumum samhliða mikilli fjölgun CD8+ T-frumusamstæðunnar [64,65]. Þetta myndi gera grein fyrir örlítið auknu magni CD8+ T-frumna sem sést hafa í PBMCs þátttakenda úr Exitus hópnum frá 6. viku sjúkrahúsvistar og áfram, þrátt fyrir að heildarmagn eitilfrumna haldist óbreytt og yfir viðmiðunarmörkum eitilfrumna. sem gefur einnig til kynna hugsanlega fækkun CD4+ T-frumna. Hins vegar sýndu þessar CD8+ T frumur litla frumudrepandi virkni, eins og var ákvarðað af lítilli tjáningu á afkornunarmerkinu CD107a á yfirborði frumunnar, en tjáning þessa merkis jókst í CD8+ T frumum frá þátttakendur Survival hópsins frá og með viku 4. Tjáning CD107a er talin lífmerki til að meta frumudrepandi getu [66] og því hefur verið lýst að hún sé minnkuð á yfirborði frumna sem eru einangraðar frá einstaklingum með COVID-19, samanborið við ósýkta, heilbrigða gjafa [15 ].
Þess vegna gæti aukin tjáning CD107a á yfirborði CD8+ T-frumna að minnsta kosti að hluta til skýrt framlag þessara frumna til aukinnar frumueyðandi virkni sem sést í PBMCs þátttakenda úr Survival hópnum. Að auki sáum við aukna tjáningu á þreytumerkinu PD-1 í bæði CD4+ og CD8+ T-frumum frá einstaklingum í Exitus hópnum, sem gæti einnig stuðlað að minni frumudrepandi áhrifum virkni og svörun við IL-15 þessara frumna. Aðrir frumuhópar geta tekið þátt í frumudrepandi virkni gegn gervigerðum SARS-CoV-2-sýktum frumum, eins og NK og NKT frumum. Eins og gerist með aðrar alvarlegar bráðar sýkingar, gætu NK frumur verið ráðnar á sýkingarstaðinn með SARS-CoV -2 [67], sem myndi útskýra minnkaðan fjölda NK frumna í blóðrás sem sást hjá öllum þátttakendum. Þar að auki gæti frumustormurinn sem myndast við alvarlegan og mikilvægan COVID-19 leitt til óvirkrar stöðu NK-frumna sem myndu tjá mikið magn af hamlandi viðtökum eins og NKG2A eða PD-1 [68]. Í rannsókn okkar var magn NK-frumna svipað hjá báðum hópum fram í viku 6, þar sem þátttakendur í Survival hópnum sýndu stigvaxandi aukningu fram að útskrift frá sjúkrahúsi. Þetta tengdist aukinni tjáningu á CD107a, sem hefur verið tengt í NK-frumum við aukna frumueytingu og bættri leysingu markfrumna [7,69], þó að hlutfall NK-frumna sem tjá virkjunarmerki eins og CD107a hafi verið lýst vera lægri hjá einstaklingum með COVID-19 samanborið við heilbrigða stjórna [70]. Hins vegar, þrátt fyrir að magn NKT frumna hafi aukist til muna í lifunarhópnum frá og með viku 6, hélst tjáning CD107a næstum óbreytt, á meðan þær sýndu aukið magn af þreytumerkinu TIGIT á yfirborði frumunnar sem jókst jafnt og þétt fram í viku 6. . Ein mikilvægasta takmörkun rannsóknarinnar okkar var minnkað úrtak. Engu að síður náðist tölfræðileg marktækni á milli hópa í nokkrum mikilvægum breytum sem sýndu einnig mikla eða mjög mikla áhrifastærð þegar samanlagður munur milli hópa var reiknaður.

cistanche tubulosa-bæta ónæmiskerfið
5. Ályktanir
Að lokum má segja að mikilvægasta framlag þessarar rannsóknar í baráttunni gegn ónæmissjúkdómum af völdum SARS-CoV-2 sýkingar er staðfesting þess að skert veirueyðandi getu PBMCs virtist vera mikilvægur þáttur í framvindu til banvæns COVID{ {2}}, jafnvel umfram aðra þjóðfélagsfræðilega, klíníska og lífefnafræðilega þætti. Þess vegna getur notkun ónæmisbætandi meðferða sem geta aukið frumudrepandi áhrif stuðlað að jákvæðri niðurstöðu á sjúkrahúsvist vegna mikilvægs COVID-19. Aukin frumudrepandi virkni sem miðlað er af IL-15 hjá einstaklingum úr Survival hópnum treysti líklega ekki á aukið magn frumudrepandi frumna heldur á ónæmishæfni þessara frumna til að bregðast við slíku áreiti. Þess vegna gæti vöktun á tjáningu þreytumerkja og svörun við hómóstatískum áreiti eins og IL-15 þessara frumuhópa hjá einstaklingum á sjúkrahúsi verið gagnleg sem forspármerki um banvæna niðurstöðu til að hefja frekari ráðstafanir til að koma í veg fyrir það. Þess vegna er þessi athugunarrannsókn sönnun þess að notkun IL-15 hjá einstaklingum á sjúkrahúsi með COVID-19 gæti bætt veirueyðandi ónæmissvörun, þó að þetta áreiti eitt og sér myndi ekki skila árangri hjá þeim einstaklingum sem ekki svara. frumur vegna þreytu ónæmis eða skertrar IL-15R boðleiðar, sem er nauðsynlegt til að koma í veg fyrir þreytu [71], jafnvel þegar þær sýna eitilfrumnafjölda yfir viðmiðunarmörkum eitilfæð. Fleiri rannsóknir með stærri þýði eru nauðsynlegar til að meta samsetningar vaxandi skammta af IL-15 með öðrum ónæmisbælandi lyfjum eins og ónæmiseftirlitshemlum eða einstofna mótefni sem miða á sýktar frumur til að hjálpa til við að endurheimta og auka veirueyðandi svörun meðan á mikilvægum tegundum COVID stendur. -19.
Heimildir
1. Atzrodt, CL; Maknojia, I.; McCarthy, RDP; Oldfield, TM; Po, J.; Ta, KTL; Stepp, HANN; Clements, TP Leiðbeiningar um COVID-19: Alheimsfaraldur af völdum hinnar nýju kransæðaveiru SARS-CoV-2. FEBS J. 2020, 287, 3633–3650. [CrossRef] [PubMed]
2. Mælaborð WHO Coronavirus (COVID-19). Aðgengilegt á netinu: https://covid19.who.int/ (sótt 18. október 2022).
3. Capalbo, C.; Aceti, A.; Simmaco, M.; Bonfini, R.; Rocco, M.; Ricci, A.; Napoli, C.; Rocco, M.; Alfonsi, V.; Teggi, A.; o.fl. Veldisstig COVID-19 heimsfaraldursins á Mið-Ítalíu: Samþætt umönnunarleið. Alþj. J. Umhverfi. Res. 2020, 17, 3792. [CrossRef] [PubMed]
4. Huang, C.; Wang, Y.; Li, X.; Ren, L.; Zhao, J.; Hu, Y.; Zhang, L.; Fan, G.; Xu, J.; Gu, X.; o.fl. Klínísk einkenni sjúklinga sem smitaðir eru af 2019 nýrri kransæðaveiru í Wuhan, Kína. Lancet 2020, 395, 497–506. [CrossRef] [PubMed]
5. Haybar, H.; Kazemnia, K.; Rahim, F. Undirliggjandi langvinn sjúkdómur og COVID-19 sýking: Nýjustu endurskoðun. Jundishapur J. Chronic Dis. Umönnun 2020, 9, e103452. [CrossRef] 6. Hamed, SM; Elkhatib, WF; Khairalla, AS; Noreddin, AM Global dynamics of SARS-CoV-2 clades og tengsl þeirra við COVID{11}} faraldsfræði. Sci. Rep. 2021, 11, 8435. [Krossvísun]
7. Erdinc, B.; Sahni, S.; Gotlieb, V. Blóðfræðileg einkenni og fylgikvillar COVID-19. Adv. Clin. Exp. Med. 2021, 30, 101–107. [Krossvísun]
8. Hu, B.; Huang, S.; Yin, L. Cýtókínstormurinn og COVID-19. J. Med. Virol. 2021, 93, 250–256. [Krossvísun]
9. Ramos-Casals, M.; Brito-Zerón, P.; López-Guillermo, A.; Khamashta, MA; Bosch, X. Blóðfrumnaheilkenni fullorðinna. Lancet 2014, 383, 1503–1516. [Krossvísun]
10. Mehta, P.; McAuley, DF; Brown, M.; Sanchez, E.; Tattersall, RS; Manson, JJ; fyrir hönd HLH Across Specialty Collaboration, Bretlandi. Yfir sérgrein. COVID-19: Hugleiddu frumustormheilkenni og ónæmisbælingu. Lancet 2020, 395, 1033–1034. [Krossvísun]
11. Li, M.-Y.; Li, L.; Zhang, Y.; Wang, X.-S. Tjáning SARS-CoV-2 frumuviðtakagensins ACE2 í fjölmörgum vefjum manna. Smitast. Dis. Fátækt 2020, 9, 45. [Krossvísun]
12. Jiang, Y.; Rubin, L.; Peng, T.; Liu, L.; Xing, X.; Lazarovici, P.; Zheng, W. Cytokine stormur í COVID-19: Frá veirusýkingu til ónæmissvörunar, greiningar og meðferðar. Alþj. J. Biol. Sci. 2022, 18, 459–472. [CrossRef] [PubMed]
13. Zhan, Y.; Carrington, EM; Zhang, Y.; Heinzel, S.; Lew, AM Líf og dauði virkra T-frumna: Hvernig eru þær frábrugðnar barnalegum T-frumum? Framan. Immunol. 2017, 8, 1809. [CrossRef] [PubMed]
14. Huang, I.; Pranata, R. Lymphopenia in severe coronavirus disease-2019 (COVID-19): Kerfisbundin endurskoðun og meta-greining. J. Gjörgæsla 2020, 8, 36. [CrossRef] [PubMed]
15. Zheng, M.; Gao, Y.; Wang, G.; Söngur, G.; Liu, S.; Sun, D.; Xu, Y.; Tian, Z. Virkur þreyta veirueyðandi eitilfrumna hjá COVID-19 sjúklingum. Cell. Mol. Immunol. 2020, 17, 533–535. [Krossvísun]
16. Rha, M.-S.; Jeong, HW; Ko, J.-H.; Choi, SJ; Seo, I.-H.; Lee, JS; Sa, M.; Kim, AR; Joo, E.-J.; Ahn, JY; o.fl. PD-1-tjáir SARS-CoV-2-sérstakar CD8+ T-frumur eru ekki útkeyrðar, en virkar hjá sjúklingum með COVID-19. Ónæmi 2021, 54, 44–52. [Krossvísun]
17. Vigón, L.; Fuertes, D.; García-Pérez, J.; Torres, M.; Rodríguez-Mora, S.; Mateos, E.; Corona, M.; Saez-Marín, AJ; Malo, R.; Navarro, C.; o.fl. Skert frumudrepandi svörun í PBMC frá sjúklingum með COVID-19 lagðir inn á gjörgæsludeild: lífmerki til að spá fyrir um alvarleika sjúkdómsins. Framan. Immunol. 2021, 12, 665329. [Krossvísun]
18. HVER. Bráðabirgðayfirlýsing um ákvarðanatöku í tengslum við notkun afbrigði uppfærðra COVID-19 bóluefna. Fáanlegt á netinu: https://www.who.int/news/item/17-06-2022-interim-statement-on-decision-making-considerations-for-the-use-of variant-updated-covid{{15} }bóluefni (sótt 15. ágúst 2022).
19. Mishra, SK; Tripathi, T. Eins árs uppfærsla um COVID-19 heimsfaraldurinn: Hvar erum við núna? Acta Trop. 2021, 214, 105778. [CrossRef] 20. Li, X.; Geng, M.; Peng, Y.; Meng, L.; Lu, S. Sameindaónæmissjúkdómur og greining á COVID-19. J. Pharm. endaþarm. 2020, 10, 102–108. [Krossvísun]
21. TRC Group. Dexametasón hjá sjúklingum á sjúkrahúsi með COVID-19. N. Engl. J. Med. 2021, 384, 693–704. [Krossvísun]
22. Zhou, X.; Yu, J.; Cheng, X.; Zhao, B.; Manyam, GC; Zhang, L.; Schluns, K.; Li, P.; Wang, J.; Sun, S.-C. Deubiquitinase Otub1 stjórnar virkjun CD8+ T-frumna og NK-frumna með því að stjórna IL-15-miðlaðri frumun. Nat. Immunol. 2019, 20, 879–889. [Krossvísun]
23. Parums, DV Núverandi staða veirueyðandi lyfja til inntöku við SARS-CoV-2 sýkingu hjá sjúklingum sem ekki eru á sjúkrahúsi. Med. Sci. Monit. 2022, 28, e935952-1. [CrossRef] [PubMed]
24. Couzin-Frankel, J. Veirueyðandi pillur gætu breytt gangi heimsfaraldurs. Am. Assoc. Adv. Sci. 2021, 12, 799–800. [CrossRef] [PubMed]
25. Muntasell, A.; Ochoa, MC; Cordeiro, L.; Berraondo, P.; de Cerio, AL-D.; Cabo, M.; López-Botet, M.; Melero, I. Miða á NK-frumueftirlitsstöðvar fyrir ónæmismeðferð gegn krabbameini. Curr. Opin. Immunol. 2017, 45, 73–81. [CrossRef] [PubMed]
26. Patidar, M.; Yadav, N.; Dalai, SK Interleukin 15: Lykilfrumuefni fyrir ónæmismeðferð. Cytokine Growth Factor Rev. 2016, 31, 49–59. [Krossvísun]
27. Kabinger, F.; Stiller, C.; Schmitzová, J.; Dienemann, C.; Kokic, G.; Hillen, HS; Höbartner, C.; Cramer, P. Mechanism of molnupiravir-induced SARS-CoV-2 stökkbreytingar. Nat. Uppbygging. Mol. Biol. 2021, 28, 740–746. [CrossRef] [PubMed]
28. Hung, Y.-P.; Lee, J.-C.; Chiu, C.-W.; Lee, C.-C.; Tsai, P.-J.; Hsu, I.-L.; Ko, W.-C. Nirmatrelvir/Ritonavir meðferð til inntöku fyrir COVID-19: The Dawn in the Dark? Sýklalyf 2022, 11, 220. [CrossRef]
29. Guo, Y.; Luan, L.; Patil, NK; Sherwood, ER Ónæmislíffræði IL-15/IL-15R flókins sem æxlis- og veirueyðandi efni. Cytokine Growth Factor Rev. 2017, 38, 10–21. [Krossvísun]
30. Zhang, S.; Zhao, J.; Bai, X.; Handley, M.; Shan, F. Líffræðileg áhrif IL-15 á ónæmisfrumur og möguleika þess til að meðhöndla krabbamein. Alþj. Immunopharmacol. 2021, 91, 107318. [Krossvísun]
31. Waldmann, TA; Dubois, S.; Miljkovic, læknir; Conlon, KC IL-15 í samsettri ónæmismeðferð við krabbameini. Framan. Immunol. 2020, 11, 868. [Krossvísun]
32. Dubois, SP; Miljkovic, læknir; Fleisher, TA; Pittaluga, S.; Hsu-Albert, J.; Bryant, BR; Petrus, MN; Perera, LP; Müller, JR; Shih, JH; o.fl. Skammtíma IL-15 gefið sem stöðugt innrennsli leiddi til gríðarlegrar stækkunar á virkum NK frumum: Afleiðingar fyrir samsetta meðferð með æxlismótefnum. J. Immunother. Krabbamein 2021, 9, e002193. [Krossvísun]
33. Conlon, KC; Potter, EL; Pittaluga, S.; Lee, C.-CR; Miljkovic, læknir; Fleisher, TA; Dubois, S.; Bryant, BR; Petrus, M.; Perera, LP; o.fl. IL15 með stöðugu innrennsli í bláæð til fullorðinna sjúklinga með föst æxli í I. stigs rannsókn framkallað dramatískt NK-frumu undirhóp. Clin. Cancer Res. 2019, 25, 4945–4954. [Krossvísun]
34. Romee, R.; Cooley, S.; Berrien-Elliott, MM; Westervelt, P.; Verneris, MR; Wagner, JE; Weisdorf, DJ; Blazar, BR; Ustun, C.; DeFor, TE; o.fl. Fyrsta stigs 1 klínísk rannsókn á IL-15 ofurörva flóknum ALT-803 til að meðhöndla bakslag eftir ígræðslu. Blóð Am. J. Hematol. 2018, 131, 2515–2527. [CrossRef] [PubMed]
35. Miller, JS; Davis, ZB; Helgeson, E.; Reilly, C.; Þorkelsson, A.; Anderson, J.; Lima, NS; Jorstad, S.; Hart, GT; Lee, JH; o.fl. Öryggi og veirufræðileg áhrif IL-15 ofurörva N-803 hjá fólki sem lifir með HIV: 1. stigs rannsókn. Nat. Med. 2022, 28, 392–400. [CrossRef] [PubMed]
36. Berenguer, J.; Ryan, P.; Rodríguez-Baño, J.; Jarrín, I.; Carratalà, J.; Pachón, J.; Yllescas, M.; Arriba, JR; Muñoz, EA; Gil Divasson, P.; o.fl. Einkenni og spádómar um dauða meðal 4035 sjúklinga á sjúkrahúsi í röð með COVID-19 á Spáni. Clin. Örverur. Smitast. 2020, 26, 1525–1536. [Krossvísun]
37. Garcia-Perez, J.; Sanchez-Palomino, S.; Perez-Olmeda, M.; Fernandez, B.; Alcami, J. Ný stefna sem byggir á raðbrigðum vírusum sem tæki til að meta lyfjanæmi fyrir ónæmisbrestsveiru af tegund 1. J. Med. Virol. 2007, 79, 127–137. [CrossRef] [PubMed]
38. Ou, X.; Liu, Y.; Lei, X.; Li, P.; Mi, D.; Ren, L.; Guo, L.; Guo, R.; Chen, T.; Hu, J.; o.fl. Einkenni á toppglýkópróteini SARS-CoV-2 við innkomu vírusa og ónæmisvíxlvirkni þess við SARS-CoV. Nat. Samfélag. 2020, 11, 1–12. [CrossRef] [PubMed]
39. Volz, E.; Hill, V.; McCrone, JT; Verð, A.; Jørgensen, D.; O'Toole, Á.; Southgate, J.; Johnson, R.; Jackson, B.; Nascimento, FF; o.fl. Mat á áhrifum SARS-CoV-2 stökkbreytingar D614G á smithæfni og sjúkdómsvaldandi áhrif. Cell 2021, 184, 64–75. [Krossvísun]
40. Korber, B.; Fischer, WM; Gnanakaran, S.; Yoon, H.; Theiler, J.; Abfalterer, W.; Hengartner, N.; Giorgi, EE; Bhattacharya, T.; Foley, B.; o.fl. Að fylgjast með breytingum á SARS-CoV-2 toppi: Vísbendingar um að D614G eykur smitvirkni COVID-19 vírusins. Cell 2020, 182, 812–827. [Krossvísun]
41. Nandagopal, N.; Ali, AK; Komal, AK; Lee, S.-H. Mikilvægt hlutverk IL-15–PI3K–mTOR ferils í náttúrulegum drápsfrumuáhrifavirkni. Framan. Immunol. 2014, 5, 187. [Krossvísun]
42. Rosenthal, R.; Groeper, C.; Bracci, L.; Adamina, M.; Feder-Mengus, C.; Zajac, P.; Iezzi, G.; Bolli, M.; Weber, WP; Frey, DM; o.fl. Mismunandi svörun við IL-2, IL-7 og IL-15 algeng viðtakakeðju frumufrumur með mótefnavaka-sértækum útlægum blóði eða minni frumueyðandi CD8+ T frumum frá heilbrigðum gjöfum og Sortuæxlissjúklingar. J. Immunother. 2009, 32, 252–261. [Krossvísun]
43. Corman, VM; Landt, O.; Kaiser, M.; Molenkamp, R.; Meijer, A.; Chu, DKW; Bleicker, T.; Brünink, S.; Schneider, J.; Schmidt, ML; o.fl. Greining á 2019 nýrri kransæðaveiru (2019-nCoV) með rauntíma RT-PCR. Eurosurveillance 2020, 25, 2000045. [CrossRef] [PubMed]
44. HVER. Diagnostic Testing for SARS-CoV-2: Bráðabirgðaleiðbeiningar, 11. september 2020; Alþjóðaheilbrigðismálastofnunin: Genf, Sviss, 2020.
45. Becker, LA Áhrif Stærð (ES); Háskólinn í Colorado Colorado Springs: Colorado Springs, CO, Bandaríkin, 2000.
46. Cohen, J. Statistical Power Analysis for the Behavioral Sciences; Routledge: Abingdon, Bretlandi, 1988. [CrossRef]
47. Moreno-Perez, O.; Ribes, I.; Boix, V.; Martinez-García, M.; Otero-Rodriguez, S.; Reus, S.; Sánchez-Martínez, R.; Ramos, JM; Chico-Sánchez, P.; Merino, E. Sjúklingar á sjúkrahúsi með bylting COVID-19: Klínískir eiginleikar og léleg útkoma spá. Alþj. J. Infect. Dis. 2022, 118, 89–94. [CrossRef] [PubMed]
48. Lee, CM; Lee, E.; Park, WB; Choe, PG; Song, K.-H.; Kim, ES; Park, S.-W. Byltingarkennd COVID-19 sýking á ríkjandi tímabili Delta Variant: Þarf einstaklingsmiðaða umönnun byggða á bólusetningarstöðu. J. Korean Med. Sci. 2022, 37, e252. [CrossRef] [PubMed]
49. Ejaz, H.; Alsrhani, A.; Zafar, A.; Javed, H.; Junaid, K.; Abdalla, AE; Abosalif, KO; Ahmed, Z.; Younas, S. COVID-19 og fylgisjúkdómar: Skaðleg áhrif á sýkta sjúklinga. J. Infect. Lýðheilsa 2020, 13, 1833–1839. [CrossRef] [PubMed]
50. Azevedo, RB; Botelho, BG; de Hollanda, JVG; Ferreira, LVL; de Andrade, LZJ; Oei, SSML; Mello, TDS; Muxfeldt, ES COVID-19 og hjarta- og æðakerfið: Alhliða umfjöllun. J. Hum. Háþrýstingur. 2021, 35, 4–11. [Krossvísun]
51. Zhang, JJ; Lee, KS; Ang, LW; Leó, YS; Young, BE Áhættuþættir fyrir alvarlegan sjúkdóm og virkni meðferðar hjá sjúklingum sem eru sýktir af COVID-19: Kerfisbundin endurskoðun, meta-greining og meta-aðhvarfsgreining. Clin. Smitast. Dis. 2020, 71, 2199–2206. [Krossvísun]
52. Kermali, M.; Khalsa, RK; Pillai, K.; Ismail, Z.; Harky, A. Hlutverk lífmerkja við greiningu á COVID-19– Kerfisbundin úttekt. Lífvísindi. 2020, 254, 117788. [Krossvísun]
53. Malik, P.; Patel, U.; Mehta, D.; Patel, N.; Kelkar, R.; Akrmah, M.; Gabrilove, JL; Sacks, H. Lífvísar og niðurstöður COVID-19 sjúkrahúsinnlagna: Kerfisbundin endurskoðun og meta-greining. BMJ Evid. Byggt Med. 2021, 26, 107–108. [Krossvísun]
54. Li, Y.; Schneider, AM; Mehta, A.; Sade-Feldman, M.; Kays, KR; Gentili, M.; Charland, NC; Gonye, AL; Gushterova, I.; Khanna, HK; o.fl. SARS-CoV-2 veirublæðing tengist aðskildum próteindaferlum og spáir fyrir um útkomu COVID-19. J. Clin. Rannsaka. 2021, 131, e148635. [Krossvísun]
55. Rodríguez-Serrano, DA; Roy-Vallejo, E.; Cruz, NDZ; Ramírez, AM; Rodríguez-García, SC; Arevalillo-Fernández, N.; Galván-Roman, JM; García-Rodrigo, LF; Vega-Piris, L.; Llano, MC; o.fl. Greining á SARS-CoV-2 RNA í sermi tengist aukinni dánartíðni hjá COVID{10}} sjúklingum á sjúkrahúsi. Sci. Rep. 2021, 11, 13134. [Krossvísun]
56. Serafim, RB; Póvoa, P.; Souza-Dantas, V.; Kalil, AC; Salluh, JI Klínískt námskeið og niðurstöður bráðveikra sjúklinga með COVID-19 sýkingu: Kerfisbundin úttekt. Clin. Örverur. Smitast. 2021, 27, 47–54. [CrossRef] [PubMed]
57. Liu, X.; Zhou, H.; Zhou, Y.; Wu, X.; Zhao, Y.; Lu, Y.; Tan, W.; Yuan, M.; Ding, X.; Zou, J.; o.fl. Áhættuþættir sem tengjast alvarleika sjúkdómsins og lengd sjúkrahúsdvalar hjá COVID-19 sjúklingum. J. Infect. 2020, 81, e95–e97. [Krossvísun]
58. Luo, XH; Zhu, Y.; Maó, J.; Du, RC T frumu ónæmisfræði og frumustormur COVID-19. Scand. J. Immunol. 2021, 93, e12989. [CrossRef] [PubMed]
59. Harwood, O.; O'Connor, S. Meðferðarmöguleikar IL-15 og N-803 við HIV/SIV sýkingu. Veirur 2021, 13, 1750. [CrossRef] [PubMed]
60. Shin, H.; Wherry, truflun á EJ CD8 T frumu við langvarandi veirusýkingu. Curr. Opin. Immunol. 2007, 19, 408–415. [Krossvísun]
61. McMahan, K.; Yu, J.; Mercado, NB; Loos, C.; Tostanoski, LH; Chandrashekar, A.; Liu, J.; Pétur, L.; Atyeo, C.; Zhu, A.; o.fl. Fylgni verndar gegn SARS-CoV-2 í rhesus macaques. Náttúra 2021, 590, 630–634. [Krossvísun]
62. Zhuang, Z.; Lai, X.; Sun, J.; Chen, Z.; Zhang, Z.; Dai, J.; Liu, D.; Li, Y.; Li, F.; Wang, Y.; o.fl. Kortlagning og hlutverk T-frumuviðbragða í SARS-CoV-2-sýktum músum. J. Exp. Med. 2021, 218, e20202187. [Krossvísun]
63. Westmeier, J.; Paniskaki, K.; Karaköse, Z.; Werner, T.; Sutter, K.; Dolff, S.; Overbeck, M.; Limmer, A.; Liu, J.; Zheng, X.; o.fl. Skert frumudrepandi CD8+ T frumusvörun hjá öldruðum COVID-19 sjúklingum. MBio 2020, 11, e02243-20. [Krossvísun]
64. Laing, AG; Lorenc, A.; del Barrio, IDM; Das, A.; Fiskur, M.; Monin, L.; Muñoz-Ruiz, M.; McKenzie, DR; Hayday, TS; Francos Quijorna, I.; o.fl. Kraftmikil COVID-19 ónæmisundirskrift inniheldur tengsl með slæmar horfur. Nat. Med. 2020, 26, 1623–1635. [Krossvísun]
65. Kuri-Cervantes, L.; Pampena, MB; Meng, W.; Rosenfeld, AM; Ittner, CAG; Weisman, AR; Agyekum, RS; Mathew, D.; Baxter, AE; Vella, LA; o.fl. Alhliða kortlagning á ónæmistruflunum sem tengjast alvarlegu COVID-19. Sci. Immunol. 2020, 5, eabd7114. [Krossvísun]
66. Aktas, E.; Kucuksezer, UC; Bilgic, S.; Erten, G.; Deniz, G. Tengsl milli CD107a tjáningar og frumudrepandi virkni. Cell. Immunol. 2009, 254, 149–154. [Krossvísun]
67. Björkström, NK; Strunz, B.; Ljunggren, H.-G. Náttúrulegar drápsfrumur í veirueyðandi ónæmi. Nat. Séra Immunol. 2022, 22, 112–123. [CrossRef] [PubMed]
68. Bi, J. NK frumuvandamál hjá sjúklingum með COVID-19. Cell. Mol. Immunol. 2022, 19, 127–129. [CrossRef] [PubMed]
69. Alter, G.; Malenfant, JM; Altfeld, M. CD107a sem starfrænt merki til að bera kennsl á náttúrulega drápsfrumuvirkni. J. Immunol. Aðferðir 2004, 294, 15–22. [CrossRef] [PubMed]
70. Gustine, JN; Jones, D. Immunopathology of Hyperinflammation in COVID-19. Am. J. Clin. Pathol. 2021, 191, 4–17. [CrossRef] [PubMed]
71. Hann, C.; Zhou, Y.; Li, Z.; Farooq, MA; Ajmal, I.; Zhang, H.; Zhang, L.; Tao, L.; Yao, J.; Du, B.; o.fl. Samtjáning á IL-7 bætir CAR T frumumeðferð sem byggir á NKG2D við krabbameini í blöðruhálskirtli með því að auka stækkun og hindra frumudauða og þreytu. Krabbamein 2020, 12, 1969. [CrossRef]
