Mesenchymal stilkur/straumfrumuafleidd exósóm 2. hluti
May 31, 2022
Vinsamlegast hafðu sambandoscar.xiao@wecistanche.comfyrir meiri upplýsingar
4.2.T frumureglugerð
MSC-exósóm móta einnig virkni eða virkni T-frumna (tafla 3). Greint var frá því að BM-MSC-exósóm umbreyttu Th1 í Th2 og dragi úr Th17 aðgreiningu í PBMCs [97]. Meira um vert, BM-MSC-exósóm juku magn Tregs í PBMCs. Þessi áhrif gætu verið miðluð af bælingu bólgueyðandi frumudrepna eins og TNF- og IL-1 og aukningu á bólgueyðandi frumudrepni TGF- [9]. Önnur skýrsla leiddi einnig í ljós að BM-MSC-exósóm móta ónæmisviðbrögð í PBMC frá astmasjúklingum [98]. Útbreiðslu- og ónæmisbælingargeta Tregs var ýtt undir með BM-MSC-exósómum með uppstýringu IL-10 og TGF- 1 í PBMCs. Tregs voru einnig framkallaðir af exósómum úr TGF- /IFN- -örvuðum UC-MSCs 【99】.cynomorium bæturFyrirhugaður fyrirkomulag þessarar Treg reglugerðar er mótefnavaka-presenting cell (APC) - en ekki CD4 plús T frumuháð ferill [97]. Fyrri skýrsla sýndi fram á að aðgreining Tregs er miðlað af virkum APCs, sem er framkallað af ESC-MSC-exósómum á mergfrumugreiningar frumsvörun 88 (MYD88) háð [100]. Einnig hefur verið greint frá því að ASC-exósóm músa valdi aukningu á Tregs þýði í einkjarna frumum milta músa með streptósótósín af völdum sjálfsofnæmis sykursýki af tegund 1 [100]. Einnig hefur verið greint frá uppstýringu á Tregs í músatilraunalíkani með sjálfsofnæmisheilabólgu í músum með BM-MSC-exosomes [101], og concanavalin A(Con A)-framkallað mús lifrarskaða líkan af músum BM-MSC- exósóm [102]. Einnig hefur verið greint frá lækkun á útbreiðslu virkjana T- og B-eitilfrumna með BM-MSC-exósómum [103]. Athugið að rannsóknir Del Fattore o.fl. og Di Trapani o.fl. hafa sýnt að EV frá BM-MSC bæla T-frumufjölgun óbeint með því að örva Treg aðgreiningu, ólíkt MSCs, sem bæla beint T-frumufjölgun [103,104]. Að auki sýndu UC-MSC-EVs hreinsuð með stærðarútilokunarskiljun aðeins hamlandi áhrif á útbreiðslu T-frumna og framkallaði ekki frumuviðbragð og einfrumuskautun [105]. Frekari rannsókna er þörf til að skýra sameindakerfi þessara reglna með MSC-exósómum.

Vinsamlegast smelltu hér til að vita meira
4.3. Bólga í húð
Greint var frá því að BM-MSC-exósóm úr mönnum draga úr ljósöldrun og bólgu í músum, sem gæti verið gagnlegt til að koma í veg fyrir og meðhöndla húðöldrun [107]. Tilkynnt var um ASC-exósóm úr mönnum að auka nýæðamyndun og lifun húðflögunnar í IR meiðsli hjá rottum í flapígræðslulíkaninu með því að draga úr bólgu og frumudauða [108]. Í þessu tilraunaumhverfi höfðu ASC-exósóm fengnar úr H, O2-forskilyrðum ASC betri niðurstöður samanborið við þær frá óskilyrtum ASC. Stjórnun á bólgu er einnig mikilvæg til að meðhöndla ofnæmishúðbólgu (AD), sem er dæmigerður bólgusjúkdómur í húð. Sýnt hefur verið fram á að ASC-exósóm manna geta bætt AD í tveimur aðskildum múslíkönum með því að draga úr meinafræðilegum einkennum og tjáningu margra frumuefna eins og IL-4, IL-5, IL-13, IL -17, IL-23, IL-31, TNF-, IFNy og thymic stromal lymphopoietin (TSLP)[20,109]. Th2 cýtókín, eins og IL-4, IL-5, I-13 og IL-31, aðallega framleidd af virkum Th2 frumum, eru mikilvægir þættir í þróun ofnæmis bólga í húð [158,159].eyðimerkurhyacinthAthyglisvert er að Th2 cýtókín þ.mt IL-4, IL-13 og I-31 eru lækningaleg markmið fyrir AD[160]. Að auki drógu ASC-exósóm einnig úr íferð bólgueyðandi húðþekjufrumna (IDECs, CD86 plús og CD206 plús), sem leiddi til losunar bólgueyðandi frumudrepna í húðsjúkdómum AD[20]. Samanlagt eru MSC-exósóm lykilaðilar í endurnýjun húðar með því að stuðla að M2 skautun átfrumna með bólgueyðandi eiginleikum og draga úr bólgueyðandi frumum sem losa frumur eins og M1 átfrumna og IDECs.
4.4. Ónæmisstjórnun í öðrum bólgusjúkdómum
Einnig var greint frá ónæmisstillingu með MSC-exósómum í ýmsum bólgusjúkdómslíkönum. Dæmi eru sem hér segir: (1) Útlendingar frá melatónín-forskilyrðum rottum BM-MSCs minnkuðu nýrnaskaða í IR-nýrnaskaða líkani rotta með því að minnka oxunarálag og frumudauða, auka andoxunarefni og and-apoptotic prótein, og auka æðamyndun [ 110]. Að auki drógu BM-MSC-exósóm músa úr nýrnaskaða á CCR2-háðan hátt [111]. Einnig hefur verið greint frá því að UC-MSC-exósóm úr mönnum dragi úr bráðum nýrnaskaða af völdum cisplatíns (AKI) hjá rottum á sjálfsátháðan hátt [112]; (2)Mannleg UC-MSC-exósóm drógu úr sjálfsofnæmisæðabólgu í tilraunaskyni hjá rottum [ 113];(3) MSC (PL-MSC)-exósóm úr fylgju úr mönnum drógu úr bandvefsmyndun og bólgu í vefjum í Duchenne vöðvarýrnunarlíkani (DMD) mús, að hluta til með því að gefa miR-29c[114]; (4) Mannleg UC-MSC-exósóm bættu meinafræði lungna, hjarta og heila í nýburamúsum með BPD með því að draga úr lungnabólgu og lungnablöðru-háræðaleka hugsanlega með afhendingu TSG-6 [115] eða átfrumna M2 skautun [86];(5) Markviss sending BM-MSC-exósóma músa með hundaæðisveiru glýkópróteini (RVG) peptíð bætti vitræna virkni erfðabreyttra APP/PS1 músa með því að draga úr skelluútfellingu, magni A , virkjun stjarnfrumna og tjáningu bólgueyðandi frumudrepna TNF-, IL- og IL-6, en aukið l evels of IL-10, IL4, and IL-13 [116];(6) BM-MSC-EVs úr mönnum bættu taugafræðilega skerðingu og langtíma taugavernd hjá stoke músum með því að draga úr ónæmisbælingu eftir blóðþurrð. og eitilfrumnafæð, og auk þess að örva taugamyndun og æðamyndun [117]; og (7) Mús BM-MSC-exósóm lækkuðu þröskuldinn fyrir hitauppstreymi og vélrænni áreiti í músa sykursýki úttaugakvilla líkani með því að stjórna mörgum þáttum sem taka þátt í átfrumuskautun í gegnum afhending miRNA sem miða á TLR4/NF-kB merkjaleiðina [118].flavonoid útdráttaraðferð pdfAðrir bólgusjúkdómar, sem hægt er að stilla af MSC-exósómum eða MSC-EVs, eru OA [119,120], hrörnun milli hryggjarskífu (IVDD)[123], mænuskaða [124-126], hjartadrep [127,128], bráð lungnaskaði (ALI)[129-131], sjálfvakinn lungnatrefjun (IPF)[132], lifrar IR skaði [133], lifrartrefjun [134], bráð lifrarbilun [135], IBD [92,136], drepandi þarmabólga [137], ósæðarbólga í kviðarholi [1391.heilaáverka [139-143l, þvagrásarþrengsli [144l,status epilepticus (SE)[145,146], sjónhimnuáverka [147,148], blóðsýkingar [150] og ígræðslu-vers. -hýsilsjúkdómur(GvHD)[150]. Ónæmisstjórnun MSC-exósóma var lögð áhersla á í fyrstu klínísku notkun þeirra í ósamgena umhverfi fyrir sjúkling sem þjáist af steraþolnum GvHD [151]. Í þessari rannsókn breyttu MSC-exósóm stöðu ónæmisfrumna sjúklingsins. Aðgreining Tregs með MSC-exósóm miðlaðri APC virkjun gæti stuðlað að bælingu GvHD [99].

Cistanche getur gegn öldrun
Í stuttu máli, MSC-exósóm eða MSC-EVs bæla bólgusvörun í ýmsum sjúkdómsaðstæðum með því að framkalla skautun og aðgreining M2 átfrumna og Tregs. Þrátt fyrir að rannsaka þurfi nákvæma farmsamsetningu og MoA exósóma frekar, benda sífellt fleiri vísbendingar til þess að MSC-exósóm hafi svipaða bólgueyðandi og ónæmisbælandi eiginleika og MSCs, sem gætu verið gagnleg til meðferðar á bólgu- og sjálfsofnæmissjúkdómum, sem og fyrir húð endurnýjun. Hins vegar geta MSC-exósóm einnig haft mismunandi ónæmisbælandi kerfi en MSCs, sem þarf að útskýra frekar til að auðvelda notkun í klínískum aðstæðum.
5. Áhrif MSC-exósóma gegn öldrun
Öldrun, skilgreind sem óafturkræf hnignun lífeðlisfræðilegra ferla lífvera með tímanum, einkennist af níu einkennum: frumuöldrun, truflun á starfsemi hvatbera, óreglubundið næringarefnisskynjun, breytingar á erfðaefni, nötnun telómera, erfðafræðilegan óstöðugleika, breytt samskipti milli frumna og þreyta stofnfrumna [2161,16] ]. Meðal þeirra hefur nýlega verið lögð áhersla á frumuöldrun sem einn af lykilþáttunum í flóknu öldrunarferlinu þar sem hún er samtengd öðrum einkennum [163]. Aldrunarfrumur safnast fyrir í vefjum hryggdýra með aldrinum.flavonoidsAthyglisvert er að brottnám öldrunarfrumna í dýrum leiðir til seinkunar á aldurstengdum sjúkdómum [164-168]. Öldrunarskeið einkennist af stöðugu stöðvun frumuhrings í Gl fasa og bólgusvörun sem kallast öldrunartengd seytingarsvipgerð (SASP), sem breytir örumhverfinu í kringum öldrunarfrumur [161]. Öldrun er framkölluð af innanfrumu- og utanfrumuálagi, þar með talið eftirmyndunarálagi, DNA-skemmdum, krabbameinsgenavirkjun, telómeraskemmdum eða styttingu, bólgu, truflun á starfsemi hvatbera, oxunarálagi og lyfjamóðgunum, til að útrýma skemmdum frumum og koma í veg fyrir hugsanlega umbreytingu illkynja frumna [161,169] . Hlutar SASP eru meðal annars vaxtarþættir, bólgueyðandi frumudrep, chemokines og ensím sem breyta utanfrumu fylki [170-172]. SASP stuðlar að bólgu, hugtak sem Franceschi o.fl. árið 2000, sem lýsir lágstigs, stýrðri, einkennalausri, langvinnri og almennri bólgu sem tengist öldrunarferlum [173]. Reyndar benda margar vísbendingar á að bólga geti að lokum leitt til aldurstengdra sjúkdóma [174-176]. Þannig geta inngrip sem bæla SASP og bólguferli haft möguleika á að draga úr ýmsum langvinnum sjúkdómum [177]. Að auki sýna öldrunarfrumur tjáningu á öldrunartengdum -galaktósíðasa (SA- -gal), hækkun á mRNA/próteinum þar á meðal p53, p21, p16 og -H2AX, og minnkun á frumufjölgun 【161】.
5.1. Rafbílar í öldrun
EVs eða exosomes hafa hlutverk bæði við að flytja öldrunarsvipgerðina og létta eða jafnvel endurnýja öldrunarfrumur, allt eftir uppruna frumum þeirra. Rannsóknir benda til þess að EV eða exosomes virki sem nýir þættir SASP og aldurstengdra sjúkdómamerkja [169-171]. Tilkynnt hefur verið um aldurstengdar breytingar á EVs eða exósómum sem leiða til eftirfarandi: (1) aukningu á fjölda EVs eða exosomes sem losna við öldrun bandvefsfruma, þekjufrumna og krabbameinsfrumna [178.179]; (2) fækkun í magni rafbíla í dreifingu með aldrinum, að minnsta kosti frá 30 til 60 í mönnum, sem og í músum og rottum [180-182]; og (3) breytingar á EV eða exosome samsetningu (miRNA, prótein eða lípíð) sem tengjast öldrun eða öldrun [171,183-189]. Reyndar miðla EVs eða exosomes paracrine öldrun, senda öldrun frá öldruðum eða sjúkum frumum til eðlilegra frumna, bæði við eðlilegar aðstæður og sjúkdóma [169,190-195]. Þessi paracrine senescence er jákvæð fylgni við upptöku exósóma af markfrumum og er komið í veg fyrir með hömlun á exosome myndun [169].

Einnig hefur verið greint frá því að ýmis löng ókóðarandi RNA (ncRNA) eru auðguð á exosomes frá öldrunarfrumum og uppsafnaðar vísbendingar sýna að þessi RNA geta stuðlað að framgangi aldurstengdra sjúkdóma eins og æðakölkun, sykursýki af tegund 2, beinþynningu, OA, gigt. liðagigt, Parkinsonsveiki og MS [196]. Einnig hefur verið greint frá því að ýmis löng ókóðarandi RNA (ncRNA) auðgast á exosomes frá öldrunarfrumum og uppsafnaðar vísbendingar sýna að þessi RNA geta stuðlað að framgangi aldurstengdra sjúkdóma eins og æðakölkun, sykursýki af tegund 2, beinþynningu, OA, iktsýki, Parkinsonsveiki og MS. Til dæmis, í æðakölkun, stýra einfrumur sem verða fyrir oxuðu lágþéttni lípópróteini (oxLDL) framgangi sjúkdómsins. Rannsókn Chen o.fl. hefur sýnt að THP-1, einfrumufrumulína, meðhöndluð með oxLDL sýnir marktæka uppstýringu á exosomal lncRNA GAS5, og þessi exosomes valda apoptosis æðaþelsfrumna [197]. Hlutverk exosomal lncRNA var einnig undirstrikað af Ruan o.fl. Í þessari rannsókn kom í ljós að utanaðkomandi lncRNA-p3134 innihald hjá sykursýkissjúklingum var hærra en hjá einstaklingum sem ekki voru með sykursýki [198]. Öldrunarfrumur hafa einnig áhrif með því að flytja próteinfarm. Til dæmis, exosomes frá öldrunarmergæxlisfrumum af völdum lyfja stuðla að virkjun og fjölgun NK-frumna með því að flytja IL-15RA og IL-15 [199]. Samanlagt geta EV frá öldrunarfrumum þjónað sem sjúkdómsmerki.
5.2.Áhrif gegn öldrun
Það hefur verið fáránlegt að miðlar í blóðrás séu ábyrgir fyrir því að endurnýja marga vefi gamalla lífvera með vænisýki ungra lífvera [200]. Mjög nýlega var sýnt fram á að EV frá plasma ungra músa lengja líftíma gamalla músa með því að seinka öldrun með exosomal nikótínamíð fosfóríbósýltransferasa (en amp) [201]. Önnur rannsókn greindi einnig frá því að exósóm frá ungum músum gætu flutt miR-126b-5p í vef gamalla músa og snúið við tjáningu öldrunartengdra sameinda eins og p16, mTOR, IGF{{6 }}R og telómerasatengd gen þar á meðal Men1, Mre11a, Tep1, Terf2, Tert og Tnks, í öldruðum músum [202]. Önnur skýrsla leiddi í ljós að rafbílar fengnir úr sermi ungra músa dró úr bólgu í gömlum músum með því að endurnýja að hluta til öldruð T-frumu ónæmisþol [203]. Ígræðsla stofn-/forfrumna í undirstúku, sem voru erfðabreyttar til að lifa af öldrunartengda undirstúkubólgu, var tilkynnt til að valda seinkun á öldrun og lengingu líftíma hjá miðaldra músum [204].
Meira um vert, vaxandi vísbendingar benda til þess að hægt sé að draga úr eða snúa við öldrun frumna með rafbílum eða exósómum úr stofnfrumum (tafla 4) [205-214]. ASC-exósóm manna drógu úr ótímabærri öldrun æðaþelsforfrumna (EPC) af völdum hás glúkósa og jók sárheilun hjá rottum með sykursýki [205]. Í sömu rannsókn, oftjáning á kjarnaþætti erythroid 2-tengdum þáttum 2 (NRF2) í ASC-exósómum úr mönnum dró enn frekar úr ótímabæra öldrun EPCs og stuðlaði að sárheilun hjá sykursjúkum rottum með því að stilla tjáningu ýmissa próteina [205]. Þar sem hár glúkósa hjá sykursýkissjúklingum veldur hvarfgefnum súrefnistegundum (ROS) og bólgu, sem stuðlar að öldrun og skerðir virkni EPCs, getur minnkað öldrun EPCs af ASC-exosomes verið gagnleg til meðferðar á fótsárum af völdum sykursýki [205]. Það hefur einnig verið greint frá því að ASC-exósóm manna innihalda lncRNA MALAT1 og endurheimta virkni hreyfihegðunar með fækkun á heilaskaða í heilaberki í heilaáverkalíkani rotta [142]. Varðandi þetta leiddi rannsókn í ljós að MALATl tjáning minnkar í eldri músum og að meðferð á UC-MSC-exósómum manna sem innihalda MALAT1 kemur í veg fyrir öldrun í D-galaktósa (gal) meðhöndluðum músum og öldrun í H, O-meðhöndluðum H9C2 hjartavöðvum [ 206]. MALATl er einn af frambjóðendum til að vinna gegn öldrun í stofnfrumuafleiddum frumum þar sem MALAT1-hækkun í UC-MSCs afnumdi þessi áhrif UM-MSC-exósóma. Á sama hátt var vitað að utanaðkomandi miR-146a stjórnar öldrun MSCs á neikvæðan hátt með því að miða á NF-B merki [191]. Nýlega var greint frá því að miR-146a í AF-MSC-exósómum minnkaði bólgu af völdum LPS í trophoblastfrumum manna [215]. Einnig er vitað að miR-146a er auðgað á UC-MSC-exósómum manna með TNF- -formeðferð og miðlar bólgueyðandi áhrifum í þvagrásarlíkani rotta [145]. Andoxunarensím peroxiredoxins (PRDXs) var tilkynnt sem mjög auðgað í iPSC-EVs og BM-MSC-EVs [208]. Flutningur PRDXs með þessum rafbílum leiddi til þess að öldrun frumufyrirbæra minnkaði eins og aukningu á SA- -gal, p21, p53, IL-1, IL-6 og -H2AX bæði í endurteknum og erfðafræðilega framkallaða öldrunar MSCs 【209】.hesperidín notarAthyglisvert er að próteingreining leiddi í ljós að ASC-exósóm innihalda einnig PRDX eins og PRDX1, PRDX4 og PRDX6 [109]. Einnig var greint frá því að ASC-exósóm úr mönnum dragi úr IL-1 -framkallaðri öldrun í beinfrumum frá OA sjúklingum 【209】. Í þessari rannsókn lækkuðu ASC-exósóm ekki aðeins magn SA- -gal, -H2AX, og IL-6 prótein, en einnig magn prostaglandíns E2, oxunarálag og hvatberahimnugetu. Greint hefur verið frá því að miR-214 í exósómum kemur í veg fyrir öldrun æðaþelsfrumna með því að bæla tjáningu á ataxia telangiectasia stökkbreytt (ATM) prótein með því að miða á 3'-óþýtt svæði (UTR) mRNA þess [216]. Athyglisvert er að næsta kynslóð raðgreiningar (NGS) greining leiddi í ljós að ASC-exósóm innihalda einnig miR-214 (Ha o.fl. óbirt athugun).
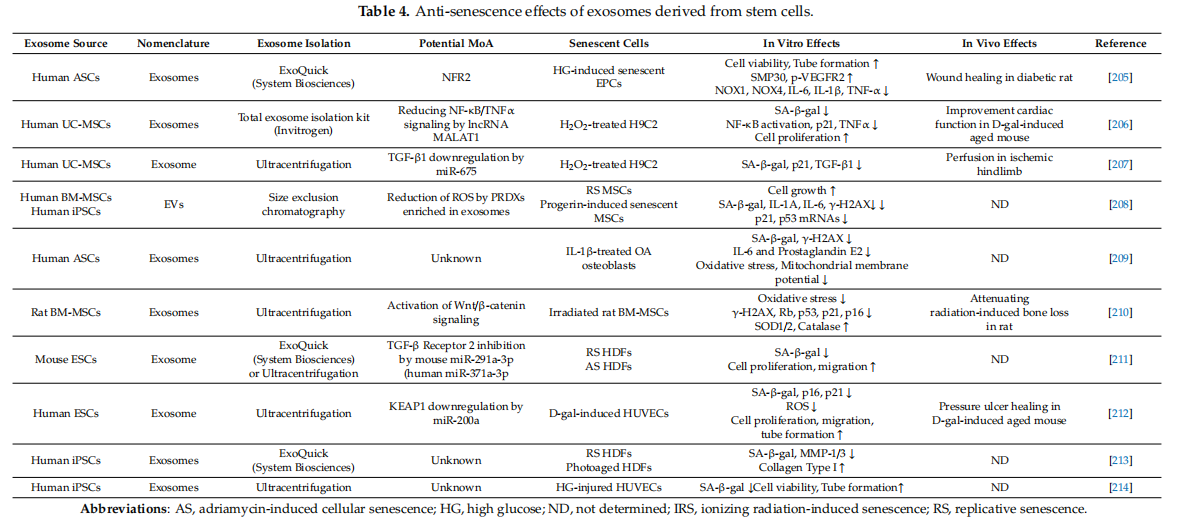
Mús miR-29la-3p var auðkennt til að miða við TGF- 2 viðtakann og sem farm af ESC-exósómum músa [211]. Meðhöndlun á ESC-exósómum músa dró úr SA- -gal tjáningu og stuðlaði að frumufjölgun og flutningi fjölfaldandi eða adriamycin-framkallaðra öldrunar HDFs [211]. Greint var frá því að ESC-exósóm úr mönnum hindruðu D-gal-framkallaða öldrun æðaþelsfrumna manna (HUVECs) [212]. Meðferð á ESC-exósómum leiddi til lækkunar á SA- -gal virkni, p16 og p21 próteingildum og ROS í HUVECs, og aukningu á frumufjölgun, flæði og slöngumyndun HUVECs. MiR-200a í ESC-exósómum minnkaði magn Kelch-líks ECH-tengds próteins 1 (KEAP1) með því að miða á 3'-UTR KEAP1 mRNA. Þar af leiðandi var magn NRF2, aðalstjórnandi af andoxunarviðbrögðum [217], var aukið til að framkalla tjáningu niðurstreymismarka þess eins og hem súrefnisasa 1 (HO1), súperoxíð dismútasa (SOD) og katalasa (CAT) [213]. ESC-exósóm ýttu undir lækningu á þrýstingssári í D-gal-völdum eldri músum með því að draga úr öldrun æðaþels og auka æðamyndun [212]. Tilkynnt var um iPSC-exósóm úr mönnum að vernda HDF frá UVB skemmdum, draga úr öldrunartengdri MMP-1/3 tjáningu og framkalla nýmyndun kollagens tegundar I bæði í UVB skemmdum og öldrunar HDF [214]. Einnig var greint frá því að iPSC-exósóm úr mönnum dragi úr SA- -gal og eykur lífvænleika frumna og slöngumyndun háglúkósaskaddaðra HUVECs með óþekktum aðferðum [214]. Exosomes frá ýmsum frumum eru einnig gagnlegar sem flutningstæki lífsameinda til að bæla öldrun. MiR-675 var uppgötvað sem merki um öldrun [207]. Sending miR-675 í gegnum UC-MSC-exósóm dró úr SA- -gal tjáningu og magn p21 og TGF- 1 próteina í H2O2-örvaði öldrunar H9C2 frumum með markvissa niðurstýringu á TGF- 1. Að auki, miR-675-UC-MCS-exósóm ýttu undir gegnflæði í blóðþurrð í afturlimum með því að hindra tjáningu bæði mRNA og próteina p21 og TGF- 1[207]. Önnur rannsókn greindi frá því að exósóm úr Wnt4-oftjáðum þekjuþekjufrumum í músum (TECs) hindruðu dexametasón-framkallaða öldrun svipgerða í TECs [218].

Samanlagt veita MSC-exósóm andstæðingur-öldrunaráhrif í gegnum einstakt miRNA, lncRNA og ensím innihald þeirra. Með því að örva fjölgun og draga úr SASP í öldruðum frumum, hafa þær mikla möguleika á að draga úr öldrunarfrumum í vefjum. Þar sem greint var frá því að fjarlæging öldrunarfrumna úr vefjum myndi skapa umhverfi sem stuðlar að endurnýjun [168] og vefjajafnvægi [166], gæti notkun MSC-exósóma til að fjarlægja öldrunarfrumurnar verið ákjósanleg aðferð til að örva endurnýjun eða endurnýjun vefja .
6. Húðsársgræðsla með MSC-Exosomes
Sár er tegund áverka á húð. Opið sár er af völdum rifs, skurðar eða gats og lokað sár stafar af barefli [219]. Húðsár má flokka í bráð og langvinn sár [220]. Bráð sár eru mjög algeng vegna taps á húð og húðþekju af völdum vélrænna, efnafræðilegra, líffræðilegra eða hitauppstreymisáverka. Langvinn sár eru aftur á móti algengir fylgisjúkdómar flókinna sjúkdóma eins og offitu, sykursýki og æðasjúkdóma. Fjórir flokkar langvinnra sára eru þrýstingssár, sykursýkissár, bláæðasár og slagæðasár samkvæmt Wound Healing Society [221]. Þar sem langvarandi sár gróa ekki innan þriggja mánaða eru þau talin vera sár sem ekki gróa [222,223]. Annað stórt læknisfræðilegt vandamál er sjúkleg sáragræðsla og örmyndun, sem valda bæði lífeðlisfræðilegum og sálrænum áskorunum [224]. Árlegur Medicare kostnaður við meðferð bráðra og langvinnra sára var áætlaður frá $ 28,1 til $ 96,8 milljarðar [225]. Að auki er áætlað að árlegur vörumarkaður fyrir sárameðferð nái 15 til 22 milljörðum dala árið 2024[225].
Sáragræðsla í húð er flókið ferli við að endurheimta slasaða húð. Það samanstendur af fjórum áföngum: jafnvægisstig, bólgu-, fjölgunar- og endurmótunarfasa [226-228]. Viðbrögð í þessum áföngum eru þétt samræmd til að tryggja mikilvæga húðhindranir [224]. Hins vegar hefur aðferð sárs í húð og samspil margs konar frumna á meðan sárgræðsluferlinu stendur aðeins verið afmarkað að hluta [229]. Margar frumugerðir hafa samskipti sín á milli í mjög háþróaðri röð meðan á sársgræðslu í húð stendur sem hér segir [230]: (1) blóðflögurnar hefja myndun blóðtappa, sem samanstanda af blóðflögum, rauðum blóðkornum og utanfrumu fylkissameindum í fyrsta homeostasis fasa;(2) daufkyrninga, einfrumur, sem og átfrumur eru helstu þátttakendur á bólgustiginu. Efnafræðilegir þættir sem gefa frá sér daufkyrninga draga að sér einfrumur og frumufrumur frá átfrumum og örva flæði trefjafruma til að komast inn á skaða staðinn frá eðlilegum vefjum í kring;(3) æðamyndun og æðamyndun æðaþelsfrumna veita súrefnisbirgðir til að styðja við útbreiðslu fluttra frumna í sárinu. staður á meðan á fjölgun stendur. Fibroblasts aðgreinast einnig í myofibroblasts til að mynda togstyrk í sárinu. Að auki seyta trefjafrumur vaxtarþáttum, sem virkja flutning og fjölgun keratínfrumna. Endurnýjun er lokið með því að stöðva flutning frumna með snertihömlun [230]; og (4) endurgerð með frumufrumu vefjafrumna, vöðvafrumna og annarra frumna, og niðurbrot á utanfrumu fylki á sér stað á meðan á endurgerð sársára stendur, sem spannar mánuði til ára. Skaðleg ör, af völdum afbrigðilegrar sáragræðslu, felur í sér langvarandi sár sem ekki gróa og sjúkleg ör eins og ofstækkun ör og keloids, og það hefur áhrif á milljónir manna um allan heim þar sem sem stendur er enginn árangursríkur meðferðarmöguleiki í boði [224]. Að koma í veg fyrir eða draga úr örum er einnig mikilvægt mál til að leysa í endurnýjandi fagurfræði [231].
MSC-EVs eða MSC-exosomes skipuleggja alla stiga sársheilunar í húð vegna getu þeirra til að móta bólgu, virkja flæði og fjölgun ýmissa frumna, þar á meðal ónæmisfrumna, trefjafrumur og keratínfrumna, og jafnvel bæta örmyndun (tafla 5) [85,87] ,88,205,226,231-245]. Sem dæmi var tilkynnt um algjöra endurþekjuvæðingu í húðsársgræðslulíkani fyrir kanínu með rafbílum frá kanínum ASC og BM-MSC með óþekktum vélbúnaði [232]. Einnig var greint frá ASC-EVs úr mönnum til að auka sár í húð hjá rottum [233].

6.1. Hom1eostasis Fasi
Á meðan á jafnvægisstiginu stendur verndar myndun blóðtappa af völdum blóðflagna slasaða staðinn. Hingað til hafa engar beinar vísbendingar verið fyrir hendi sem sýna þátttöku MSC-exósóma í blóðstorknun á meðan sár gróa. Nýleg niðurstaða gæti bent til hugsanlegs ávinnings af MSC-exósómum á blóðstorknun í sársgræðsluferlinu; Tilkynnt hefur verið um að UC-MSC-EV úr mönnum valdi blóðstorknun in vitro [244]. Hins vegar er þörf á frekari rannsóknum til að greina áhrif MSC-EV eða MSC-exósóma á blóðstorknun bæði við heilbrigða og sjúkdóma.
6.2.Bólgustig
Reglugerð bólgu er einnig mikilvæg í endurnýjun húðar á meðan sár gróa. Þrátt fyrir að bólga sé einn áfangi venjulegs húðviðgerðarfalls, er langvarandi bólga skaðleg og getur valdið of miklum örum [245]. Langvarandi bólga á sér stað aðallega í langvinnum sárum eða brunasárum [226,246] og það er mikilvægt að fara á viðeigandi hátt frá bólgustigum til fjölgunarfasa í eðlilegri sárgræðslu [247]. Átfrumur skipta sköpum í sársgræðsluferlinu, sem ætti að skipta á viðeigandi hátt úr M1 til M2 átfrumna [248,249]. M2 átfrumur hafa bólgueyðandi eiginleika, sem eru stuðlað að því að gera við sár á síðari stigum sársheilunar í húð [248,249]. Eins og fyrr segir stuðla MSC-exósóm að skautun átfrumna frá M1 til M2 í sáragræðslulíkönum í húð (sjá 4. Bólgueyðandi og ónæmisstýring með MSC-exósómum):(1) BM-MSC-exósóm manna og IM-MSC- exósóm stuðla að gróun sára í húð í músum með því að flytja miR-223[85]; (2) UC-MSC-exósóm manna ýttu undir lækningu á húðsárum af völdum sykursýki í rottum með því að gefa let-7b [88]; og (3) UC-MSC-exósóm úr mönnum jók sársheilun hjá rottum með alvarlega brunasár með miR-181c flutningi [88].
Þessi grein er dregin út úr Cells 2020, 9, 1157; doi:10.3390/cells9051157 www.mdpi.com/journal/cells
